X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻。X的核电荷数是Y的核外电子数的一半,Y与M可形成化合物M2Y。用微粒符号完成下列问题:
(1)Y、Z两种元素的最高价氧化物的水化物酸性___________ 强于___________ 。
(2)M、Z、Y形成的简单离子的半径的大小________________ 。
(3)M2X2固体中阴、阳离子个数比____________ ,其电子式为_______________ 。该物质中含有化学键的类型有______________ 和______________ 。
(4)将Z的单质通入YX2的水溶液中发生反应的离子方程式为____________ 。
(1)Y、Z两种元素的最高价氧化物的水化物酸性
(2)M、Z、Y形成的简单离子的半径的大小
(3)M2X2固体中阴、阳离子个数比
(4)将Z的单质通入YX2的水溶液中发生反应的离子方程式为
10-11高一下·福建漳州·期中 查看更多[1]
(已下线)2010-2011学年福建省长泰一中高一下学期期中考试化学试卷
更新时间:2016-12-09 01:46:15
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
【推荐1】周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增。R基态原子中,2p轨道上有2个未成对电子,最外层电子数是内层电子数的3倍。Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和。Z基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
(1)Z基态核外电子排布式为:_______ 。
(2)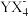 的空间构型是
的空间构型是_______ 。
(3)结构简式为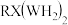 的化合物中R原子的杂化轨道类型为
的化合物中R原子的杂化轨道类型为_______ ;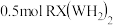 分子中含有
分子中含有 键数目为
键数目为_______ 。(H为氢元素,下同)
(4)往Z的硫酸盐溶液中通入过量的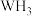 ,可生成
,可生成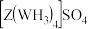 ,下列说法正确的是_______(填字母)。
,下列说法正确的是_______(填字母)。
(5)某Y与Z形成的化合物的晶胞如图所示(黑点代表Z原子)。
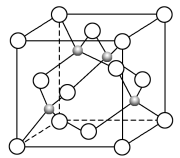
①该晶体的化学式为_______ 。
②已知Z和Y的电负性分别为1.9和3.0,则Y与Z形成的化合物属于_______ (填“离子”或“共价”)化合物。
③已知该晶体的密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体中Z原子和Y原子之间的最短距离为
,则该晶体中Z原子和Y原子之间的最短距离为_______  (只写计算式)(Z原子位于体对角线上)。
(只写计算式)(Z原子位于体对角线上)。
(1)Z基态核外电子排布式为:
(2)
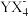 的空间构型是
的空间构型是(3)结构简式为
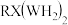 的化合物中R原子的杂化轨道类型为
的化合物中R原子的杂化轨道类型为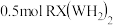 分子中含有
分子中含有 键数目为
键数目为(4)往Z的硫酸盐溶液中通入过量的
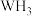 ,可生成
,可生成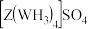 ,下列说法正确的是_______(填字母)。
,下列说法正确的是_______(填字母)。A.在 中 中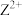 给出孤对电子, 给出孤对电子,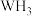 提供空轨道 提供空轨道 |
B.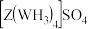 组成元素中第一电离能最大的是氧元素 组成元素中第一电离能最大的是氧元素 |
C.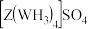 中所含的化学键有离子键、极性键和配位键 中所含的化学键有离子键、极性键和配位键 |
D. 分子内的 分子内的 键角大于 键角大于 分子内的 分子内的 键角 键角 |

①该晶体的化学式为
②已知Z和Y的电负性分别为1.9和3.0,则Y与Z形成的化合物属于
③已知该晶体的密度为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体中Z原子和Y原子之间的最短距离为
,则该晶体中Z原子和Y原子之间的最短距离为 (只写计算式)(Z原子位于体对角线上)。
(只写计算式)(Z原子位于体对角线上)。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】现有X、Y、Z三种非金属元素,A、B、C三种金属元素,有如下情况:
①X、Y、Z的单质在常温下均为气体。
②X的单质在Z的单质中燃烧,火焰呈苍白色。产物XZ的水溶液可使石蕊试液变红。
③2molX的单质可与1molY的单质化合生成2molX2Y,X2Y在常温下为液体。
④Z的单质溶于X2Y中所得的溶液具有漂白性。
⑤A的单质可以在Z的单质中燃烧,产生棕褐色的烟,生成的固体溶于水形成黄色溶液。
⑥B与Z形成的化合物BZ3溶于水后逐滴滴加NaOH溶液先生成白色沉淀后又逐渐溶解。
⑦C的单质与Y的单质发生反应可能得到两种产物,其中一种为淡黄色固体M。
请回答下列问题:
(1)A在元素周期表的位置_______ ,
(2)Z的单质溶于X2Y中所得的溶液中,起漂白作用的物质是(填化学式)_______ 。
(3)A的单质与Z的单质发生反应的化学方程式是_______ 。
(4)BZ3与过量的NaOH溶液发生反应的离子方程式是_______ 。
(5)X的单质与Z的单质的混合气体经点燃充分反应后,冷却至室温,再通入足量的NaOH溶液中,气体被完全吸收,求原混合气体中X的单质与Z的单质的体积比关系为_______ 。
①X、Y、Z的单质在常温下均为气体。
②X的单质在Z的单质中燃烧,火焰呈苍白色。产物XZ的水溶液可使石蕊试液变红。
③2molX的单质可与1molY的单质化合生成2molX2Y,X2Y在常温下为液体。
④Z的单质溶于X2Y中所得的溶液具有漂白性。
⑤A的单质可以在Z的单质中燃烧,产生棕褐色的烟,生成的固体溶于水形成黄色溶液。
⑥B与Z形成的化合物BZ3溶于水后逐滴滴加NaOH溶液先生成白色沉淀后又逐渐溶解。
⑦C的单质与Y的单质发生反应可能得到两种产物,其中一种为淡黄色固体M。
请回答下列问题:
(1)A在元素周期表的位置
(2)Z的单质溶于X2Y中所得的溶液中,起漂白作用的物质是(填化学式)
(3)A的单质与Z的单质发生反应的化学方程式是
(4)BZ3与过量的NaOH溶液发生反应的离子方程式是
(5)X的单质与Z的单质的混合气体经点燃充分反应后,冷却至室温,再通入足量的NaOH溶液中,气体被完全吸收,求原混合气体中X的单质与Z的单质的体积比关系为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】已知短周期元素 、
、 、
、 、
、 、
、 分布在三个周期,
分布在三个周期, 、
、 最外层电子数相同,物质
最外层电子数相同,物质 由原子序数依次增大的元素
由原子序数依次增大的元素 、
、 、
、 组成,其中
组成,其中 的简单离子半径在同周期中最小,
的简单离子半径在同周期中最小, 、
、 、
、 简单离子的核外电子排布相同,物质
简单离子的核外电子排布相同,物质 的结构式如下图所示:
的结构式如下图所示:
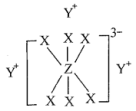
回答下列问题:
(1) 、
、 元素的中文名称为徐寿确定并使用至今,
元素的中文名称为徐寿确定并使用至今, 在周期表中的位置是
在周期表中的位置是___________ ,写出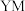 的电子式:
的电子式:___________ 。
(2) 、
、 、
、 、
、 简单离子的半径由大到小的顺序(用对应离子符号表示):
简单离子的半径由大到小的顺序(用对应离子符号表示):___________ 。
(3)在 ,与
,与 的混合液中,通入足量
的混合液中,通入足量 ,是工业制取
,是工业制取 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:___________ 。
(4)镓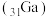 与
与 为同主族元素,氮化镓
为同主族元素,氮化镓 和砷化镓
和砷化镓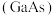 作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是___________ 。
a. 位于元素周期表第四周期ⅣA族
位于元素周期表第四周期ⅣA族
b. 为新型无机非金属材料
为新型无机非金属材料
c. 的最高价氧化物对应水化物的碱性比
的最高价氧化物对应水化物的碱性比 元素最高价氧化物对应水化物的碱性强
元素最高价氧化物对应水化物的碱性强
d.酸性:
②废弃的含 的半导体材料可以用浓硝酸溶解,生成
的半导体材料可以用浓硝酸溶解,生成 和
和 ,写出该反应的化学方程式为
,写出该反应的化学方程式为___________ 。
(5) 是有机合成的重要还原剂,其合成路线如图所示
是有机合成的重要还原剂,其合成路线如图所示
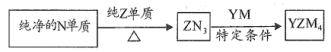
利用 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。
①其反应的化学方程式为___________ 。
②现设计如图四种装置测定 样品的纯度(假设杂质不参与反应)。
样品的纯度(假设杂质不参与反应)。
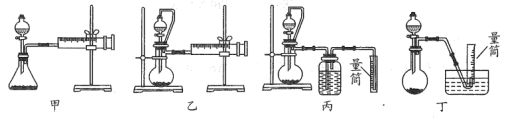
从简约性、准确性考虑,最适宜的方案是___________ (填编号)。
③取样品 ,若实验测得氢气的体积为
,若实验测得氢气的体积为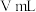 (标准状态),则
(标准状态),则 样品纯度为
样品纯度为___________ (用代数式表示)。
 、
、 、
、 、
、 、
、 分布在三个周期,
分布在三个周期, 、
、 最外层电子数相同,物质
最外层电子数相同,物质 由原子序数依次增大的元素
由原子序数依次增大的元素 、
、 、
、 组成,其中
组成,其中 的简单离子半径在同周期中最小,
的简单离子半径在同周期中最小, 、
、 、
、 简单离子的核外电子排布相同,物质
简单离子的核外电子排布相同,物质 的结构式如下图所示:
的结构式如下图所示: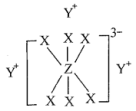
回答下列问题:
(1)
 、
、 元素的中文名称为徐寿确定并使用至今,
元素的中文名称为徐寿确定并使用至今, 在周期表中的位置是
在周期表中的位置是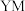 的电子式:
的电子式:(2)
 、
、 、
、 、
、 简单离子的半径由大到小的顺序(用对应离子符号表示):
简单离子的半径由大到小的顺序(用对应离子符号表示):(3)在
 ,与
,与 的混合液中,通入足量
的混合液中,通入足量 ,是工业制取
,是工业制取 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:(4)镓
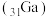 与
与 为同主族元素,氮化镓
为同主族元素,氮化镓 和砷化镓
和砷化镓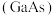 作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。①下列有关说法正确的是
a.
 位于元素周期表第四周期ⅣA族
位于元素周期表第四周期ⅣA族b.
 为新型无机非金属材料
为新型无机非金属材料c.
 的最高价氧化物对应水化物的碱性比
的最高价氧化物对应水化物的碱性比 元素最高价氧化物对应水化物的碱性强
元素最高价氧化物对应水化物的碱性强d.酸性:

②废弃的含
 的半导体材料可以用浓硝酸溶解,生成
的半导体材料可以用浓硝酸溶解,生成 和
和 ,写出该反应的化学方程式为
,写出该反应的化学方程式为(5)
 是有机合成的重要还原剂,其合成路线如图所示
是有机合成的重要还原剂,其合成路线如图所示
利用
 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。①其反应的化学方程式为
②现设计如图四种装置测定
 样品的纯度(假设杂质不参与反应)。
样品的纯度(假设杂质不参与反应)。
从简约性、准确性考虑,最适宜的方案是
③取样品
 ,若实验测得氢气的体积为
,若实验测得氢气的体积为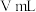 (标准状态),则
(标准状态),则 样品纯度为
样品纯度为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】已知X、Y、Z、M、Q、E为原子序数依次增大的前四周期元素,X的核外电子总数与其电子层数相同,Y元素基态原子中s电子总数与p电子总数相等,Z在元素周期表中电负性最大,M元素原子半径在同周期中最大,Q元素基态原子最外层电子排布式为 ,基态E原子d轨道中成对电子与成单电子的数目比为4∶3。回答下列问题:
,基态E原子d轨道中成对电子与成单电子的数目比为4∶3。回答下列问题:
(1)E在周期表中的位置为_______ ,其基态原子的价层电子的轨道表示式为_______ ;其基态原子的核外空间运动状态不同的电子有_______ 种。
(2)Y、Z、M、Q简单离子的半径由大到小的顺序(用对应离子符号表示)_______ 。
(3)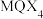 是有机合成的重要还原剂,利用
是有机合成的重要还原剂,利用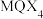 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定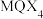 样品纯度。
样品纯度。
①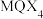 与水反应后的溶液中仅有一种溶质,且溶液显碱性,则
与水反应后的溶液中仅有一种溶质,且溶液显碱性,则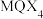 与水反应的化学方程式为
与水反应的化学方程式为_______ 。
②现设计如图四种装置测定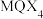 样品的纯度(即质量分数),假设杂质不参与反应。
样品的纯度(即质量分数),假设杂质不参与反应。
从简约性、准确性角度考虑,最适宜的方案是_______ (填编号)。
③取样品0.0100g,若实验测得氢气的体积为14.56mL(已换算为标准状况),则样品纯度为_______ 。
 ,基态E原子d轨道中成对电子与成单电子的数目比为4∶3。回答下列问题:
,基态E原子d轨道中成对电子与成单电子的数目比为4∶3。回答下列问题:(1)E在周期表中的位置为
(2)Y、Z、M、Q简单离子的半径由大到小的顺序(用对应离子符号表示)
(3)
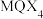 是有机合成的重要还原剂,利用
是有机合成的重要还原剂,利用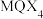 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定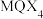 样品纯度。
样品纯度。①
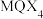 与水反应后的溶液中仅有一种溶质,且溶液显碱性,则
与水反应后的溶液中仅有一种溶质,且溶液显碱性,则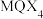 与水反应的化学方程式为
与水反应的化学方程式为②现设计如图四种装置测定
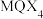 样品的纯度(即质量分数),假设杂质不参与反应。
样品的纯度(即质量分数),假设杂质不参与反应。
从简约性、准确性角度考虑,最适宜的方案是
③取样品0.0100g,若实验测得氢气的体积为14.56mL(已换算为标准状况),则样品纯度为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】现有A、B、C、D、E、F六种短周期元素,原子序数依次增大.已知A与D、C与E分别同主族,D、E、F同周期;A、B的最外层电子数之和与C的最外层电子数相等,A与C形成的化合物常温下均为液态,A分别与E、F形成的气体分子电子总数相等.
请回答下列问题:
(1)元素B在周期表中的位置是____________ ,元素D的原子结构示意图为__________ .
(2)A2C比A2E沸点高的原因是__________________________________ .
(3)在一定条件下,A、C的单质和A、C、D形成的离子化合物的水溶液可构成电池,该电池正极的电极反应式为_________________ ,负极的电极反应式为____________________ ,该电池在放电过程中,电解质溶液的pH将______ (填“增大”、“减小”或“不变”).
(4)化合物B2A4和B2C4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染.1mol B2A4与B2C4完全反应生成两种气体时放出热量516.8kJ,则该反应的热化学方程式为___________________________________________ .
请回答下列问题:
(1)元素B在周期表中的位置是
(2)A2C比A2E沸点高的原因是
(3)在一定条件下,A、C的单质和A、C、D形成的离子化合物的水溶液可构成电池,该电池正极的电极反应式为
(4)化合物B2A4和B2C4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染.1mol B2A4与B2C4完全反应生成两种气体时放出热量516.8kJ,则该反应的热化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】A、B、C、D、E五种短周期元素,原子序数依次增大,A、E 同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物,E2D2可用于呼吸面具或潜水艇中氧气的来源。请根据以上信息回答下列问题:
(1)BD2的电子式为___________________ 。
(2)EAB2D4水溶液显酸性的原因是________________________________________ 。
(3)等浓度的EABD3和E2BD3混合溶液中,各离子的离子浓度由大到小的顺序为________________ 。
(4)A、B、D、E 四种元素组成的某无机化合物,受热易分解。写出该化合物的溶液与足量的Ba(OH)2溶液反应的离子方程式____________________________________________ 。
(5)常温下,测得X 和Y的水溶液的pH均为5,则两种水溶液中由水电离出的H+浓度之比是__________ 。
(6)在一个装有可移动活塞的密闭容器中进行如下可逆反应:C2(g)+3A2 (g ) ⇌ 2CA3(g) ΔH=-92.4 kJ·mol-1。反应达到平衡后,测得容器中各物质的物质的量分别为C2 0.5mol、A2 0.2mol、CA3 0.2 mol,此时容器体积为1.0 L。
①实验室制备CA3的的化学方程式____________________________ 。
②如果保持温度和压强不变,向上述平衡体系中加入0.18molC2,平衡将__________ 移动(填“正向”、“逆向”或“不”)。
(1)BD2的电子式为
(2)EAB2D4水溶液显酸性的原因是
(3)等浓度的EABD3和E2BD3混合溶液中,各离子的离子浓度由大到小的顺序为
(4)A、B、D、E 四种元素组成的某无机化合物,受热易分解。写出该化合物的溶液与足量的Ba(OH)2溶液反应的离子方程式
(5)常温下,测得X 和Y的水溶液的pH均为5,则两种水溶液中由水电离出的H+浓度之比是
(6)在一个装有可移动活塞的密闭容器中进行如下可逆反应:C2(g)+3A2 (g ) ⇌ 2CA3(g) ΔH=-92.4 kJ·mol-1。反应达到平衡后,测得容器中各物质的物质的量分别为C2 0.5mol、A2 0.2mol、CA3 0.2 mol,此时容器体积为1.0 L。
①实验室制备CA3的的化学方程式
②如果保持温度和压强不变,向上述平衡体系中加入0.18molC2,平衡将
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】X、Y、Z、W四种短周期元素在元素周期表中的位置关系如图:
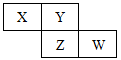
Ⅰ.若Z元素原子的最外层电子数是电子层数的2倍。
(1)写出铜和X的最高价氧化物的水化物的稀溶液反应的离子方程式:___________________ 。
(2)W最高价氧化物的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有14mol电子发生转移时,共产生4.5mol气体,则该反应的另一种气体产物的结构式为_____________ 。
Ⅱ.若Y和Z的核外电子数之和为22。
(3)Y的气态氢化物的电子式为_____________ ,实验室合成该物质的化学方程式为_____________________________________________ 。
(4)X的单质与W的最高价氧化物的水化物的浓溶液反应,当电子转移0.2mol时,产生气体的体积是__________ (标准状况)。

Ⅰ.若Z元素原子的最外层电子数是电子层数的2倍。
(1)写出铜和X的最高价氧化物的水化物的稀溶液反应的离子方程式:
(2)W最高价氧化物的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有14mol电子发生转移时,共产生4.5mol气体,则该反应的另一种气体产物的结构式为
Ⅱ.若Y和Z的核外电子数之和为22。
(3)Y的气态氢化物的电子式为
(4)X的单质与W的最高价氧化物的水化物的浓溶液反应,当电子转移0.2mol时,产生气体的体积是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】A、B、C、D、E是五种短周期元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
请回答下列问题:
(1)元素E在周期表中的位置为___________________________ ;
(2)把D的单质放到NaOH溶液中,反应的化学方程式为:_______________________ ;
(3)用电子式表示甲的形成过程:_________________________ ;
(4)在密闭容器中充入BC2、BC和乙的混合气体共mg,若加入足量Na2O2,充分振荡并不断用电火花点燃至反应完全,测得固体质量增重mg,则BC2与乙的体积比为________________ ;
(5)有200mL MgCl2和丙的混合溶液,其中c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1 NaOH 溶液的体积是:______ 。
| 物质组成 | 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素 原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
(1)元素E在周期表中的位置为
(2)把D的单质放到NaOH溶液中,反应的化学方程式为:
(3)用电子式表示甲的形成过程:
(4)在密闭容器中充入BC2、BC和乙的混合气体共mg,若加入足量Na2O2,充分振荡并不断用电火花点燃至反应完全,测得固体质量增重mg,则BC2与乙的体积比为
(5)有200mL MgCl2和丙的混合溶液,其中c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1 NaOH 溶液的体积是:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】有A、B、C、D、E、F、G7种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是____ ,B位于周期表中第____ 周期____ 族,C的原子结构示意图是________________ 。
(2)E的单质颜色是_______ 。
(3)A元素与D元素形成的化合物的电子式是_________ 。
(4)G的单质与水反应的化学方程式是________ 。
(5)F的元素符号是__________ 。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是_____ (填化学式,下同),酸性最强的是_______ ,气态氢化物最稳定的是__________ 。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是_______________ 。
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是
(2)E的单质颜色是
(3)A元素与D元素形成的化合物的电子式是
(4)G的单质与水反应的化学方程式是
(5)F的元素符号是
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】A、B、C、D、E、F是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐X;D与A同主族,且与F同周期;F元素的最外层电子数是其次外层电子数的3/4倍,A、B、D、F这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。D、E、F三种元素对应的最高价氧化物的水化物间两两皆能反应。
请回答下列问题:
(1)写出B、C、E元素的名称B_________ 、C___________ 、E____________ ;
(2)写出C、D两种元素形成的原子个数比为1:1的物质的电子式为_______________ ;
(3)可以验证C和F两种元素非金属性强弱的结论是(填编号)_________________ ;
①比较这两种元素的气态氢化物的沸点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
④比较这两种元素反应中得电子的多少
(4)向E的硝酸盐溶液中滴加过量D的最高价氧化物的水化物溶液,反应的离子方程式为____________ 。
(5)A、C、D、F四种元素可以形成两种酸式盐 均由四种元素组成
均由四种元素组成 ,这两种酸式盐的化学式分别为
,这两种酸式盐的化学式分别为_____ 、______ ,这两种酸式盐相互反应的离子方程式为______________________ 。
请回答下列问题:
(1)写出B、C、E元素的名称B
(2)写出C、D两种元素形成的原子个数比为1:1的物质的电子式为
(3)可以验证C和F两种元素非金属性强弱的结论是(填编号)
①比较这两种元素的气态氢化物的沸点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
④比较这两种元素反应中得电子的多少
(4)向E的硝酸盐溶液中滴加过量D的最高价氧化物的水化物溶液,反应的离子方程式为
(5)A、C、D、F四种元素可以形成两种酸式盐
 均由四种元素组成
均由四种元素组成 ,这两种酸式盐的化学式分别为
,这两种酸式盐的化学式分别为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】下表是元素周期表的一部分。
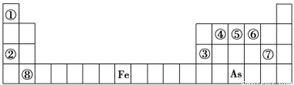
已知A、B、C、D、E、X、Y是由表中给出元素组成的常见单质或化合物,并存在如图所示的转化关系(部分生成物和反应条件已略去):
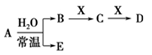
(1)元素⑧的最高价氧化物对应水化物的化学式是____________ 。
(2)元素⑤与As两种元素中,简单气态氢化物较稳定的是_______ (填化学式)。
(3)元素②⑥⑦的简单离子半径由大到小的顺序是_______ (用化学符号表示)。
(4)元素③的单质与元素②的最高价氧化物对应的水化物反应的离子方程式是__________________ 。
(5)若A为红棕色气体,则X、D的化学式分别为___________ 、___________ 。

已知A、B、C、D、E、X、Y是由表中给出元素组成的常见单质或化合物,并存在如图所示的转化关系(部分生成物和反应条件已略去):
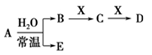
(1)元素⑧的最高价氧化物对应水化物的化学式是
(2)元素⑤与As两种元素中,简单气态氢化物较稳定的是
(3)元素②⑥⑦的简单离子半径由大到小的顺序是
(4)元素③的单质与元素②的最高价氧化物对应的水化物反应的离子方程式是
(5)若A为红棕色气体,则X、D的化学式分别为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】W、X、Y、Z为原子序数依次递增的短周期主族元素,W的单质是同条件下密度最小的气体,X、Y、Z为同一周期紧邻元素,M、R为同一主族的元素,M的单质常温为液态,R的单质常温为固态,且易升华。回答下列问题:
(1)写出下列元素的名称:W___ ;M____ 。
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:___ ;X、Y、Z的简单氢化物的沸点由高到低的顺序为__ (写化学式)。
②上述反应的离子方程式为___ 。
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,__ (填“能”或“不能”)发生,其原因是____ 。
②请写出R2与含YO32-溶液反应的离子方程式为____ 。
(1)写出下列元素的名称:W
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:
②上述反应的离子方程式为
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,
②请写出R2与含YO32-溶液反应的离子方程式为
您最近一年使用:0次



