下图为从海带中提取碘的工业生产过程,有关说法错误的是
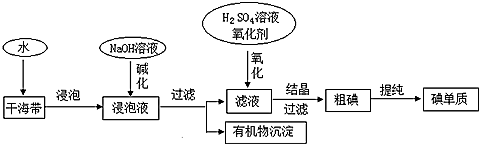

| A.因海水中蕴藏着极其丰富的碘元素,所以工业上也可以直接用海水来提取碘元素 |
| B.碱化操作时,加入NaOH溶液的原因是在碱性溶液中,可溶性有机质可形成沉淀 |
| C.在实验室进行氧化操作时,加入的氧化剂可以是新制氯水、双氧水等 |
| D.在实验室进行过滤操作时,需要用到玻璃仪器有玻璃棒、烧杯、漏斗 |
更新时间:2016-12-09 11:22:36
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】碲(52Te)被誉为“国防与尖端技术的维生素”;锡酸钠(Na2SnO3)可用于制造陶瓷电容器的基体。以锡碲渣(主要含Na2SnO3和Na2TeO3)为原料,回收锡酸钠并制备碲单质的流程图如下,下列说法错误的是
已知:锡酸钠(Na2SnO3)和亚碲酸钠(Na2TeO3)均易溶于碱。

已知:锡酸钠(Na2SnO3)和亚碲酸钠(Na2TeO3)均易溶于碱。

| A.在生产过程中,要将锡碲渣粉碎,其目的是增大锡碲渣的碱浸速率和浸出率 |
B.“氧化”时,反应的离子方程式为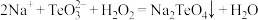 |
| C.“氧化”的温度应该越高越好,因为温度越高化学反应速率越快 |
D.以石墨为电极电解Na2TeO3溶液可获得Te,电解过程中阴极上的电极反应为: |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】某混合物可能含有Al、Cu、Fe2O3、Al2O3中的一种或几种,为探究该混合物成分,某小组设计方案如下。下列说法正确的是
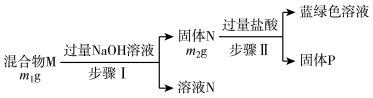

| A.已知m2<m1,则混合物中一定含有Al |
| B.蓝绿色溶液中含有的阳离子为Cu2+、Fe3+和 H+ |
| C.固体P一定是纯净物 |
| D.向溶液N中滴加足量盐酸,最终有白色沉淀生成 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
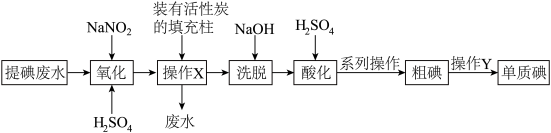
【推荐1】某学习小组按如下实验流程从海带中提取碘单质。

已知:3I2+6NaOH=5NaI+NaIO3+3H2O,根据以上流程,判断下列说法不正确 的是( )

已知:3I2+6NaOH=5NaI+NaIO3+3H2O,根据以上流程,判断下列说法
| A.方案甲采用蒸馏法不合理主要由于碘易升华,会导致碘的损失 |
| B.步骤X中,萃取后分液漏斗内观察到的现象为液体分上下两层,上层呈紫红色 |
| C.步骤Y中,应控制NaOH溶液的浓度和体积 |
| D.步骤Y的目的将碘转化成离子进入水层 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】海水中含有丰富的碘元素,海洋中许多藻类植物具有富集碘的能力,如海带中含碘量可达0.3%~0.5%,约为海水中碘浓度的10万倍。工业上可通过下列工艺流程从净化除氯后的含碘海水中提取 。
。

下列说法错误的是
 。
。
下列说法错误的是
| A.“富集”得到的含碘化合物为AgI |
B.“转化”后的溶液中主要含有 和 和 |
| C.用稀硝酸溶解滤渣Y得到的溶液可循环利用 |
D.为控制制备成本,“氧化”时应采取 |
您最近一年使用:0次





 +8H+=3I2+N2↑+4H2O
+8H+=3I2+N2↑+4H2O

