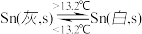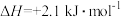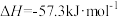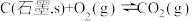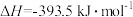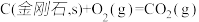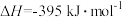已知下列数据:
Fe(s)+ O2(g)=FeO(s) △H=-272kJ·mol-1
O2(g)=FeO(s) △H=-272kJ·mol-1
2Al(s)+ O2(g)=Al2O3(s) △H=-1675kJ·mol-1
O2(g)=Al2O3(s) △H=-1675kJ·mol-1
则2Al(s) +3FeO(s)=Al2O3(s) + 3Fe(s)的△H是
Fe(s)+
 O2(g)=FeO(s) △H=-272kJ·mol-1
O2(g)=FeO(s) △H=-272kJ·mol-12Al(s)+
 O2(g)=Al2O3(s) △H=-1675kJ·mol-1
O2(g)=Al2O3(s) △H=-1675kJ·mol-1则2Al(s) +3FeO(s)=Al2O3(s) + 3Fe(s)的△H是
| A.+859 kJ·mol-1 | B.-859 kJ·mol-1 |
| C.-1403 kJ·mol-1 | D.-2491 kJ·mol-1 |
更新时间:2016/12/09 14:41:07
|
【知识点】 盖斯定律与热化学方程式解读
相似题推荐
单选题
|
适中
(0.65)
【推荐1】碱金属单质M和 反应的能量变化如下图所示。下列说法正确的是
反应的能量变化如下图所示。下列说法正确的是
 反应的能量变化如下图所示。下列说法正确的是
反应的能量变化如下图所示。下列说法正确的是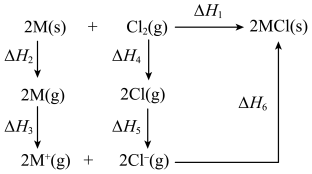
| A.CsCl晶体是共价晶体 |
B. |
C.若M分别为Na和K,则 :Na<K :Na<K |
D.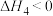 , ,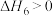 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,将1mol Na2CO3·10H2O(s)溶于水会使溶液温度升高,热效应为∆H1,将1mol Na2CO3(s)溶于水会使溶液温度升高,热效应为∆H2;Na2CO3·10H2O(s)受热分解的化学方程式为Na2CO3·10H2O(s) Na2CO3(s)+10H2O(l),热效应为∆H3。则下列判断正确的是
Na2CO3(s)+10H2O(l),热效应为∆H3。则下列判断正确的是
 Na2CO3(s)+10H2O(l),热效应为∆H3。则下列判断正确的是
Na2CO3(s)+10H2O(l),热效应为∆H3。则下列判断正确的是| A.∆H2<∆H3 | B.∆H1>∆H3 | C.∆Hl+∆H3=∆H2 | D.∆H1+∆H2>∆H3 |
您最近一年使用:0次

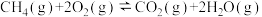
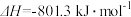
 的燃烧热
的燃烧热 为-801.3
为-801.3