有下列转化关系: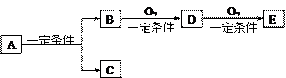
(1)若C是可用于自来水消毒的气体,A生成的B的反应为工业上冶炼金属B的反应,反应条件为电解,D、E是氧化物,D转化为E时增加氧的质量是总质量的25.8%,则写出A在一定条件下生成的C方程式_________________ , E的电子式为______________ ;
(2)若E是酸酐,且为无色易挥发的晶体,A为气态氢化物,则A与D反应生成B的化学方程式为_________________ 。
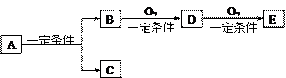
(1)若C是可用于自来水消毒的气体,A生成的B的反应为工业上冶炼金属B的反应,反应条件为电解,D、E是氧化物,D转化为E时增加氧的质量是总质量的25.8%,则写出A在一定条件下生成的C方程式
(2)若E是酸酐,且为无色易挥发的晶体,A为气态氢化物,则A与D反应生成B的化学方程式为
9-10高二下·河北衡水·期末 查看更多[1]
(已下线)2009—2010学年衡水中学高二下学期期末考试化学
更新时间:2016-12-09 00:41:30
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)L的元素符号为______ ;M在元素周期表中的位置为_____ ;Z元素的最高正价和最低负价分别为________ 、________ ,它的氢化物和最高价氧化物对应水化物的化学式分别是__________ 、__________ 。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为____ ,B的结构式为_____ 。
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子原子结构示意图为_________ 。
(4)五种元素的原子半径从大到小的顺序是_____________ (用元素符号表示)。
(5)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构。用电子式表示羰基硫分子:___________________ .
(6)写出由X、Z、L三种元素组成的离子化合物与稀NaOH溶液反应的离子方程式:___________________________________ 。
(1)L的元素符号为
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子原子结构示意图为
(4)五种元素的原子半径从大到小的顺序是
(5)羰基硫(COS)分子结构与二氧化碳分子结构相似,所有原子的最外层都满足8电子结构。用电子式表示羰基硫分子:
(6)写出由X、Z、L三种元素组成的离子化合物与稀NaOH溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知六种短周期主族元素A、B、C、D、E、F的原子序数依次增大,A是短周期中原子半径最小的元素,A、D同主族,C、F同主族,A和B可形成5核10电子的阳离子,C与D形成的离子化合物 中所有离子的电子数相同,E的最高价氧化物的水化物可与D、F的最高价氧化物的水化物反应,试回答下列问题:
中所有离子的电子数相同,E的最高价氧化物的水化物可与D、F的最高价氧化物的水化物反应,试回答下列问题:
(1)F在元素周期表中的位置是_______ 。
(2)写出A和B形成的一种18电子的分子的电子式_______ 。
(3)C、D、F的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(4)用电子式表示A、D形成化合物的过程_______ 。
(5)多原子分子具有一定的空间结构,如 的空间结构是直线形。A、C形成的简单氢化物的空间结构是
的空间结构是直线形。A、C形成的简单氢化物的空间结构是_______ ,其中含有的化学键类型为_______ 。
(6)E的单质与D的最高价氧化物的水化物反应的离子方程式为_______ 。
 中所有离子的电子数相同,E的最高价氧化物的水化物可与D、F的最高价氧化物的水化物反应,试回答下列问题:
中所有离子的电子数相同,E的最高价氧化物的水化物可与D、F的最高价氧化物的水化物反应,试回答下列问题:(1)F在元素周期表中的位置是
(2)写出A和B形成的一种18电子的分子的电子式
(3)C、D、F的简单离子半径由大到小的顺序为
(4)用电子式表示A、D形成化合物的过程
(5)多原子分子具有一定的空间结构,如
 的空间结构是直线形。A、C形成的简单氢化物的空间结构是
的空间结构是直线形。A、C形成的简单氢化物的空间结构是(6)E的单质与D的最高价氧化物的水化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期元素A、B、C、D、E的原子序数依次增大。A、B、C三种元素原子核外电子层数之和是5;A、B两元素原子最外层电子数之和等于C元素原子最外层电子数;B元素原子最外层上的电子数是其电子层数的2倍,A和C可以形成化合物CA3;B与D的原子序数之比为3∶4;E元素原子最外层电子数比次外层电子数少1。请回答:
(1)由A、B两种元素组成的分子有多种,其中一种分子含10个电子,写出其电子式_______ 。
(2)化合物甲由A、B、C、D四种元素组成,既可以与盐酸反应又可以与NaOH溶液反应,且甲为无机正盐,其化学式为____________ ,该物质含有的化学键为____________ 。
(3)A和D按1:1形成的化合物的电子式_____________ ,写出由该物质制备D的一种常见单质的反应的化学方程式______________________ ;
(4)下列说法中正确的是____________ 。
①质子数相同的粒子一定属于同一种元素 ②电子数相同的粒子不一定是同一种元素 ③两个原子如果核外电子排布相同,一定是同一种元素 ④质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子 ⑤所含质子数和电子数相等的粒子一定是原子 ⑥同种元素的原子的质量数必相等
A.①②④ B.②③④ C.③④⑥ D.①⑤⑥
(5)有关H、D、T、HD、H2、D+、H-这七种微粒的说法正确的是_______ 。
A.互为同位素 B.是七种氢元素 C.电子数相同 D.HD和H2均是单质
(1)由A、B两种元素组成的分子有多种,其中一种分子含10个电子,写出其电子式
(2)化合物甲由A、B、C、D四种元素组成,既可以与盐酸反应又可以与NaOH溶液反应,且甲为无机正盐,其化学式为
(3)A和D按1:1形成的化合物的电子式
(4)下列说法中正确的是
①质子数相同的粒子一定属于同一种元素 ②电子数相同的粒子不一定是同一种元素 ③两个原子如果核外电子排布相同,一定是同一种元素 ④质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子 ⑤所含质子数和电子数相等的粒子一定是原子 ⑥同种元素的原子的质量数必相等
A.①②④ B.②③④ C.③④⑥ D.①⑤⑥
(5)有关H、D、T、HD、H2、D+、H-这七种微粒的说法正确的是
A.互为同位素 B.是七种氢元素 C.电子数相同 D.HD和H2均是单质
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
真题
【推荐1】各物质之间的转换关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,l有漂白作用,反应①常用于制作印刷电路板。
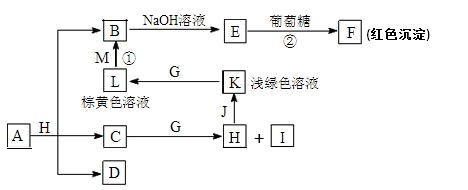
请回答下列问题:
(1)写出A的化学式_________ , C的电子式_________ 。
(2)比较Y与Z的原子半径大小________ >_______ (填写元素符号)。
(3)写出反应②的化学方程式(有机物用结构简式表示)________ ,举出该反应的一个应用实例_________ 。
(4)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体。请写出该反应的化学方程式_______________ 。
(5)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其2种同素异形体的名称______ 、______ 、______ 。

请回答下列问题:
(1)写出A的化学式
(2)比较Y与Z的原子半径大小
(3)写出反应②的化学方程式(有机物用结构简式表示)
(4)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体。请写出该反应的化学方程式
(5)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其2种同素异形体的名称
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
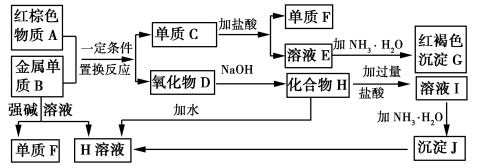
请回答下列问题:
(1)物质A的化学式为____________________ 。
(2)写出单质B与强碱溶液反应的离子方程式_______________ ,氧化物D与NaOH溶液反应的化学方程式________________________________ 。
(3)溶液E中加入氨水时,先生成白色沉淀L,L最终变为红褐色沉淀G,写出L变为G的化学反应方程式__________________________________ 。
(4)溶液E敞口放置容易变质,写出检验溶液E是否变质的实验操作、现象及结论__________ ,为了防止溶液E的变质,可往溶液中加入___________________ 。
(5)溶液I中所含金属离子是____________ 。

请回答下列问题:
(1)物质A的化学式为
(2)写出单质B与强碱溶液反应的离子方程式
(3)溶液E中加入氨水时,先生成白色沉淀L,L最终变为红褐色沉淀G,写出L变为G的化学反应方程式
(4)溶液E敞口放置容易变质,写出检验溶液E是否变质的实验操作、现象及结论
(5)溶液I中所含金属离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下图表示各物质之间的转化关系。已知A、D、F、H均为单质,X常温下为液体,B为淡黄色固体,J溶于酸得到黄色溶液

请按要求填空:
(1)写出生成E的电极反应式:_______________________
反应⑤的现象是:__________________________________________________
(2)反应①的化学反应方程式:_____________________________________
在实验室中引发反应④的操作是:_______________________________
(3)I和G溶液反应的化学方程式:__________________________________________

请按要求填空:
(1)写出生成E的电极反应式:
反应⑤的现象是:
(2)反应①的化学反应方程式:
在实验室中引发反应④的操作是:
(3)I和G溶液反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】亚硫酸钠用途广泛,可作漂白剂、显影剂、防护剂等。近年来,以SO2、NH3和NaCl为原料生产无水亚硫酸钠的新方法得到发展。生产流程如图所示:

完成下列填空:
(1)中学化学实验室实现上述流程中“分离器”作用的操作名称是:_________ ;所需玻璃仪器有___________________________ 。
(2)“反应液1”是由SO2通入14.8%氨水形成的亚硫酸铵溶液,在60℃~80℃时,不断搅拌,加入NaCl细晶体,就有无水亚硫酸钠析出,析出无水亚硫酸钠的离子反应方程式为____________________________ 。
(3)在“反应液2”通入足量SO2后,溶液中的阴离子除OH-外还有:_______________ ;在“反应液3”中通入足量NH3的目的是:__________________________________________ 。
(4)该生产方法的原料利用率(每制100g无水亚硫酸钠,各物质的消耗量及副产品物量)如表:
副产品NH4Cl的理论值a为:_________ ;它与NH4Cl实际值有差别的可能原因是:_________________ 。
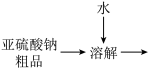
(5)无水亚硫酸钠粗品常用重结晶的方法进行精制,请完善以下能实现物料循环的精制亚硫酸钠操作的流程图。______________

完成下列填空:
(1)中学化学实验室实现上述流程中“分离器”作用的操作名称是:
(2)“反应液1”是由SO2通入14.8%氨水形成的亚硫酸铵溶液,在60℃~80℃时,不断搅拌,加入NaCl细晶体,就有无水亚硫酸钠析出,析出无水亚硫酸钠的离子反应方程式为
(3)在“反应液2”通入足量SO2后,溶液中的阴离子除OH-外还有:
(4)该生产方法的原料利用率(每制100g无水亚硫酸钠,各物质的消耗量及副产品物量)如表:
| 原料 | 理论值 | 实际值 | 利用率 |
| SO2 | 80.79 | 54.4 | 93.36% |
| NaCl | 92.86 | 101.0 | 91.94% |
| NH3 | 26.98 | 30.5 | 88.46% |
| 副产品NH4Cl | a | 87.1 | …… |
副产品NH4Cl的理论值a为:
(5)无水亚硫酸钠粗品常用重结晶的方法进行精制,请完善以下能实现物料循环的精制亚硫酸钠操作的流程图。

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫代硫酸钠晶体(Na2S2O3·5H2O)俗名“大苏打”。已知它易溶于水,难溶于乙醇,在中性或碱性环境中稳定,受热、遇酸易分解。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:
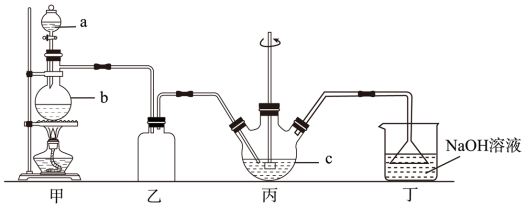
(1)装置甲中,a仪器的名称是_______ ;a中盛有浓硫酸,b中盛有亚硫酸钠,实验中要控制SO2生成速率,可以采取的措施有_______ (写出一条即可)
(2)装置乙的作用是_______
(3)装置丙中,将Na2S和Na2CO3以2:1的物质的量之比配成溶液再通入SO2,便可制得Na2S2O3和CO2。写出反应的化学方程式:_______
(4)本实验所用的Na2CO3中含有少量NaOH,检验含有NaOH的实验方案为_______ 。
[实验中供选择的试剂及仪器:CaCl2溶液、Ca(OH)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管。提示:室温时CaCO3饱和溶液的PH=9.5]
(5)反应结束后过滤丙中的混合物,滤液经蒸发、结晶、过滤、洗涤、干燥等得到产品,生成的硫代硫酸钠粗品可用_______ 洗涤。为了测定粗产品中Na2S2O3·5H2O的含量,采用在酸性条件下用KMnO4标准液滴定的方法(假设粗产品中的杂质与酸性KMnO4溶液不反应)。称取1.50g粗产品溶于水,用0.20 mol/L 的KMnO4溶液(加适量稀硫酸酸化)滴定,当溶液中S2O 被氧化为SO
被氧化为SO 时消耗高锰酸钾溶液的体积为40.00mL。则产品中Na2S2O3·5H2O的质量分数为
时消耗高锰酸钾溶液的体积为40.00mL。则产品中Na2S2O3·5H2O的质量分数为_______ (保留小数点后一位)

(1)装置甲中,a仪器的名称是
(2)装置乙的作用是
(3)装置丙中,将Na2S和Na2CO3以2:1的物质的量之比配成溶液再通入SO2,便可制得Na2S2O3和CO2。写出反应的化学方程式:
(4)本实验所用的Na2CO3中含有少量NaOH,检验含有NaOH的实验方案为
[实验中供选择的试剂及仪器:CaCl2溶液、Ca(OH)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管。提示:室温时CaCO3饱和溶液的PH=9.5]
(5)反应结束后过滤丙中的混合物,滤液经蒸发、结晶、过滤、洗涤、干燥等得到产品,生成的硫代硫酸钠粗品可用
 被氧化为SO
被氧化为SO 时消耗高锰酸钾溶液的体积为40.00mL。则产品中Na2S2O3·5H2O的质量分数为
时消耗高锰酸钾溶液的体积为40.00mL。则产品中Na2S2O3·5H2O的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】Na2S2O5常用作纺织业棉麻脱氯剂;酸化时可放出SO2气体。其制备工艺流程
如下:
(1)Na2S2O5的名称为_______________ (选填“焦硫酸钠”或“焦亚硫酸钠”)。
(2)“反应I ”中应先通入的气体是______ ,反应后析出的固体产物是____________ 。
(3)“反应Ⅱ”的化学方程式为_________________________ 。
(4)若反应条件或用量等控制不当,则所得的Na2S2O5产品中往往含有杂质。
①若产品中含有杂质Na2SO3,其具体原因可能是______________ (任答一条即可);
②若检验产品中含有杂质Na2CO3,下列试剂的使用顺序依次为_________ (填编号)。
a.稀硫酸 b.澄清石灰水 c.品红溶液 d.酸性KMnO4溶液
(5)Na2S2O3也可用作棉麻的脱氯剂。
①Na2S2O5溶液与Cl2反应的离子方程式为____________________ ;
②Na2S2O5与Na2S2O3脱氯等效时,消耗二者的质量之比为____________ 。
如下:

(1)Na2S2O5的名称为
(2)“反应I ”中应先通入的气体是
(3)“反应Ⅱ”的化学方程式为
(4)若反应条件或用量等控制不当,则所得的Na2S2O5产品中往往含有杂质。
①若产品中含有杂质Na2SO3,其具体原因可能是
②若检验产品中含有杂质Na2CO3,下列试剂的使用顺序依次为
a.稀硫酸 b.澄清石灰水 c.品红溶液 d.酸性KMnO4溶液
(5)Na2S2O3也可用作棉麻的脱氯剂。
①Na2S2O5溶液与Cl2反应的离子方程式为
②Na2S2O5与Na2S2O3脱氯等效时,消耗二者的质量之比为
您最近一年使用:0次



