某温度时,在2L密闭容器中,X、Y、Z 三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
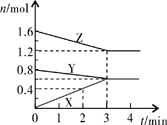
(1)该反应的化学方程式:____________ ;
(2)反应开始至2min末,X的反应速率为______ (mol·L-1·min-1);
(3)3min后图中曲线所表示的含义是______ 。

(1)该反应的化学方程式:
(2)反应开始至2min末,X的反应速率为
(3)3min后图中曲线所表示的含义是
9-10高一下·河南焦作·期末 查看更多[3]
(已下线)2010年河南省焦作市高一下学期期末测试化学(必修2)试题(已下线)2010年山东省聊城四中高一第二学期期末考试化学试题(已下线)2011-2012学年海南省海南中学高一下学期期末考试化学试卷
更新时间:2016-12-09 00:43:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某温度下,在 密闭容器中
密闭容器中 三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图.据图回答:
三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图.据图回答:
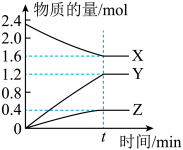
(1)该反应的化学方程式可表示为___________ .
(2)反应起始至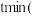 设
设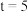 ),
), 的平均反应速率是
的平均反应速率是___________ , 的转化率为
的转化率为___________ (用百分数表示);在此温度下,该反应的平衡常数是___________ .
(3)下列可判断反应已达到平衡状态的是___________ .
A.X、Y、Z的反应速率相等
B.体系的压强保持不变
C.混合气体的密度不变
D.生成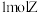 的同时生成
的同时生成
E.混合气体的平均分子质量不变
(4)一定能使该反应的反应速率增大的措施有___________ .
A.其他条件不变,及时分离出产物
B.适当降低温度
C.其他条件不变,增大 的浓度
的浓度
D.保持温度不变,将容器体积压缩为
E.恒容条件下冲入氦气,使压强增大
F.加入合适的催化剂
 密闭容器中
密闭容器中 三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图.据图回答:
三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图.据图回答:
(1)该反应的化学方程式可表示为
(2)反应起始至
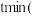 设
设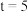 ),
), 的平均反应速率是
的平均反应速率是 的转化率为
的转化率为(3)下列可判断反应已达到平衡状态的是
A.X、Y、Z的反应速率相等
B.体系的压强保持不变
C.混合气体的密度不变
D.生成
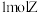 的同时生成
的同时生成
E.混合气体的平均分子质量不变
(4)一定能使该反应的反应速率增大的措施有
A.其他条件不变,及时分离出产物
B.适当降低温度
C.其他条件不变,增大
 的浓度
的浓度D.保持温度不变,将容器体积压缩为

E.恒容条件下冲入氦气,使压强增大
F.加入合适的催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】脱硝技术是处理氮氧化物的有效方法之一。在1 L的恒容密闭容器中充入2 mol NH3、1 mol NO和1 mol NO2,发生反应:2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g) ΔH。在不同温度下发生上述反应,测得N2的物质的量(mol)与时间的关系如下表:
2N2(g)+3H2O(g) ΔH。在不同温度下发生上述反应,测得N2的物质的量(mol)与时间的关系如下表:
回答下列问题:
(1)T1____ (填“>”“<”或“=”)T2,理由是_______ 。
(2)平衡后,增大压强反应向____ (填“正”或“逆”,下同)反应方向移动,升高温度反应向____ 反应方向移动。
(3)T1 K下,0~20 min内v(NO)=____________ 。
(4)T2 K下,NO2的平衡转化率为____ 。
 2N2(g)+3H2O(g) ΔH。在不同温度下发生上述反应,测得N2的物质的量(mol)与时间的关系如下表:
2N2(g)+3H2O(g) ΔH。在不同温度下发生上述反应,测得N2的物质的量(mol)与时间的关系如下表:| 0 min | 10 min | 20 min | 30 min | 40 min | |
| T1 K | 0 | 0.6 | 1.1 | 1.5 | 1.5 |
| T2 K | 0 | 0.8 | 1.4 | 1.4 | 1.4 |
回答下列问题:
(1)T1
(2)平衡后,增大压强反应向
(3)T1 K下,0~20 min内v(NO)=
(4)T2 K下,NO2的平衡转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】298K时,将20mL3xmol•L-1Na3AsO3、20mL3xmol•L-1I2和20mLNaOH溶液混合,发生反应:AsO (aq)+I2(aq)+2OH-(aq)
(aq)+I2(aq)+2OH-(aq) AsO
AsO (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
(aq)+2I-(aq)+H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
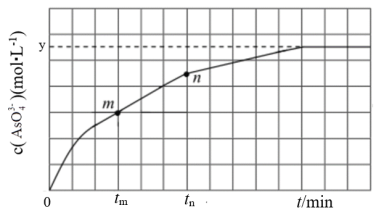
①下列可判断反应达到平衡的是___ (填标号)。
a.溶液的pH不再变化
b.v(I-)=2v(AsO )
)
c.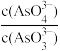 不再变化
不再变化
d.c(I-)=ymol•L-1
②tm时,v正___ v逆(填“大于”“小于”或“等于”)。
③tm时,v逆___ tnv逆(填“大于”“小于”或“等于”),理由是___ 。
 (aq)+I2(aq)+2OH-(aq)
(aq)+I2(aq)+2OH-(aq) AsO
AsO (aq)+2I-(aq)+H2O(l)。溶液中c(AsO
(aq)+2I-(aq)+H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
①下列可判断反应达到平衡的是
a.溶液的pH不再变化
b.v(I-)=2v(AsO
 )
)c.
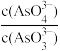 不再变化
不再变化d.c(I-)=ymol•L-1
②tm时,v正
③tm时,v逆
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用。
(1)一定温度下,某贮氢合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。
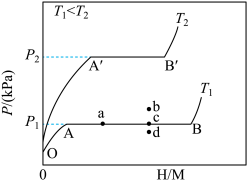
在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐渐增大;在AB段,MHx与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g)=ZMHy(s)△H(Ⅰ);在B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。反应(Ⅰ)中z=___ (用含x和y的代数式表示)。温度为T1时,2g某合金4min内吸收氢气240mL,吸氢速率v=___ mL•g-1•min。反应的焓变△H1__ 0(填“>”“<”或“=”)。
(2)η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)____ η(T2)(填“>”“<”或“=”)。当反应(Ⅰ)处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,达到平衡后反应(Ⅰ)可能处于图中的___ 点(填“b”“c”或“d”),该贮氢合金可通过___ 或___ 的方式释放氢气。
(1)一定温度下,某贮氢合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。

在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐渐增大;在AB段,MHx与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g)=ZMHy(s)△H(Ⅰ);在B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。反应(Ⅰ)中z=
(2)η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业制硝酸的主要反应是:4NH3(g)+5O2(g) 4NO(g)+6H2O (g)+1025 kJ
4NO(g)+6H2O (g)+1025 kJ
(1)该反应的平衡常数表达式为K=________________ ;升高温度K值__________ (填“增大”、“减小”或“不变”)。
(2)若反应物起始的物质的量相同,下列关系图错误的是________ (填字母序号)。
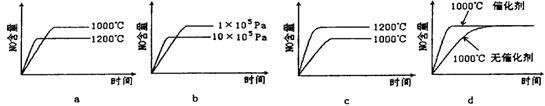
(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①起始时物料比c (O2):c(NH3)>1.25,其原因是_________________________ 。
②反应在第2min到第4min时O2的平均反应速率为______________ mol/L·min;
③反应在第2min改变了反应条件,改变的条件可能是________ (填字母序号)。
a.使用催化剂 b.升高温度 c.增大压强 d.增加O2的浓度
④反应在第8min改变的反应条件可能是_______________________________ 。
 4NO(g)+6H2O (g)+1025 kJ
4NO(g)+6H2O (g)+1025 kJ(1)该反应的平衡常数表达式为K=
(2)若反应物起始的物质的量相同,下列关系图错误的是

(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.8 | 1.6 | 0.5 |
①起始时物料比c (O2):c(NH3)>1.25,其原因是
②反应在第2min到第4min时O2的平均反应速率为
③反应在第2min改变了反应条件,改变的条件可能是
a.使用催化剂 b.升高温度 c.增大压强 d.增加O2的浓度
④反应在第8min改变的反应条件可能是
您最近一年使用:0次

 的部分数据。请分析后回答下列问题。
的部分数据。请分析后回答下列问题。


 )
) 时的浓度(
时的浓度(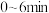 内该反应的化学反应速率
内该反应的化学反应速率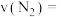
 为
为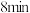 末
末 ,则
,则

