填写下列空白:
(1)表示含有17个质子、20个中子的原子的化学符号是___________________ 。
(2)第三周期0族元素的原子结构示意图为_______________ 。
(3)周期表中被称为第Ⅷ族的元素位于第_____________________ 纵行。
(4)周期表中最活泼的非金属元素位于第__________ 周期、第_________ 族。
(5)所含元素超过18种的周期是第__________ 、_________ 周期。
(1)表示含有17个质子、20个中子的原子的化学符号是
(2)第三周期0族元素的原子结构示意图为
(3)周期表中被称为第Ⅷ族的元素位于第
(4)周期表中最活泼的非金属元素位于第
(5)所含元素超过18种的周期是第
9-10高一下·广东佛山·期末 查看更多[1]
(已下线)2010年广东省佛山一中高一下学期期末考试化学试题
更新时间:2016-12-09 00:46:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】如图是元素周期表的一部分,其中所列的字母分别代表某一化学元素。
(1)硒是人体的微量元素之一,可保护细胞组织,请在周期表中标出元素符号_______ 。
(2)比较元素c、d、e、f的离子半径,由大到小的顺序是_______ (填离子符号)。
(3)根据核外电子的排布分区,字母g属于_______ 区元素,该区的价层电子通式为_______ 。
(4)位于金属元素与非金属元素分界线上的元素常被称为半金属或类金属,其单质及化合物有一定特殊性,如ef3为_______ (填“离子化合物”或“共价化合物”),元素e的最高价氧化物对应的水化物与强碱反应的离子方程式是_______ 。
(5)第VIIA的元素组成的单质,从上到下熔沸点逐渐升高,其原因是_______ 。
| a | |||||||||||||||||
| b | c | ||||||||||||||||
| d | e | f | g | ||||||||||||||
(2)比较元素c、d、e、f的离子半径,由大到小的顺序是
(3)根据核外电子的排布分区,字母g属于
(4)位于金属元素与非金属元素分界线上的元素常被称为半金属或类金属,其单质及化合物有一定特殊性,如ef3为
(5)第VIIA的元素组成的单质,从上到下熔沸点逐渐升高,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】右表是元素周期表的一部分。
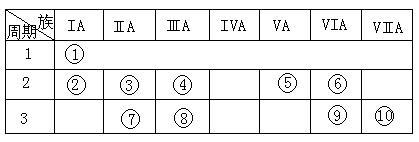
(1)表中元素⑩的氢化物的化学式为__________ ,此氢化物的还原性比元素⑨的氢化物的还原性_____________ (填强或弱)
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是_____ ,其单质的电子式为________________ 。
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式____________________ ;又如表中与元素⑦的性质相似的不同族元素是___________ (填元素符号)

(1)表中元素⑩的氢化物的化学式为
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】联合国大会将 2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性。下表显示了元素周期表中短周期的一部分,①~⑦代表七种短周期元素。
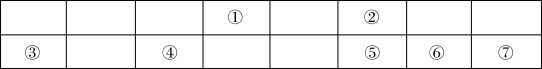
(1)七种元素中化学性质最不活泼的是_______ (填元素符号),形成化合物数目最多的元素是_______ (填元素符号)。
(2)元素②的最低价阴离子的离子结构示意图是_______ 。
(3)②、⑤两种元素的最简单氢化物中稳定性较强的是_______ (填化学式)。
(4)⑤、⑥两种元素的最高价氧化物对应的水化物中,酸性较弱的是_______ (填化学式)。
(5)元素③的最高价氧化物对应水化物与元素④的单质反应的离子方程式为_______ 。
(6)用电子式表示元素③和元素⑥形成化合物的过程_______ 。

(1)七种元素中化学性质最不活泼的是
(2)元素②的最低价阴离子的离子结构示意图是
(3)②、⑤两种元素的最简单氢化物中稳定性较强的是
(4)⑤、⑥两种元素的最高价氧化物对应的水化物中,酸性较弱的是
(5)元素③的最高价氧化物对应水化物与元素④的单质反应的离子方程式为
(6)用电子式表示元素③和元素⑥形成化合物的过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分。表中所列字母分别代表一种元素。
回答下列问题:
(1)j在元素周期表中的位置是______ 。
(2)e、h、m形成的简单离子其半径由大到小的顺序为________ 。(填写离子符号)
(3)n与g形成的化合物为______ (填写化学式,下同),将该化合物进行焰色反应,火焰呈______ 色。
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为______ 。
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg_____ Al(选填“>”或“<”);
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释______ 。
| a | b | |||||||
| c | d | e | f | |||||
| g | h | i | j | k | l | m | ||
| n |
(1)j在元素周期表中的位置是
(2)e、h、m形成的简单离子其半径由大到小的顺序为
(3)n与g形成的化合物为
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分。表中所列的字母分别代表一种元素。
回答下列问题:
(1)D的简单气态氢化物分子的立体构型为___________ 。
(2)第一电离能H___________ X(填“>”、“<”或“=”)。
(3)DA3的沸点比D2E的沸点高,其原因是___________ 。
(4)YE 的立体构型为
的立体构型为___________ ,YE 的键角比YE
的键角比YE 的键角小的原因是
的键角小的原因是___________ 。
| A | R | ||||||||||||||||
| B | D | E | M | T | |||||||||||||
| G | H | X | J | Y | L | ||||||||||||
| N |
(1)D的简单气态氢化物分子的立体构型为
(2)第一电离能H
(3)DA3的沸点比D2E的沸点高,其原因是
(4)YE
 的立体构型为
的立体构型为 的键角比YE
的键角比YE 的键角小的原因是
的键角小的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如表是元素周期表的一部分。回答下列问题:
(1)地球上99%的溴元素存在于海水中,因此溴被称为“海洋元素”。
①该表中溴在元素周期表中的位置为____________ 。
②该表中最高价氧化物对应的水化物酸性最强的是______ (填化学式),该元素形成化合物HXO的结构式为______ (X用对应元素符号表示)。
③卤素互化物(如IBr)与卤素单质性质相似。已知IBr能与水发生非氧化还原反应,写出IBr与水反应的化学方程式____________ ,IBr中含有的化学键是______ (填“离子键”、“极性键”或“非极性键”)。
(2) 溶于水形成
溶于水形成 溶液,向所得溶液中通入
溶液,向所得溶液中通入 气体,反应生成Se和
气体,反应生成Se和 。写出
。写出 与
与 反应的化学方程式
反应的化学方程式____________ 。
(3)已知某主族元素离子结构示意图为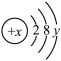 ,其中
,其中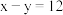 ,此元素与氯元素组成化合物的电子式为
,此元素与氯元素组成化合物的电子式为______ 。
16 S 硫 32.06 | 17 Cl 氯 35.45 |
34 Se 硒 78.96 | 35 Br 溴 79.90 |
53 I 碘 126.9 |
(1)地球上99%的溴元素存在于海水中,因此溴被称为“海洋元素”。
①该表中溴在元素周期表中的位置为
②该表中最高价氧化物对应的水化物酸性最强的是
③卤素互化物(如IBr)与卤素单质性质相似。已知IBr能与水发生非氧化还原反应,写出IBr与水反应的化学方程式
(2)
 溶于水形成
溶于水形成 溶液,向所得溶液中通入
溶液,向所得溶液中通入 气体,反应生成Se和
气体,反应生成Se和 。写出
。写出 与
与 反应的化学方程式
反应的化学方程式(3)已知某主族元素离子结构示意图为
 ,其中
,其中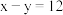 ,此元素与氯元素组成化合物的电子式为
,此元素与氯元素组成化合物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表为某元素周期表的一部分,按要求完成各小题。
(1)化学性质最不活泼的元素_______ (填元素编号),非金属性最强的元素是 ______ (填元素编号)。
(2)该表中金属性最强的元素单质与水反应的离子方程式为__________ 。
(3)①③⑤三种元素的最高价氧化物水化物中,碱性最强的是_______ (填物质的化学式)。
(4)④⑤⑧三种元素的原子半径由大到小的顺序为________ (用元素符号回答) 。
(5)元素⑧的最高价氧化物对应的水化物是________ (填化学式),该物质与元素⑤的最高价氧化物对应的水化物反应的离子方程式是____________ 。
 族 族周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)化学性质最不活泼的元素
(2)该表中金属性最强的元素单质与水反应的离子方程式为
(3)①③⑤三种元素的最高价氧化物水化物中,碱性最强的是
(4)④⑤⑧三种元素的原子半径由大到小的顺序为
(5)元素⑧的最高价氧化物对应的水化物是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】部分短周期元素原子半径与原子序数的关系如图所示。
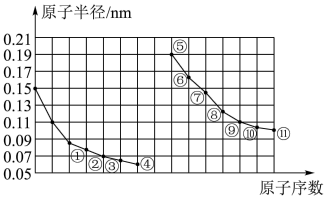
(1)元素①在周期表中的位置为___________ ;
(2)元素⑤⑥⑦的最高价氧化物对应的水化物中,碱性较强的是___________ (填化学式,下同);⑦、⑩、⑪三种元素常见离子的半径最大的是___________ ;
(3)元素③、⑩形成的简单氢化物中,沸点更高的是___________ ;元素③、④形成的简单氢化物中,稳定性较强的是___________ ;写出由③元素组成的氢化物中即含有极性键又含非极性键的化合物的结构式:___________ ;
(4)请设计实验比较元素氮的非金属性强于碳,选择的试剂有:稀硝酸、饱和 溶液、稀盐酸、澄清石灰水,化学仪器根据需要选择。
溶液、稀盐酸、澄清石灰水,化学仪器根据需要选择。

(1)元素①在周期表中的位置为
(2)元素⑤⑥⑦的最高价氧化物对应的水化物中,碱性较强的是
(3)元素③、⑩形成的简单氢化物中,沸点更高的是
(4)请设计实验比较元素氮的非金属性强于碳,选择的试剂有:稀硝酸、饱和
 溶液、稀盐酸、澄清石灰水,化学仪器根据需要选择。
溶液、稀盐酸、澄清石灰水,化学仪器根据需要选择。| 实验操作 | 实验现象 | 实验结论 |
| 元素N的非金属性强于C |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表为元素周期表中的一部分,表中列出的10种元素在周期表中的位置,按要求回答问题。
(1)元素性质最不活泼的元素是_______ (填名称)。
(2)元素③的单质在空气中燃烧,产生的现象是_______ ,生成物的化学式是_______ 。
(3)①③⑤元素的最高价氧化物的水化物,碱性最强的是_______ (填化学式)。
(4)②③④元素形成的简单离子半径由大到小的顺序是_______ (填离子符号)。
(5)元素①和⑧的最高价氧化物对应水化物的化学式分别为_______ 和_______ 。
(6)NaBr的溶液与元素⑧的单质反应的离子方程式为_______ 。
(7)⑧⑩两种元素形成的气态氢化物中最稳定的是_______ (填化学式),两种元素的非金属性的强弱顺序为_______ (填元素符号)。
(8)已知元素硒(Se)与元素⑦同主族,位于第4周期,则硒元素原子的最外层电子数为_______ ,根据硒在元素周期表中的位置推测,硒可能具有的性质有_______ 。
A.其单质常温下为气态
B.SeO2既有氧化性又有还原性
C.最高价对应的氧化物的水化物的化学式为H2SeO4
D.气态氢化物比H2S稳定
| 族/周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑨ | |||
| 4 | ② | ④ |
(1)元素性质最不活泼的元素是
(2)元素③的单质在空气中燃烧,产生的现象是
(3)①③⑤元素的最高价氧化物的水化物,碱性最强的是
(4)②③④元素形成的简单离子半径由大到小的顺序是
(5)元素①和⑧的最高价氧化物对应水化物的化学式分别为
(6)NaBr的溶液与元素⑧的单质反应的离子方程式为
(7)⑧⑩两种元素形成的气态氢化物中最稳定的是
(8)已知元素硒(Se)与元素⑦同主族,位于第4周期,则硒元素原子的最外层电子数为
A.其单质常温下为气态
B.SeO2既有氧化性又有还原性
C.最高价对应的氧化物的水化物的化学式为H2SeO4
D.气态氢化物比H2S稳定
您最近一年使用:0次



