下表为某元素周期表的一部分,按要求完成各小题。
(1)化学性质最不活泼的元素_______ (填元素编号),非金属性最强的元素是 ______ (填元素编号)。
(2)该表中金属性最强的元素单质与水反应的离子方程式为__________ 。
(3)①③⑤三种元素的最高价氧化物水化物中,碱性最强的是_______ (填物质的化学式)。
(4)④⑤⑧三种元素的原子半径由大到小的顺序为________ (用元素符号回答) 。
(5)元素⑧的最高价氧化物对应的水化物是________ (填化学式),该物质与元素⑤的最高价氧化物对应的水化物反应的离子方程式是____________ 。
 族 族周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)化学性质最不活泼的元素
(2)该表中金属性最强的元素单质与水反应的离子方程式为
(3)①③⑤三种元素的最高价氧化物水化物中,碱性最强的是
(4)④⑤⑧三种元素的原子半径由大到小的顺序为
(5)元素⑧的最高价氧化物对应的水化物是
更新时间:2018-12-23 23:09:10
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据元素在周期表中的位置能推测元素的原子结构以及相关物质的性质。下图是元素周期表的一部分,请根据图中字母所示元素的位置回答问题。
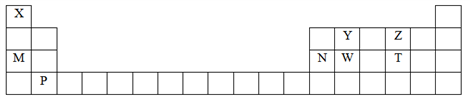
(1)元素W在周期表中所处的位置是______________ ;元素P的原子结构示意图为__________ ;元素Y的最高价氧化物的电子式为________________ 。
(2)元素M和N的单质中还原性较强的是_________ (填元素符号,下同):元素Y、Z、W的非金属性由强到弱的顺序为_______________ 。
(3)元素Z、N、T形成的简单离子中,半径由大到小的顺序为____________ (填离子符号)。
(4)下列说法中,正确的有______________ 。
①元素Y的单质有多种同素异形体
②M2Z中仅含离子键,M2Z2中仅含共价键
③X2T和M2Z都是离子化合物
④X2Z比X2T的沸点更高
(5)X、Z、M、T可形成含Z原子个数不同的两种常见酸式盐(均含四种元素),这两种酸式盐在溶液中相互反应的离子方程式为____________________ 。

(1)元素W在周期表中所处的位置是
(2)元素M和N的单质中还原性较强的是
(3)元素Z、N、T形成的简单离子中,半径由大到小的顺序为
(4)下列说法中,正确的有
①元素Y的单质有多种同素异形体
②M2Z中仅含离子键,M2Z2中仅含共价键
③X2T和M2Z都是离子化合物
④X2Z比X2T的沸点更高
(5)X、Z、M、T可形成含Z原子个数不同的两种常见酸式盐(均含四种元素),这两种酸式盐在溶液中相互反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素A、B、C、D、E的原子序数依次增大。常温下,A、B组成的化合物是常见液体,C的原子半径是短周期主族元素中最大的,D最外层电子数等于电子层数的2倍。回答下列问题:
(1)B在元素周期表中的位置为________ ;A、B组成的原子个数比为1:1的化合物的电子式为________ 。
(2)B、C的简单离子中,半径较大的是________ (填离子符号);A、B、C三种元素组成的化合物中含有的化学键类型是________ 。
(3)C、D的最高价氧化物对应的水化物间反应的离子方程式为________ 。
(4)下列叙述能说明E的非金属性强于D的是________ (填序号)。
a.D的简单氢化物的稳定性强于E的
b.D的氧化物对应的水化物的酸性弱于E的
c.D的单质常温下为固体,E的单质常温下为气体
d.E的单质通入D的简单氢化物的水溶液中,有D单质生成
(1)B在元素周期表中的位置为
(2)B、C的简单离子中,半径较大的是
(3)C、D的最高价氧化物对应的水化物间反应的离子方程式为
(4)下列叙述能说明E的非金属性强于D的是
a.D的简单氢化物的稳定性强于E的
b.D的氧化物对应的水化物的酸性弱于E的
c.D的单质常温下为固体,E的单质常温下为气体
d.E的单质通入D的简单氢化物的水溶液中,有D单质生成
您最近一年使用:0次
【推荐3】氮、碳、硼元素形成的化合物具有独特的结构。请回答:
(1)固态的N2O5为离子晶体(阴阳离子中所含原子个数均不超过4个),其阳离子的空间结构名称为___________ ,阴离子中氮原子的杂化方式为___________ 。
(2)比较酸性强弱:
___________  (填“>”、“<”),请说明理由
(填“>”、“<”),请说明理由___________ 。
(3)当石墨被过量的K处理后(未反应的金属被汞洗出),K+离子在石墨层间嵌入,K+层在石墨层的投影如图所示。该钾石墨晶体的化学式是___________ ,晶体类型是___________ 。不正确 的是___________。
(5)硼砂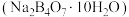 与NaOH的混合溶液中加入H2O2可以制备
与NaOH的混合溶液中加入H2O2可以制备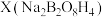 ,已知X的阴离子
,已知X的阴离子 只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式
只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式___________ 。
(1)固态的N2O5为离子晶体(阴阳离子中所含原子个数均不超过4个),其阳离子的空间结构名称为
(2)比较酸性强弱:

 (填“>”、“<”),请说明理由
(填“>”、“<”),请说明理由(3)当石墨被过量的K处理后(未反应的金属被汞洗出),K+离子在石墨层间嵌入,K+层在石墨层的投影如图所示。该钾石墨晶体的化学式是
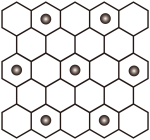
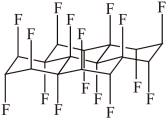
| A.与石墨相比,(CF)x导电性增强 | B.与石墨相比,(CF)x抗氧化性增强 |
| C.(CF)x中C—F的键长比C—C短 | D.1mol(CF)x中含有2x mol共价单键 |
(5)硼砂
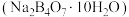 与NaOH的混合溶液中加入H2O2可以制备
与NaOH的混合溶液中加入H2O2可以制备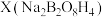 ,已知X的阴离子
,已知X的阴离子 只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式
只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表短周期的一部分

(1)①~⑦元素中金属性最强的元素在元素周期表中的位置是___________ 。
(2)表中元素⑥的原子结构示意图为___________ 。
(3)④与⑤形成的化合物的化学键类型为_______ ,该化合物的电子式为____________ 。
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是___________ (填化学式,下同);④所在主族的前四种元素的单质分别与氢气化合形成的气态氢化物的稳定性由强到弱的顺序是_________ 。
(5)表中元素②的单质与③的最高价含氧酸反应的化学方程式为___________________ 。

(1)①~⑦元素中金属性最强的元素在元素周期表中的位置是
(2)表中元素⑥的原子结构示意图为
(3)④与⑤形成的化合物的化学键类型为
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是
(5)表中元素②的单质与③的最高价含氧酸反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知A、B两种元素,A的原子序数为x,A和B所在周期的元素种类数目分别为m和n。
(1)如果A和B同在IA族,当B在A的上一周期时,B的原子序数为___________ ,当B在A的下一周期时,B的原子序数为___________ ;
(2)如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为___________ ;当B在A的下一周期时,B的原子序数为___________ 。
(1)如果A和B同在IA族,当B在A的上一周期时,B的原子序数为
(2)如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为
您最近一年使用:0次
填空题
|
适中
(0.65)
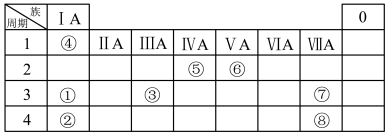
【推荐3】几种主族元素在周期表中的位置如下
(1)⑥元素的简单氢化物的化学式是_______ 。
(2)①③⑦三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为_______ ,该元素在周期表中的位置是_______ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是_______ (填化学式)①与③最高价氧化物对应水化物反应的离子方程_______ 。
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:_______ 。下列表述中能证明这一事实的是_______ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
(1)⑥元素的简单氢化物的化学式是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图是元素周期表的一部分,表中列出了八种元素的位置:
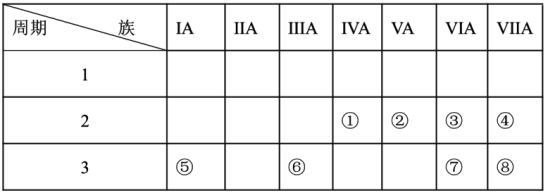
请回答下列问题:
(1)①元素的最简单氢化物的电子式为___________ 。
(2)在元素①-⑧中,金属性最强的元素是___________ (填元素符号);在元素⑤-⑧中,最高价含氧酸酸性最强的是___________ (填化学式)。
(3)③、④、⑤三种元素的原子半径由大到小的顺序是___________ (填元素符号),③和⑦的简单氢化物的稳定性较强的是___________ (填化学式)。
(4)④和⑤所形成的化合物属于___________ (填“离子”或“共价”)化合物。
(5)将等物质的量的①的最简单的氢化物和⑧的单质混合后,在漫射光的照射下充分反应,生成物中物质的量最大的是___________ (写分子式);
(6)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为___________ 。

请回答下列问题:
(1)①元素的最简单氢化物的电子式为
(2)在元素①-⑧中,金属性最强的元素是
(3)③、④、⑤三种元素的原子半径由大到小的顺序是
(4)④和⑤所形成的化合物属于
(5)将等物质的量的①的最简单的氢化物和⑧的单质混合后,在漫射光的照射下充分反应,生成物中物质的量最大的是
(6)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据题意填空:
(1)表中是几种短周期元素的原子半径及主要化合价。
则L元素的名称是_____ ,R元素在周期表中的位置为_____ 。
(2)某种融雪剂的主要成分为XY2,且X、Y均为周期表中前20号元素。XY2中阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子,则该融雪剂主要成分的电子式为_____ 。
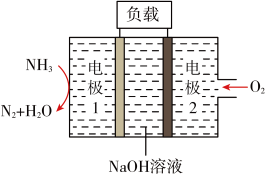
(3)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池如图所示,该燃料电池工作时,负极的电极反应式为_____ ;电池的总反应为_____ 。
(1)表中是几种短周期元素的原子半径及主要化合价。
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.111 | 0.106 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
则L元素的名称是
(2)某种融雪剂的主要成分为XY2,且X、Y均为周期表中前20号元素。XY2中阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子,则该融雪剂主要成分的电子式为
(3)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池如图所示,该燃料电池工作时,负极的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。根据下表中短周期元素的原子半径和主要化合价,回答表后的问题。
(1)上述元素中与元素⑧处于同一周期的有______________________ (填元素符号)
(2)元素①在元素周期表中的位置是_______________________
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为__________________ (填化学式)
(4)请写出下列元素形成的常见化合物的电子式:
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:_________________________ 。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
-2 | -3 | -1 | -3 |
(1)上述元素中与元素⑧处于同一周期的有
(2)元素①在元素周期表中的位置是
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为
(4)请写出下列元素形成的常见化合物的电子式:
③⑤
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)写出元素符号:
①________ ,②________ ,⑨________ 。
(2)写出下列反应的化学方程式:
⑤的单质跟④的氢氧化物溶液反应:________________________________________ 。
⑥的单质在③的单质中燃烧:__________________________________________ 。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 四 | ⑨ |
①
(2)写出下列反应的化学方程式:
⑤的单质跟④的氢氧化物溶液反应:
⑥的单质在③的单质中燃烧:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表列出了a~m 13种元素在周期表(已省略了过渡元素 )中的位置:
(1)元素b为________ (填名称);画出g的原子结构示意图__________ 。
(2)元素f、i、j的原子半径从大到小的顺序是____________ (用元素符号表示);这三种原子分别形成简单离子后,离子半径从大到小的顺序是_____________ (用离子符号表示)。
(3)h和k的原子序数相差___________ (填数字)。
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为___________ ,该化合物中化学键有____________ ,该化合物与c的最高价氧化物反应的化学方程式为_________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | a | |
| 2 | b | c | d | |||||
| 3 | e | f | g | h | i | |||
| 4 | j | k | l | |||||
| 5 | m |
(1)元素b为
(2)元素f、i、j的原子半径从大到小的顺序是
(3)h和k的原子序数相差
(4)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下表列出了①-⑨九种元素在元素周期表中的位置:

请按要求回答下列问题:
(1)元素⑤的原子结构示意图是_______ 。
(2)⑤、⑥、⑨三种元素原子半径由大到小的顺序是_______ (填元素符号);这三种元素最高价氧化物对应水化物中碱性最强的是_______ (填化学式)。
(3)③、④元素的简单氢化物的稳定性较弱的是_______ (填化学式)。
(4)写出一种含②元素的10电子化合物_______ (填化学式)。
(5)写出元素⑨的单质与水反应的化学方程式_______ 。
(6)写出元素⑦的最高价氧化物跟盐酸反应的离子方程式_______ 。

请按要求回答下列问题:
(1)元素⑤的原子结构示意图是
(2)⑤、⑥、⑨三种元素原子半径由大到小的顺序是
(3)③、④元素的简单氢化物的稳定性较弱的是
(4)写出一种含②元素的10电子化合物
(5)写出元素⑨的单质与水反应的化学方程式
(6)写出元素⑦的最高价氧化物跟盐酸反应的离子方程式
您最近一年使用:0次



