氮、碳、硼元素形成的化合物具有独特的结构。请回答:
(1)固态的N2O5为离子晶体(阴阳离子中所含原子个数均不超过4个),其阳离子的空间结构名称为___________ ,阴离子中氮原子的杂化方式为___________ 。
(2)比较酸性强弱:
___________  (填“>”、“<”),请说明理由
(填“>”、“<”),请说明理由___________ 。
(3)当石墨被过量的K处理后(未反应的金属被汞洗出),K+离子在石墨层间嵌入,K+层在石墨层的投影如图所示。该钾石墨晶体的化学式是___________ ,晶体类型是___________ 。不正确 的是___________。
(5)硼砂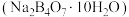 与NaOH的混合溶液中加入H2O2可以制备
与NaOH的混合溶液中加入H2O2可以制备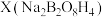 ,已知X的阴离子
,已知X的阴离子 只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式
只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式___________ 。
(1)固态的N2O5为离子晶体(阴阳离子中所含原子个数均不超过4个),其阳离子的空间结构名称为
(2)比较酸性强弱:

 (填“>”、“<”),请说明理由
(填“>”、“<”),请说明理由(3)当石墨被过量的K处理后(未反应的金属被汞洗出),K+离子在石墨层间嵌入,K+层在石墨层的投影如图所示。该钾石墨晶体的化学式是
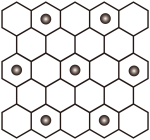
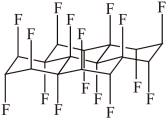
| A.与石墨相比,(CF)x导电性增强 | B.与石墨相比,(CF)x抗氧化性增强 |
| C.(CF)x中C—F的键长比C—C短 | D.1mol(CF)x中含有2x mol共价单键 |
(5)硼砂
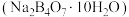 与NaOH的混合溶液中加入H2O2可以制备
与NaOH的混合溶液中加入H2O2可以制备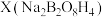 ,已知X的阴离子
,已知X的阴离子 只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式
只有一种化学环境的B原子,且B和O原子最外层都达到8电子稳定结构,写出X阴离子的结构式
更新时间:2024-05-23 10:09:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(I)原子序数小于等于36的Q、W、X、Y、Z五种元素,其中Q是原子半径最小的元素,W和Y的基态原子2p能级所含成单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子。回答下列问题(涉及元素时用对应的元素符号表示):
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是___________ 。
(2)1molQWX与1molWQ2Y所含σ键的比值为___________ 。
(3)根据等电子体理论可以预测WXY-的空间构型为___________ 。
(4)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为_______ 。

(5)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为:___________ 。
②预测该化合物熔点应___________ 金刚石(填“高于”或“低于”)。
(II)铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(1)Fe3+可以与SCN-、CN-、有机分子等形成配合物。基态Fe3+的电子排布式为___________ ;与SCN-互为等电子体且为非极性分子的化学式为___________ 。
(2)普鲁士蓝俗称铁蓝,结构如图甲所示(K+未画出),平均每两个立方体中含有一个K+,该晶体的化学式为___________ 。又知该晶体中铁元素有+2价和+3价两种,则Fe3+与Fe2+的个数比为___________ 。
(3)在一定条件下铁形成的晶体的基本结构单元如图乙和图丙所示,则图乙和图丙的结构中铁原子的配位数之比为___ ,两种晶体中空间利用率较高的是__ 。(填“图乙”或“图丙”)

(1)X、Y、Z三种元素的第一电离能由大到小的顺序是
(2)1molQWX与1molWQ2Y所含σ键的比值为
(3)根据等电子体理论可以预测WXY-的空间构型为
(4)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为

(5)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为:
②预测该化合物熔点应
(II)铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(1)Fe3+可以与SCN-、CN-、有机分子等形成配合物。基态Fe3+的电子排布式为
(2)普鲁士蓝俗称铁蓝,结构如图甲所示(K+未画出),平均每两个立方体中含有一个K+,该晶体的化学式为
(3)在一定条件下铁形成的晶体的基本结构单元如图乙和图丙所示,则图乙和图丙的结构中铁原子的配位数之比为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:A_________ ,B__________ ,C____________ ,D___________ ,E_________
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:______________________ 。
(3)写出A、B两元素的最高价氧化物的水化物相互反应的化学方程式:______________________ 。
(4)C、D、E的氢化物稳定性由强到弱依次为:(用化学式表示)_______________________ 。
(1)写出下列元素符号:A
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
(3)写出A、B两元素的最高价氧化物的水化物相互反应的化学方程式:
(4)C、D、E的氢化物稳定性由强到弱依次为:(用化学式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知五种元素原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成的离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。试回答下列问题:
(1) 写出C元素的名称是___________________
(2) 用电子式表示离子化合物A2B的形成过程_____________________________ ;
(3) 写出下列物质的电子式:E与B形成的化合物_______________ ;A、B、E形成的化合物
____________ ;D、E形成的化合物_____________ 。
(4) A、B两元素组成的化合物A2B2属于___________ (离子或共价)化合物,存在的化学键____________________________________ 。
(1) 写出C元素的名称是
(2) 用电子式表示离子化合物A2B的形成过程
(3) 写出下列物质的电子式:E与B形成的化合物
(4) A、B两元素组成的化合物A2B2属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铁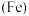 、钴
、钴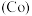 、镍
、镍 是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体.
是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体.
(1)基态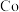 原子的核外电子排布式为
原子的核外电子排布式为
_____________ ,第二周期中基态原子与基态 原子具有相同未成对电子数的元素是
原子具有相同未成对电子数的元素是______________ .
(2) 、
、 、
、 原子半径相似、化学性质相似,原因是
原子半径相似、化学性质相似,原因是_______________ .
(3)配合物 的中心原子价电子数与配体提供电子总数之和为
的中心原子价电子数与配体提供电子总数之和为_________ . 与
与 互为等电子体,
互为等电子体, 分子具有的化学键类型有
分子具有的化学键类型有____________ .
A. 键 B.
键 B. 键 C.离子键 D.金属键
键 C.离子键 D.金属键
(4) 的结构与相关性质见下表,其空间构型为
的结构与相关性质见下表,其空间构型为______________ , 的杂化形式为
的杂化形式为_________ ,其为_____________ 晶体.
(5)钙钛矿中含有 、
、 、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中
、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中 和O如下图所示,
和O如下图所示, 位于O形成正八面体空隙中.晶胞边长为
位于O形成正八面体空隙中.晶胞边长为 ,设
,设 为阿伏加 德罗常数的数值,则该氧化物的密度为
为阿伏加 德罗常数的数值,则该氧化物的密度为________________  (列出计算表达式).
(列出计算表达式).

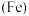 、钴
、钴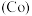 、镍
、镍 是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体.
是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体.(1)基态
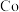 原子的核外电子排布式为
原子的核外电子排布式为
 原子具有相同未成对电子数的元素是
原子具有相同未成对电子数的元素是(2)
 、
、 、
、 原子半径相似、化学性质相似,原因是
原子半径相似、化学性质相似,原因是(3)配合物
 的中心原子价电子数与配体提供电子总数之和为
的中心原子价电子数与配体提供电子总数之和为 与
与 互为等电子体,
互为等电子体, 分子具有的化学键类型有
分子具有的化学键类型有A.
 键 B.
键 B. 键 C.离子键 D.金属键
键 C.离子键 D.金属键(4)
 的结构与相关性质见下表,其空间构型为
的结构与相关性质见下表,其空间构型为 的杂化形式为
的杂化形式为| 相对分子质量 | 熔点 | 沸点 | 结构 |
| 171 | 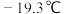 | 43℃ |  |
(5)钙钛矿中含有
 、
、 、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中
、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中 和O如下图所示,
和O如下图所示, 位于O形成正八面体空隙中.晶胞边长为
位于O形成正八面体空隙中.晶胞边长为 ,设
,设 为阿伏加 德罗常数的数值,则该氧化物的密度为
为阿伏加 德罗常数的数值,则该氧化物的密度为 (列出计算表达式).
(列出计算表达式).
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】乙炔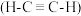 是有机合成工业的一种重要原料。下列两种方法可生产乙炔。
是有机合成工业的一种重要原料。下列两种方法可生产乙炔。

碳化钙晶胞示意图
(1)甲烷在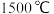 电弧中经极短时间加热分解产生乙炔。
电弧中经极短时间加热分解产生乙炔。
①反应的化学方程式为_______ 。
②上述反应中碳原子轨道杂化类型的变化为_______ 。
③乙炔分子中 键和
键和 键数目之比为
键数目之比为_______ 。
(2)工业上曾用电石(主要成分为碳化钙)与水反应生成乙炔。
① 基态核外电子排布式为
基态核外电子排布式为_______ 。
②由图可知,碳化钙的化学式为_______ 。
③碳化钙晶体中哑铃形 的存在,使晶胞延一个方向拉长。碳化钙晶体中1个
的存在,使晶胞延一个方向拉长。碳化钙晶体中1个 周围距离
周围距离最近 的 围成的几何图形为
围成的几何图形为_______ (填正方形、正四面体或正八面体)。
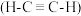 是有机合成工业的一种重要原料。下列两种方法可生产乙炔。
是有机合成工业的一种重要原料。下列两种方法可生产乙炔。
碳化钙晶胞示意图
(1)甲烷在
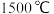 电弧中经极短时间加热分解产生乙炔。
电弧中经极短时间加热分解产生乙炔。①反应的化学方程式为
②上述反应中碳原子轨道杂化类型的变化为
③乙炔分子中
 键和
键和 键数目之比为
键数目之比为(2)工业上曾用电石(主要成分为碳化钙)与水反应生成乙炔。
①
 基态核外电子排布式为
基态核外电子排布式为②由图可知,碳化钙的化学式为
③碳化钙晶体中哑铃形
 的存在,使晶胞延一个方向拉长。碳化钙晶体中1个
的存在,使晶胞延一个方向拉长。碳化钙晶体中1个 周围距离
周围距离 围成的几何图形为
围成的几何图形为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】有下列微粒:①CH4;②CH2=CH2;③CH CH;④NH3;⑤NH
CH;④NH3;⑤NH ;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):
;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):
(1)呈正四面体的是_______ 。
(2)中心原子轨道为sp3杂化的是_______ ,为sp2杂化的是_______ ,为sp杂化的是_______ 。
(3)互为等电子体的一组是_______ 。
(4)为减少温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2。若有1molCH4生成,则有_______ molσ键和_______ molπ键断裂。
 CH;④NH3;⑤NH
CH;④NH3;⑤NH ;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):
;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):(1)呈正四面体的是
(2)中心原子轨道为sp3杂化的是
(3)互为等电子体的一组是
(4)为减少温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2。若有1molCH4生成,则有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】《旧唐书•舆服志》中关于白铜的记载:“自馀一品乘白铜饰犊车”,古时云南所产的镍白铜(铜镍合金)最为有名,称为“云白铜”,曾主要用于造币,亦可用于制作仿银饰品。请回答下列问题:

(1)基态Cu原子的核外电子排布式为[Ar]______ ,Cu的焰色反应为亮绿色,该现象与核外电子发生______ 有关。
(2)向CuSO4溶液中逐滴加入氨水,首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色透明溶液。
①在[Cu(NH3)4]2+中Cu2+和NH3之间形成的化学键为______ ,Cu 提供的空轨道数目是______ ,提供孤电子对的成键原子是______ (填元素符号)。
②[Cu(NH3)4]SO4中含有的四种非金属元素中电负性最大的是______ (填元素符号),根据价层电子对互斥理论,氧与硫元素所形成的SO42-、SO2、SO3三种微粒中,中心原子价层电子对数不同于其他微粒的是______ 。
③在[Cu(NH3)4]SO4中,NH3的中心原子的杂化轨道类型为______ ,NH3的立体构型是______ ,HNO3和HNO2是N的两种含氧酸,请根据物质结构与性质的关系解释,HNO3比HNO2酸性强的原因是______ 。
(3)某镍白制合金的立方晶胞结构如图所示。
①在镍白铜合金中金属原子的堆积方式为______ 。
②若合金晶胞边长为a nm,其密度为dg•cm-3,则阿伏伽德罗常数(NA)的数值为______ (列出计算式即可)。

(1)基态Cu原子的核外电子排布式为[Ar]
(2)向CuSO4溶液中逐滴加入氨水,首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色透明溶液。
①在[Cu(NH3)4]2+中Cu2+和NH3之间形成的化学键为
②[Cu(NH3)4]SO4中含有的四种非金属元素中电负性最大的是
③在[Cu(NH3)4]SO4中,NH3的中心原子的杂化轨道类型为
(3)某镍白制合金的立方晶胞结构如图所示。
①在镍白铜合金中金属原子的堆积方式为
②若合金晶胞边长为a nm,其密度为dg•cm-3,则阿伏伽德罗常数(NA)的数值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E都是元素周期表中的前20号元素,它们的原子序数依次递增。已知B、D两种元素原子的最外层电子数是最内层电子数的两倍,而C元素原子的最外层电子数等于B元素原子的核外电子数,E的价电子数为1.回答下列问题。
(1)画出C元素的原子结构示意图_______ 。
(2)在1mol DC2中,有___ mol D—C键。
(3)在化合物BC2的晶体中,每个BC2分子周围与它距离最近的BC2分子有___ 个。
(4)原子序数介于B、C之间的元素X和B、C都可与A形成10e-的化合物。则X、B、C的第一电离能顺序是_____ (填元素符号),三种10e-的化合物中沸点最低的___ 。
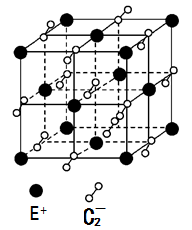
(5)已知高温下C和E元素形成的晶体呈立方体结构,晶体中元素C的化合价部分为0价,部分为-2价。如下图所示为C和E元素形成的晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是__________ 。
A.该晶体化学式为EC2(KO2),每个晶胞含有个4个E+和4个C2-
B.晶体中每个E+周围有8个C2-,每个C2-周围有8个E+
C.晶体中与每个E+距离最近的E+有8个
D.晶体中,0价C与-2价C的数目比为3:1
E.C2-与N2互为等电子体
(1)画出C元素的原子结构示意图
(2)在1mol DC2中,有
(3)在化合物BC2的晶体中,每个BC2分子周围与它距离最近的BC2分子有
(4)原子序数介于B、C之间的元素X和B、C都可与A形成10e-的化合物。则X、B、C的第一电离能顺序是
(5)已知高温下C和E元素形成的晶体呈立方体结构,晶体中元素C的化合价部分为0价,部分为-2价。如下图所示为C和E元素形成的晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是

A.该晶体化学式为EC2(KO2),每个晶胞含有个4个E+和4个C2-
B.晶体中每个E+周围有8个C2-,每个C2-周围有8个E+
C.晶体中与每个E+距离最近的E+有8个
D.晶体中,0价C与-2价C的数目比为3:1
E.C2-与N2互为等电子体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.金属铝的晶胞结构如图甲所示,原子之间相互位置关系的平面图如图乙所示。若已知Al的原子半径为 ,
, 代表阿伏伽德罗常数的值,Al的摩尔质量为
代表阿伏伽德罗常数的值,Al的摩尔质量为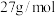 ,请回答:
,请回答:

(1)一个晶胞中Al原子的数目为___________ 。
(2)该晶体的密度为___________  (列出表达式即可)。
(列出表达式即可)。
Ⅱ.硫化锌是一种半导体材料,S与Zn所形成化合物晶体的晶胞如图所示。
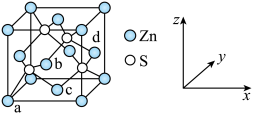
(3)原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为 ;b为
;b为 ;c为
;c为 。则d的坐标参数为
。则d的坐标参数为___________ 。
(4)已知该晶胞的密度为 ,若晶胞的边长为x,则x为
,若晶胞的边长为x,则x为___________ cm;则其中阴阳离子间最短的距离为___________ cm。(均用 表示,列出计算式即可)
表示,列出计算式即可)
 ,
, 代表阿伏伽德罗常数的值,Al的摩尔质量为
代表阿伏伽德罗常数的值,Al的摩尔质量为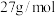 ,请回答:
,请回答:
(1)一个晶胞中Al原子的数目为
(2)该晶体的密度为
 (列出表达式即可)。
(列出表达式即可)。Ⅱ.硫化锌是一种半导体材料,S与Zn所形成化合物晶体的晶胞如图所示。

(3)原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为
 ;b为
;b为 ;c为
;c为 。则d的坐标参数为
。则d的坐标参数为(4)已知该晶胞的密度为
 ,若晶胞的边长为x,则x为
,若晶胞的边长为x,则x为 表示,列出计算式即可)
表示,列出计算式即可)
您最近一年使用:0次



