有下列微粒:①CH4;②CH2=CH2;③CH CH;④NH3;⑤NH
CH;④NH3;⑤NH ;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):
;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):
(1)呈正四面体的是_______ 。
(2)中心原子轨道为sp3杂化的是_______ ,为sp2杂化的是_______ ,为sp杂化的是_______ 。
(3)互为等电子体的一组是_______ 。
(4)为减少温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2。若有1molCH4生成,则有_______ molσ键和_______ molπ键断裂。
 CH;④NH3;⑤NH
CH;④NH3;⑤NH ;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):
;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):(1)呈正四面体的是
(2)中心原子轨道为sp3杂化的是
(3)互为等电子体的一组是
(4)为减少温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2。若有1molCH4生成,则有
21-22高三上·山西运城·阶段练习 查看更多[2]
更新时间:2021-09-23 21:40:37
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请回答下面问题
(1)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
解释表中氟化物熔点差异的原因:____________________________________ 。
(2)CO的结构可表示为C≡O,N2的结构可表示为N≡N。下表是两者的键能数据:(单位:kJ·mol-1)
CO与N2的结构相似,分子中都含有共价三键,其中含有_______ 个π键;结合数据说明CO比N2活泼的原因:__________________________________________ 。
(1)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1266 | 1534 | 183 |
解释表中氟化物熔点差异的原因:
(2)CO的结构可表示为C≡O,N2的结构可表示为N≡N。下表是两者的键能数据:(单位:kJ·mol-1)
| C-O | C=O | C≡O | |
| CO | 357.7 | 798.9 | 1071.9 |
| N-N | N=N | N≡N | |
| N2 | 154.8 | 418.4 | 941.7 |
CO与N2的结构相似,分子中都含有共价三键,其中含有
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】共价键的分类
| 分类标准 | 类型 |
| 共用电子对数 | |
| 电子云重叠方式 | |
| 共用电子对是否偏移 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题。
(1)CCl4、H2S、BF3、CO2键角由大到小的顺序是___________ 。
(2)As4O6的分子结构如图所示: ,其中As原子的杂化方式为
,其中As原子的杂化方式为___________ ,O原子的杂化方式为___________ 。
(3)[Co(NO2)(NH3)5]Cl2中Co3+的配位数为___________ ,粒子中的大π键可用符号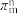 表示,中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大
表示,中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则配体中NO
),则配体中NO 的大π键可表示为
的大π键可表示为___________ ,空间构型为___________ 。
(4)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)回答下列问题:
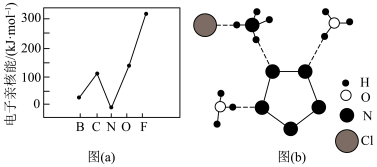
①元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1(纵坐标)变化趋势如图(a)。其中除氮元素外,其他元素的E1自左而右依次增大的原因___________ ,氮元素的E1呈现异常的原因是___________ 。
②用X射线衍射实验方法测得化合物R的晶体结构,其局部结构如图(b)所示:从结构分析,R中两种阳离子的相同之处为___________ (填标号),不同之处为___________ (填标号)。
A.中心原子的杂化类型
B.中心原子的价层电子对数
C.立体结构
(1)CCl4、H2S、BF3、CO2键角由大到小的顺序是
(2)As4O6的分子结构如图所示:
 ,其中As原子的杂化方式为
,其中As原子的杂化方式为(3)[Co(NO2)(NH3)5]Cl2中Co3+的配位数为
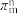 表示,中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大
表示,中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大 键可表示为
键可表示为 ),则配体中NO
),则配体中NO 的大π键可表示为
的大π键可表示为(4)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)回答下列问题:

①元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1(纵坐标)变化趋势如图(a)。其中除氮元素外,其他元素的E1自左而右依次增大的原因
②用X射线衍射实验方法测得化合物R的晶体结构,其局部结构如图(b)所示:从结构分析,R中两种阳离子的相同之处为
A.中心原子的杂化类型
B.中心原子的价层电子对数
C.立体结构
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示:
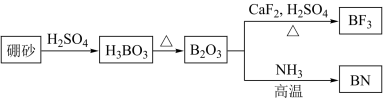
请回答下列问题:
(1)写出B2O3与NH3反应生成BN的化学反应方程式______________
(2)基态N原子的价层电子排布式为________ 。
(3)B、N、O相比,第一电离能最大的是______ ,BN中B元素的化合价为_____
(4)写出一个与SO42﹣互为等电子体的微粒__________ 。
(5)BF3能与NH3反应生成BF3•NH3,BF3•NH3中BF3与NH3之间通过________ (填“离子键”、“配位键”或“氢键”) 结合。

请回答下列问题:
(1)写出B2O3与NH3反应生成BN的化学反应方程式
(2)基态N原子的价层电子排布式为
(3)B、N、O相比,第一电离能最大的是
(4)写出一个与SO42﹣互为等电子体的微粒
(5)BF3能与NH3反应生成BF3•NH3,BF3•NH3中BF3与NH3之间通过
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】明代宋应星所著《天工开物》中已经记载了我国古代用炉甘石(主要成分ZnCO3)和煤冶锌工艺,锌的主要用途是制造锌合金和作为其他金属的保护层。回答下列问题:
(1) Zn原子基态核外电子排布式为___________________ 。
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①SO42-中心原子的轨道杂化类型为_____ ,与它互为等电子体的阴离子化学式为____ (写出一种)。
②在[Zn(NH3)4]2+中Zn2+与NH3之间形成的化学键为___ ,提供孤电子对的成键原子是____ 。 ③氨的热稳定性强于膦(PH3),原因是_______ 。
(3)黄铜是由铜和锌所组成的合金,元素铜与锌的第一电离能分别为:ICu=746kJ/mol,Izn=906 kJ/mol,ICu < Izn的原因是_____________ 。
(4)《本草纲目》中记载炉甘石(主要成分ZnCO3)可止血,消肿毒,生肌,明目……。
Zn、C、O电负性由大至小的顺序是________ 。ZnCO3中阴离子的立体构型是______ 。
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶胞结构如图所示,每个Zn原子周围最近的Zn原子数目为____________ 。
晶胞边长为a pm,阿伏伽德罗常数为NA,则ZnS晶体的密度为_____ g/cm3 (列出计算式即可)
(1) Zn原子基态核外电子排布式为
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①SO42-中心原子的轨道杂化类型为
②在[Zn(NH3)4]2+中Zn2+与NH3之间形成的化学键为
(3)黄铜是由铜和锌所组成的合金,元素铜与锌的第一电离能分别为:ICu=746kJ/mol,Izn=906 kJ/mol,ICu < Izn的原因是
(4)《本草纲目》中记载炉甘石(主要成分ZnCO3)可止血,消肿毒,生肌,明目……。
Zn、C、O电负性由大至小的顺序是
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶胞结构如图所示,每个Zn原子周围最近的Zn原子数目为
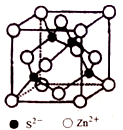
晶胞边长为a pm,阿伏伽德罗常数为NA,则ZnS晶体的密度为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】下图是元素周期表中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题:
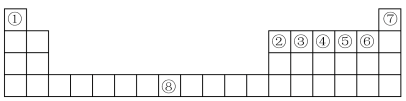
(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,⑦元素位于周期表的__________ 区。
(2)②、⑥两元素形成的化合物的空间构型为__________ ,其中心原子的杂化轨道类型为__________ 。
(3)写出元素⑧基态原子的电子排布式_______________________ 。
(4)③④⑤⑥四种元素第一电离能的由小到大的顺序为______________ (填元素符号)。
(5)与③⑤形成的三原子化合物互为等电子体的分子为__________________ 。
(6)元素⑧与CO可形成的X(CO)5型化合物,该化合物常温下呈液态,熔点为−20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于__________ 晶体(填晶体类型)。

(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,⑦元素位于周期表的
(2)②、⑥两元素形成的化合物的空间构型为
(3)写出元素⑧基态原子的电子排布式
(4)③④⑤⑥四种元素第一电离能的由小到大的顺序为
(5)与③⑤形成的三原子化合物互为等电子体的分子为
(6)元素⑧与CO可形成的X(CO)5型化合物,该化合物常温下呈液态,熔点为−20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有下列粒子:①CH4 ②CH2 =CH2 ③CH≡CH ④NH3 ⑤NH4+ ⑥BF3 ⑦H2O。填写下列空白(填序号):
(1)呈正四面体的是__________
(2)中心原子轨道为 sp3 杂化的是__________ ,为 sp2 杂化的是__________ ,为 sp 杂化的是__________
(3)所有原子共平面的是__________
(4)粒子存在配位键的是__________
(5)含有极性键的极性分子的是__________
(1)呈正四面体的是
(2)中心原子轨道为 sp3 杂化的是
(3)所有原子共平面的是
(4)粒子存在配位键的是
(5)含有极性键的极性分子的是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】砷化镓(GaAs)是优良的半导体材料或用于制作微型激光器或太阳能电池的材料等。部分元素在周期表中位置如下:
回答下列问题:
(1)六种元素中,非金属性最强的元素是:________ .写出As原子的最外层的电子排布式_________ ,As原子核外有_____ 个未成对电子。
(2)根据元素周期律,可判断原子半径Ga_____ As。(选填“>”、 “<”或“=”)。写出铝的最高价氧化物对应水化物的电离方程式:________________
(3)NH3 的分子构型是_______ 。GaF3的熔点高于1000°C,GaCl3的熔点为77.9°C,可能的原因是_______ .写出C2H2的电子式为:_________
(4)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因___________
| A1 | Si | P |
| Ga | Ge | As |
回答下列问题:
(1)六种元素中,非金属性最强的元素是:
(2)根据元素周期律,可判断原子半径Ga
(3)NH3 的分子构型是
(4)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/°C | -49.5 | 26 | 146 |
| 沸点/°C | 83.1 | 186 | 约400 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g) 2SO3(g) △H=-190kJ•mol-1。
2SO3(g) △H=-190kJ•mol-1。
(1)基态O原子核外电子排布式是_______ 。
(2)根据价电子对互斥理论可预测SO2的空间结构是_______ ,中心原子S杂化轨道的类型是_______ 。
(3)该反应的平衡常数表达式K=________ ,温度升高后,平衡常数将_______ (选填“增大”、“减小”或“不变”)。
(4)在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2,10分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=_______ 。
(5)假设该反应在恒容密闭容器中进行,一定能说明该反应达到平衡状态的是_______ 。
 2SO3(g) △H=-190kJ•mol-1。
2SO3(g) △H=-190kJ•mol-1。(1)基态O原子核外电子排布式是
(2)根据价电子对互斥理论可预测SO2的空间结构是
(3)该反应的平衡常数表达式K=
(4)在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2,10分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=
(5)假设该反应在恒容密闭容器中进行,一定能说明该反应达到平衡状态的是
| A.混合气体的密度不再变化 |
| B.v(SO2)=2v(O2) |
| C.混合气体的平均相对分子质量不再变化 |
| D.混合气体中氧元素的质量分数不再变化 |
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下表中的空白:
| 粒子 | 中心原子孤电子对数 | 中心原子的杂化轨道类型 | 空间结构 |
| BF3 | |||
| H2S | |||
| PCl3 | |||
 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】常用CH3CHO+NaOH+2Cu(OH)2 CH3COONa+Cu2O↓+3H2O检验醛类。
CH3COONa+Cu2O↓+3H2O检验醛类。
(1)基态Cu2+核外电子排布式为_________ 。
(2)CH3COONa中碳原子轨道的杂化类型是______ ,1 mol CH3COONa中含有σ键的数目为_______ 。
(3)与OH- 离子互为等电子体的阴离子为________ 。
(4)沸点高低:乙酸钠>乙酸>乙醛,这是因为_________ 。
(5)Cu2O 晶体结构可能是________ (填字母)。

 CH3COONa+Cu2O↓+3H2O检验醛类。
CH3COONa+Cu2O↓+3H2O检验醛类。 (1)基态Cu2+核外电子排布式为
(2)CH3COONa中碳原子轨道的杂化类型是
(3)与OH- 离子互为等电子体的阴离子为
(4)沸点高低:乙酸钠>乙酸>乙醛,这是因为
(5)Cu2O 晶体结构可能是

您最近半年使用:0次



