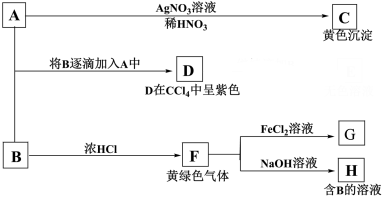
A、B、C、D四种元素的核电荷数依次增加,它们的离子的电子层数相同,且最外层电子数均为8.A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。回答以下问题:
(1)四种元素的符号依次是 A_________ ,B_________ ,C________ ,D________ 。
(2)试画出四种元素的离子结构示意图:A__________ ,D__________ 。它们的离子半径由大到小的顺序 ______________________ 。
(3)写出各元素最高价氧化物对应水化物的分子式_______________________ ,分别比较酸性和碱性的强弱____________________ 。
(1)四种元素的符号依次是 A
(2)试画出四种元素的离子结构示意图:A
(3)写出各元素最高价氧化物对应水化物的分子式
更新时间:2016-12-09 14:56:43
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,表中所列序号分别代表短周期中的一种元素:
(1)元素④的原子结构示意图是_______ 。
(2)元素⑤在周期表中的位置是_______ 。
(3)②⑥⑦最高价氧化物对应水化物中的碱性最强的是(用电子式表示)_______ 。
(4)⑤⑧⑨的氢化物中稳定性最好的是(用电子式表示)_______ 。
(5)⑧⑩的最高价氧化物对应水化物的酸性顺序(用化学式表示)_______ 。
(6)化合物X由①⑤⑥三种元素组成,化合物Y是元素③的最高价氧化物,将标准状况下11.2LY通入到200mL3mol/L的X溶液中完全被吸收。通过计算判断所得溶液组成的化学式及质量(不用写出计算过程):_______ 。
| ① | |||||||
| ② | ③ | ④ | ⑤ | ||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素⑤在周期表中的位置是
(3)②⑥⑦最高价氧化物对应水化物中的碱性最强的是(用电子式表示)
(4)⑤⑧⑨的氢化物中稳定性最好的是(用电子式表示)
(5)⑧⑩的最高价氧化物对应水化物的酸性顺序(用化学式表示)
(6)化合物X由①⑤⑥三种元素组成,化合物Y是元素③的最高价氧化物,将标准状况下11.2LY通入到200mL3mol/L的X溶液中完全被吸收。通过计算判断所得溶液组成的化学式及质量(不用写出计算过程):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知某物质主要成分的化学式为XY2,X原子的结构示意图为 ,
, 的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的
的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的 倍,Z与Y相邻且Z、W能形成一种
倍,Z与Y相邻且Z、W能形成一种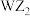 型分子。
型分子。
(1)m=_______ ,该物质主要成分的化学式为_______ 。
(2)Z在周期表中位置为_______ 。
(3)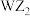 的电子式为
的电子式为_______ 。
(4)用电子式表示 的形成过程为
的形成过程为_______ 。
(5)Y的单质与X最高价氧化物对应的水化物反应的化学方程式为:_______
 ,
, 的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的
的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的 倍,Z与Y相邻且Z、W能形成一种
倍,Z与Y相邻且Z、W能形成一种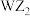 型分子。
型分子。(1)m=
(2)Z在周期表中位置为
(3)
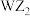 的电子式为
的电子式为(4)用电子式表示
 的形成过程为
的形成过程为(5)Y的单质与X最高价氧化物对应的水化物反应的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E都是前四周期元素,A原子价电子排布式为nsnnPn,B原子核外有3种能量不同的电子,B、C同主族,B与C形成的一种化合物是形成酸雨的重要物质。D原子核外电子有11种不同的运动状态。E是前四周期中原子核外成单电子数最多的元素。
回答下列问题:
(1)元素A的一种单质的结构如图所示。
其中A-A-A键之间的夹角是____________ ,含有1mol A的该单质中,形成的共价键有____ mol。
(2)等径圆球在二维空间里可形成密置层和非密置层排列。在二维空间里D晶体的配位数是_______ 。
(3)E的基态原子的外围电子排布式为_______ ,AC2的电子式为 _______________ 。
(4)下列关于AB2的晶体和冰的比较中正确的是______ (填标号)。
a.晶体的密度:AB2的晶体 > 冰
b.晶体的熔点:AB2的晶体 >冰
c.晶体中的空间利用率:AB2的晶体 >冰
d.晶体中分子间相互作用力类型相同
(5)D2C的晶胞如图,设晶体密度是ρg/㎝3
①比较D2C与D2B的熔点,较高的是_______ (填化学式),其原因是 ___________________ 。
②试计算●与〇的最短距离______ (只写出计算式,阿伏伽德罗常数的值用NA表示)。
回答下列问题:
(1)元素A的一种单质的结构如图所示。

其中A-A-A键之间的夹角是
(2)等径圆球在二维空间里可形成密置层和非密置层排列。在二维空间里D晶体的配位数是
(3)E的基态原子的外围电子排布式为
(4)下列关于AB2的晶体和冰的比较中正确的是
a.晶体的密度:AB2的晶体 > 冰
b.晶体的熔点:AB2的晶体 >冰
c.晶体中的空间利用率:AB2的晶体 >冰
d.晶体中分子间相互作用力类型相同
(5)D2C的晶胞如图,设晶体密度是ρg/㎝3
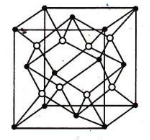
①比较D2C与D2B的熔点,较高的是
②试计算●与〇的最短距离
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】M、N、X、Y、Z、W、R是原子序数依次增大的前四周期元素,基态N原子的最外层电子数是电子层数的2倍,W是电负性最小的短周期主族元素,基态R原子含有4个未成对电子,其中4种元素形成的一种阳离子结构如图所示。
(1)基态W原子核外有_____ 种不同空间运动状态的电子;R元素在周期表中的位置为___ 。
(2)M、X形成两种离子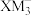 、
、 ,键角:
,键角: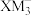
_____  (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是______ 。
(3)R的一种配合物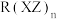 的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应:
的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应: 。
。
①
____ 。
②该配合物中σ键与π键的数目之比为_____ 。
③反应过程中断裂的化学键只有配位键,形成的化学键是________ 。
(4)在超高压下,W与N可形成化合物 ,
, (小圆球)按简单立方排布,形成
(小圆球)按简单立方排布,形成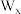 立方体空隙(如下图所示),电子对
立方体空隙(如下图所示),电子对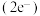 和N原子交替分布填充在立方体的中心。
和N原子交替分布填充在立方体的中心。
______ ;晶体中 配位的N原子数为
配位的N原子数为_____ ;晶胞中W和N的最短距离为d nm, 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为_______  。
。

(1)基态W原子核外有
(2)M、X形成两种离子
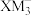 、
、 ,键角:
,键角: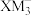
 (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是(3)R的一种配合物
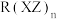 的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应:
的中心原子价电子数与配体提供的电子数之和为18,一定条件下发生分解反应: 。
。①

②该配合物中σ键与π键的数目之比为
③反应过程中断裂的化学键只有配位键,形成的化学键是
(4)在超高压下,W与N可形成化合物
 ,
, (小圆球)按简单立方排布,形成
(小圆球)按简单立方排布,形成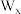 立方体空隙(如下图所示),电子对
立方体空隙(如下图所示),电子对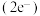 和N原子交替分布填充在立方体的中心。
和N原子交替分布填充在立方体的中心。

 配位的N原子数为
配位的N原子数为 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,请回答下列问题:

(1)在①~⑩元素中:金属性最强的元素是_______ (填元素符号,下同),原子半径最小的是_______ ,化学性质最不活泼的是_______ 。
(2)中国学者雷晓光被国际组织推选为“元素①代言人”,元素①的原子结构示意图是_______ 。
(3)②~④三种元素分别形成的简单离子中,离子半径最小的是_______ (用离子符号表示)。
(4)⑤的最高价氧化物和④的最高价氧化物的水化物溶液反应的离子方程式为_______ 。
(5)用电子式表示⑥和⑨的简单离子间构成的化合物的形成过程为_______ 。
(6)砷化镓(GaAs)是一种优良的半导体材料。砷(As)与元素①同主族,原子序数为33,砷(As)在周期表中的位置是_______ 。镓与砷同周期,与元素⑤同主族。下列说法错误的是_______ (填标号)。
A.原子半径:Ga>Al B.热稳定性:
C.酸性: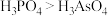 D.碱性:
D.碱性:
(7)设计一个实验方案来比较⑦、⑩单质氧化性的强弱(可供选择的试剂有:KBr溶液、 、新制氯水),你的实验方案是
、新制氯水),你的实验方案是_______ 。

(1)在①~⑩元素中:金属性最强的元素是
(2)中国学者雷晓光被国际组织推选为“元素①代言人”,元素①的原子结构示意图是
(3)②~④三种元素分别形成的简单离子中,离子半径最小的是
(4)⑤的最高价氧化物和④的最高价氧化物的水化物溶液反应的离子方程式为
(5)用电子式表示⑥和⑨的简单离子间构成的化合物的形成过程为
(6)砷化镓(GaAs)是一种优良的半导体材料。砷(As)与元素①同主族,原子序数为33,砷(As)在周期表中的位置是
A.原子半径:Ga>Al B.热稳定性:

C.酸性:
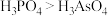 D.碱性:
D.碱性:
(7)设计一个实验方案来比较⑦、⑩单质氧化性的强弱(可供选择的试剂有:KBr溶液、
 、新制氯水),你的实验方案是
、新制氯水),你的实验方案是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表是元素周期表的一部分,每个编号代表一种元素,请根据要求回答问题:
(1)表中金属性最强的元素为___ (填元素符号);
(2)最稳定的元素为___ (填元素符号);
(3)③、⑦的原子半径大小关系:③___ (填“>”“<”或“=”)⑦);
(4)④和⑦两种元素组成的化合物与AgNO3溶液反应的离子方程式为___ 。
族 周期 | ⅠA | 0 | |||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
2 | ① | ② | ⑥ | ||||||
3 | ③ | ④ | ⑤ | ⑦ | |||||
(2)最稳定的元素为
(3)③、⑦的原子半径大小关系:③
(4)④和⑦两种元素组成的化合物与AgNO3溶液反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下列是从上到下原子序数依次增大的六种短周期主族元素,其元素性质或原子结构如下表所示:
回答下列问题:
(1)元素F在元素周期表中的位置是_________ 。
(2)元素A的一种核素可测定文物年代,这种核素是___________ (填核素符号)。B、C、D、E四种元素的离子半径由大到小的顺序为_________ (填离子符号)。
(3)火箭发动机曾经利用B2H4作燃料、H2C2作助燃剂,产物无污染,二者反应的化学方程式为__________ ,氧化产物与还原产物物质的量之比为__________ 。
(4)元素C的单质与钠在常温下生成物质X。用电子式表示物质X的形成过程:__________ 。
(5)A、B、E、F四种元素的最高价氧化物对应的水化物中,酸性最强的是__________ (填化学式)。E的最高价氧化物对应的水化物溶液与D的最高价氧化物反应的离子方程式为___________ 。
| 元素编号 | 元素性质或原子结构 |
| A | A的一种同素异形体可用作润滑剂 |
| B | 单质是空气中含量最高的气体 |
| C | 最外层电子数是最内层电子数的3倍 |
| D | 简单阳离子半径是同周期阳离子半径最小的 |
| E | M层电子数是电子层数的2倍 |
| F | 元素最高正价是+7,最低价是-1 |
(1)元素F在元素周期表中的位置是
(2)元素A的一种核素可测定文物年代,这种核素是
(3)火箭发动机曾经利用B2H4作燃料、H2C2作助燃剂,产物无污染,二者反应的化学方程式为
(4)元素C的单质与钠在常温下生成物质X。用电子式表示物质X的形成过程:
(5)A、B、E、F四种元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,①~⑧代表对应的元素,回答下列问题:

(1)①的一种核素的质量数为3,该核素的符号为___________ 。
(2)⑦在元素周期表中的位置是___________ ;⑧的原子结构示意图为___________ 。
(3)②③⑧的最高价氧化物对应水化物酸性最强的是___________ (填化学式),②⑥的最高价氧化物对应水化物碱性更强的是___________ (填化学式)。
(4)④⑤⑧的简单离子,半径最小的是___________ (填离子),④和⑧的简单氢化物沸点更高的是___________ (填化学式)。
(5)写出⑥的单质与⑤最高价氧化物对应水化物反应的离子方程式:_______ 。
(6)设计实验比较⑤和⑥的金属性强弱:_________ 。

(1)①的一种核素的质量数为3,该核素的符号为
(2)⑦在元素周期表中的位置是
(3)②③⑧的最高价氧化物对应水化物酸性最强的是
(4)④⑤⑧的简单离子,半径最小的是
(5)写出⑥的单质与⑤最高价氧化物对应水化物反应的离子方程式:
(6)设计实验比较⑤和⑥的金属性强弱:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中,A、C及B、D分别是同主族元素;A元素的原子半径是所有主族元素中原子半径最小的;B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍;四种元素所形成的单质中A、B单质是气体,C、D单质是固体。
(1)写出以下元素的名称: B____________ ;C___________ 。
(2)用电子式表示C2D的形成过程:___________ 。
(3)由B、C两元素所形成的原子个数比为1:1的化合物属于__________ (填“离子” 或“共价”)化合物,存在的化学键的种类有________ (若有共价键需要写出具体的共价键类型),写出它与水反应的离子方程式___________________ 。
(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,写出实验室中用固体药品制备该气体的的化学方程式______________ 。
(5)写出B的原子结构示意图______________________ 若一个B原子中有8个中子,写出B的原子符号_______________
(6)写出均由A、B、C、D四种元素组成的两种物质之间发生反应的离子方程式__ 。
(7)由A、B两元素形成的单质在以铂作电极稀硫酸作电解液形成的燃料电池中,正极的电极方程式为___________ ,若以氢氧化钾为电解液则负极的电极方程式为______________________ 。
(1)写出以下元素的名称: B
(2)用电子式表示C2D的形成过程:
(3)由B、C两元素所形成的原子个数比为1:1的化合物属于
(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,写出实验室中用固体药品制备该气体的的化学方程式
(5)写出B的原子结构示意图
(6)写出均由A、B、C、D四种元素组成的两种物质之间发生反应的离子方程式
(7)由A、B两元素形成的单质在以铂作电极稀硫酸作电解液形成的燃料电池中,正极的电极方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、W代表四种短周期元素,有关它们的部分结构信息及性质信息如表所示。请按要求回答下列问题:
(1)Z在元素周期表中的位置是___ 。
(2)X、Y的最简单气态氢化物的稳定性由强到弱的顺序是___ (用化学式表示)。
(3)X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是___ (用化学式表示)。
(4)实验室用X的气态氢化物的水溶液制取W的氢氧化物的方法是___ (用离子方程式表示)。
(5)写出Z的单质与二氧化硫的混合气体通入水中所发生反应的离子方程式:___ 。
| 元素 | 部分结构信息 | 部分性质信息 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数大于4 | Z元素的最高正化合价与最低负化合价的代数和等于6 |
| W | W原子的最外层电子数等于(2n-3)(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
(2)X、Y的最简单气态氢化物的稳定性由强到弱的顺序是
(3)X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是
(4)实验室用X的气态氢化物的水溶液制取W的氢氧化物的方法是
(5)写出Z的单质与二氧化硫的混合气体通入水中所发生反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知非金属元素A、B、C、D、E均属于短周期元素,其原子序数依次增大,A元素原子形成的离子核外电子数为零,B原子的最外层电子数是内层电子数的2倍,通常状况下E的单质是黄色晶体,不溶于水,易溶于二硫化碳,D与E在同一主族,C、D在周期表中处于相邻的位置,请回答下列问题:
(1)A元素的名称是________ ,E的阴离子结构示意图是__________________ 。
(2)元素C的最高价氧化物对应水化物与其气态氢化物反应生成化合物Z,该反应的离子方程式为____________________________________________ ,化合物Z属于________________ (填“离子化合物”或“共价化合物”),Z中含有的化学键类型是________________ 。
(3)C元素的最高价氧化物对应的水化物的稀溶液能与D、E元素形成的一种化合物发生氧化还原反应,其离子反应方程式为__________________________ 。
(1)A元素的名称是
(2)元素C的最高价氧化物对应水化物与其气态氢化物反应生成化合物Z,该反应的离子方程式为
(3)C元素的最高价氧化物对应的水化物的稀溶液能与D、E元素形成的一种化合物发生氧化还原反应,其离子反应方程式为
您最近一年使用:0次