位于短周期的四种主族元素A、B、C、D原子序数依次增大,已知A.C位于同一主族,A在周期表中原子半径最小。B.D的最外层电子数相等,且B.D的原子序数之和为A.C原子序数之和的两倍。根据你的推断回答下列问题:
(1)写出由上述元素形成的具有漂白作用的四种物质的化学式:_______ ,_______ ,_______ ,_______ 。
(2)C与D形成D的最低价化合物的电子式:_______
(3)仅由B、C、D三种元素形成的一种盐,溶于水后呈碱性,请用一个离子方程式表示其呈碱性的原因:_______ 。
(1)写出由上述元素形成的具有漂白作用的四种物质的化学式:
(2)C与D形成D的最低价化合物的电子式:
(3)仅由B、C、D三种元素形成的一种盐,溶于水后呈碱性,请用一个离子方程式表示其呈碱性的原因:
9-10高二下·江苏·期末 查看更多[1]
(已下线)2010年江苏省清江中学高二第二学期期末考试化学试卷
更新时间:2016-12-08 16:50:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题。
(1)V2O5是常见催化剂,V的基态原子的价电子的轨道表示式为___________ ;其电子占据的原子轨道数为 ___________ ,最高能层符号为 ___________ 。
(2)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子简化的核外电子排布式为___________ ,该离子更稳定的原因是 ___________ 。
(3)基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(4)所有短周期元素中,基态原子具有1个未成对电子的元素共有___________ 种。
(5)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是___________  填序号,下同
填序号,下同 ,由离子键和非极性共价键构成的物质是
,由离子键和非极性共价键构成的物质是___________ ,属于共价化合物的是___________ 。
(1)V2O5是常见催化剂,V的基态原子的价电子的轨道表示式为
(2)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子简化的核外电子排布式为
(3)基态S原子电子占据最高能级的电子云轮廓图为
(4)所有短周期元素中,基态原子具有1个未成对电子的元素共有
(5)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是
 填序号,下同
填序号,下同 ,由离子键和非极性共价键构成的物质是
,由离子键和非极性共价键构成的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐2】W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数一次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的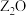 和黑色的ZO两种氧化物。
和黑色的ZO两种氧化物。
(1)W位于元素周期表第_________ 周期第_________ 族。W的气态氢化物稳定性比

__________ (填“强”或“弱”)。
(2)Y的基态原子核外电子排布式是________ ,Y的第一电离能比X的__________ (填“大”或“小”)。
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
_________________________________________________________________________ 。
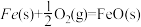
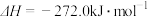
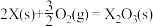
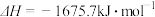
X的单质和FeO反应的热化学方程式是_________________________________________ 。
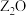 和黑色的ZO两种氧化物。
和黑色的ZO两种氧化物。(1)W位于元素周期表第

(2)Y的基态原子核外电子排布式是
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
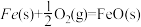
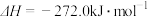
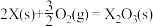
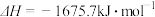
X的单质和FeO反应的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】非金属元素在生活中占有十分重要的位置,如C、N、O、Si、Cl等。
(1)上述元素中原子最外层电子排布中s亚层和p亚层电子数相等的是_______ 。(填元素符号)
(2)由氮元素与硅元素组成的物质 可用于制造发动机的耐热耐磨部件。请写出一个与它晶体类型相同的物质的化学式:
可用于制造发动机的耐热耐磨部件。请写出一个与它晶体类型相同的物质的化学式:_______ ,请从元素周期律的角度解释 中N元素显负价的原因
中N元素显负价的原因_______ 。
(3)氧元素的简单阴离子最外层电子排布式是_______ 。
下列事实能说明氯与氧两元素非金属性相对强弱的有_______ (选填编号)。
a.Cl原子最外层电子数比O多 b.酸性: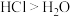
c. 中氯元素为+4价,氧元素为-2价 d.沸点:
中氯元素为+4价,氧元素为-2价 d.沸点: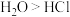
(1)上述元素中原子最外层电子排布中s亚层和p亚层电子数相等的是
(2)由氮元素与硅元素组成的物质
 可用于制造发动机的耐热耐磨部件。请写出一个与它晶体类型相同的物质的化学式:
可用于制造发动机的耐热耐磨部件。请写出一个与它晶体类型相同的物质的化学式: 中N元素显负价的原因
中N元素显负价的原因(3)氧元素的简单阴离子最外层电子排布式是
下列事实能说明氯与氧两元素非金属性相对强弱的有
a.Cl原子最外层电子数比O多 b.酸性:
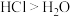
c.
 中氯元素为+4价,氧元素为-2价 d.沸点:
中氯元素为+4价,氧元素为-2价 d.沸点: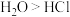
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。请根据下表中短周期元素的原子半径和主要化合价,回答表后问题。
(1)元素①在周期表中的位置为_____ 。
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为____ (填化学式)。
(3)元素①、③形成的18电子化合物的电子式为____ ,元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是______ (填化学式)。
(4)元素②、⑤形成化合物的电子式为_____ 。
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的离子方程式为______
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10 m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)元素①在周期表中的位置为
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为
(3)元素①、③形成的18电子化合物的电子式为
(4)元素②、⑤形成化合物的电子式为
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】X、Y、Z为周期表前四周期中的常见元素。X的单质是人体呼吸及新陈代谢中必不少的气体。Y的单质也为气体,易溶于水,溶液呈浅黄绿色。Z的基态原子外围电子排布为3d64s2。
(1)将Z2X3与ZY3按等物质的量放在密闭管中加热使其恰好完全反应,只生成一种产物A,其物质的量是反应物的1.5倍。A为菱形片晶,具有金属光泽。此化学反应方程式为___ 。
(2)A不溶于冷水,但在沸水中缓慢水解,生成黄棕色沉淀B,溶液呈酸性,且无气泡产生。取水解后的上层清液,滴入硝酸银溶液,生成白色沉淀,说明Y在A中与___ 是直接相连的,所以水解时Y进入水中。B的化学式为___ 。
(3)将A溶于稀盐酸中,滴入硫氰化铵溶液,星红色,说明A中的Z的氧化数为___ ,A的命名应为___ 。
(1)将Z2X3与ZY3按等物质的量放在密闭管中加热使其恰好完全反应,只生成一种产物A,其物质的量是反应物的1.5倍。A为菱形片晶,具有金属光泽。此化学反应方程式为
(2)A不溶于冷水,但在沸水中缓慢水解,生成黄棕色沉淀B,溶液呈酸性,且无气泡产生。取水解后的上层清液,滴入硝酸银溶液,生成白色沉淀,说明Y在A中与
(3)将A溶于稀盐酸中,滴入硫氰化铵溶液,星红色,说明A中的Z的氧化数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】百余种不同的元素,是构成大千世界中所有物质的“基石”。科学家们根据元素的性质递变规律、电子排布规律等对元素进行编排设计元素周期表。请根据所学内容回答下列问题:
(1)地壳中含量最多的元素的基态原子的轨道表示式是___________ ,能量最高的电子所在的轨道呈___________ 形。
(2) 、
、 是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是
是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是___________ 。
(3)研究发现,正离子的颜色与未成对电子数有关。例如: 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是___________ 。
(4)当原子、分子或离子内有单电子存在时,能被外磁场吸引,表现出顺磁性。则铬元素的基态原子是否具有磁性?填___________ (填“有”或“无”)该元素在元素周期表中的位置:第___________ 周期,第___________ 族,该周期共有___________ 种元素。
(5)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。下表中列出了第三周期的几种元素的部分性质:
预测X值的区间:___________ ;上表中五种元素的第一电离能由大到小的顺序是___________ 。(写元素符号)
(6)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。基态 原子的外围电子排布式为
原子的外围电子排布式为___________ ; 位于周期表中
位于周期表中___________ 区,基态 、
、 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
(7) 和
和 的第一电离能:
的第一电离能: ,原因是
,原因是___________ 。
(8)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是___________。
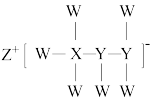
(1)地壳中含量最多的元素的基态原子的轨道表示式是
(2)
 、
、 是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是
是工业生产中重要的两种金属,将乙醇蒸气通过赤热的氧化铜粉末,发生的反应的化学方程式是(3)研究发现,正离子的颜色与未成对电子数有关。例如:
 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是(4)当原子、分子或离子内有单电子存在时,能被外磁场吸引,表现出顺磁性。则铬元素的基态原子是否具有磁性?填
(5)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。下表中列出了第三周期的几种元素的部分性质:
| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 主要化合价 |  , , |  , , |  , , |  |  |
(6)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。基态
 原子的外围电子排布式为
原子的外围电子排布式为 位于周期表中
位于周期表中 、
、 离子中未成对的电子数之比为
离子中未成对的电子数之比为(7)
 和
和 的第一电离能:
的第一电离能: ,原因是
,原因是(8)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是___________。
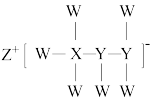
| A.该化合物中,W、X、Y之间均为共价键 |
| B.Z的单质既能与水反应,也可与甲醇反应 |
| C.Y的最高化合价氧化物的水化物为强酸 |
D.X的氟化物 中原子均为8电子稳定结构 中原子均为8电子稳定结构 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】U、W、X、Y、Z都是短周期元素,且原子序数依次增大。其中U与W可形成三角锥形分子A,U与X可形成常温下呈液态的分子B,A、B均为10电子分子;Y元素原子的K层电子数与M层电子数相同;Z元素的单质、氧化物均为原子晶体。请回答下列问题:
(1)Z元素在周期表中的位置_______________ 。W、X、Y、Z四种元素的原子半径由小到大的顺序是___________________ (用元素符号表示)。
(2)用电子式表示U与X形成的18电子化合物的形成过程____________________ 。
(3)ZX2与NaOH溶液反应的离子方程式___________________ 。
(4)一定量的Y单质在足量二氧化碳中充分燃烧的化学方程式是______________ ,将生成的全部固体与足量的热浓硝酸混合,充分反应后,产物中二氧化碳和二氧化氮共aL(标准状况),则 Y 单质的质量是______________________ g(用含a的代数式表示)。
(1)Z元素在周期表中的位置
(2)用电子式表示U与X形成的18电子化合物的形成过程
(3)ZX2与NaOH溶液反应的离子方程式
(4)一定量的Y单质在足量二氧化碳中充分燃烧的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
请完成下列空白。
(1)属于卤族元素的有_______ (填元素符号)。
(2)②在⑥的单质中燃烧产物的电子式为_______ ,其中所含化学键类型为_______ 。
(3)能证明元素⑧比⑨的非金属性强的实验事实有(用离子方程式表示):_______ 。
(4)元素⑥的一种中子数为10的核素的符号为_______
(5)元素⑤的单质与NaOH溶液反应的化学方程式为_______
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ⑥ | |||||||
| 3 | ② | ④ | ⑤ | ⑦ | ⑧ | |||
| 4 | ③ | ⑨ | ||||||
请完成下列空白。
(1)属于卤族元素的有
(2)②在⑥的单质中燃烧产物的电子式为
(3)能证明元素⑧比⑨的非金属性强的实验事实有(用离子方程式表示):
(4)元素⑥的一种中子数为10的核素的符号为
(5)元素⑤的单质与NaOH溶液反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y.W原子的最外层没有p电子,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为1:1,Z原子核外电子中p电子数比Y原子多2个.
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:__________________ .
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为__________ (用分子式表示).
(3)四种元素原子半径的由大到小为_________ (填元素符号).
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为
(3)四种元素原子半径的由大到小为
您最近一年使用:0次



