W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数一次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的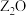 和黑色的ZO两种氧化物。
和黑色的ZO两种氧化物。
(1)W位于元素周期表第_________ 周期第_________ 族。W的气态氢化物稳定性比

__________ (填“强”或“弱”)。
(2)Y的基态原子核外电子排布式是________ ,Y的第一电离能比X的__________ (填“大”或“小”)。
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
_________________________________________________________________________ 。
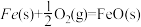
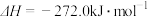
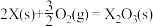
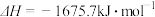
X的单质和FeO反应的热化学方程式是_________________________________________ 。
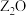 和黑色的ZO两种氧化物。
和黑色的ZO两种氧化物。(1)W位于元素周期表第

(2)Y的基态原子核外电子排布式是
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
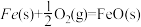
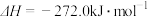
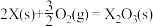
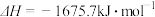
X的单质和FeO反应的热化学方程式是
2009·安徽·高考真题 查看更多[3]
更新时间:2009-11-22 23:51:48
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】面对世界范围内的能源危机,甲醇作为一种可再生能源,有广泛的应用前景。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g) ⇌CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g) ⇌CO2(g)+H2(g) ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式:____
(2)对于CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-90 kJ·mol-1,在容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡时CO的转化率与温度、压强的关系如图所示。
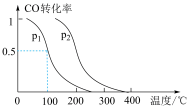
①p1_______ (填“大于”“小于”或“等于”) p2。
②在其他条件不变的情况下,缩小体积使压强增大,达到新平衡时,CO的转化率________ (填“增大”“减小”或“不变”),平衡常数________ (填“增大”“减小”或“不变”)。
(3)已知在温度T时,CO(g)+H2O(g) ⇌CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,判断此时刻υ正________ (填“>” 、“=”或“<”)υ逆。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g) ⇌CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g) ⇌CO2(g)+H2(g) ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式:
(2)对于CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-90 kJ·mol-1,在容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡时CO的转化率与温度、压强的关系如图所示。

①p1
②在其他条件不变的情况下,缩小体积使压强增大,达到新平衡时,CO的转化率
(3)已知在温度T时,CO(g)+H2O(g) ⇌CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,判断此时刻υ正
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据要求回答:
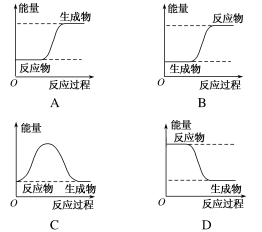
(1)下列各图中,表示反应是吸热反应的是_______
(2)到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。在25 ℃、101 kPa下,16 g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352 kJ的热量,则表示甲醇燃烧的热化学方程式为_____________________________ 。
(3)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1
E(H—H)=436 kJ·mol-1
E(Cl—Cl)=243 kJ·mol-1
则E(H—Cl)=________________________________ 。
(4)已知:
甲醇脱水反应 2CH3OH(g)=CH3OCH3(g)+H2O(g)△H1=-23.9KJ·mol-1
甲醇制烯烃反应 2CH3OH(g)=C2H4(g)+2H2O(g)△H2=-29.1KJ·mol-1
乙醇异构化反应 CH3CH2OH(g)=CH3OCH3(g)△H3=+50.7KJ·mol-1
则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H=____________ kJ·mol-1
(1)下列各图中,表示反应是吸热反应的是

(2)到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。在25 ℃、101 kPa下,16 g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352 kJ的热量,则表示甲醇燃烧的热化学方程式为
(3)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1
E(H—H)=436 kJ·mol-1
E(Cl—Cl)=243 kJ·mol-1
则E(H—Cl)=
(4)已知:
甲醇脱水反应 2CH3OH(g)=CH3OCH3(g)+H2O(g)△H1=-23.9KJ·mol-1
甲醇制烯烃反应 2CH3OH(g)=C2H4(g)+2H2O(g)△H2=-29.1KJ·mol-1
乙醇异构化反应 CH3CH2OH(g)=CH3OCH3(g)△H3=+50.7KJ·mol-1
则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学反应常伴随能量变化,是人类获得能量的重要途径。
(1)一种即热饭盒的结构如图所示,这种饭盒使用起来非常方便,撤去底部的隔板几分钟后,饭菜就变热了。
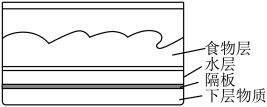
①下层物质可以是由镁粉、铁粉和食盐组成的混合物,则镁粉和铁粉的作用依次为___________ 、___________ 。
②化学能转化为热能在生产或生活中的应用还有___________ (填一种)。
③某种冷敷袋盛装的物质是硝酸铵,加少量水即可达到冷却效果,该冷敷袋的主要工作原理为___________ 热(填“吸”或“放”)的___________ 变化(填“物理”或“化学”)。
(2)借鉴中和反应反应热的测定方法,某同学测定放热反应 的焓变
的焓变 (忽略温度对焓变的影响,忽略溶液体积、质量变化和金属吸收的热量。近似的认为溶液的密度、比热容与水的相同,已知水的比热容为4.18
(忽略温度对焓变的影响,忽略溶液体积、质量变化和金属吸收的热量。近似的认为溶液的密度、比热容与水的相同,已知水的比热容为4.18 )。实验结果见下表。
)。实验结果见下表。
则温度:b___________ c(填“>”“<”或“=”);
___________  (用含a、c的代数式表示)。
(用含a、c的代数式表示)。
(3)已知298 K,101 kPa时,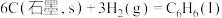
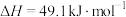 ,相关物质的摩尔燃烧焓数据如表:
,相关物质的摩尔燃烧焓数据如表:
则表示C(石墨,s)摩尔燃烧焓的热化学方程式为___________ ,a=___________ 。
(1)一种即热饭盒的结构如图所示,这种饭盒使用起来非常方便,撤去底部的隔板几分钟后,饭菜就变热了。

①下层物质可以是由镁粉、铁粉和食盐组成的混合物,则镁粉和铁粉的作用依次为
②化学能转化为热能在生产或生活中的应用还有
③某种冷敷袋盛装的物质是硝酸铵,加少量水即可达到冷却效果,该冷敷袋的主要工作原理为
(2)借鉴中和反应反应热的测定方法,某同学测定放热反应
 的焓变
的焓变 (忽略温度对焓变的影响,忽略溶液体积、质量变化和金属吸收的热量。近似的认为溶液的密度、比热容与水的相同,已知水的比热容为4.18
(忽略温度对焓变的影响,忽略溶液体积、质量变化和金属吸收的热量。近似的认为溶液的密度、比热容与水的相同,已知水的比热容为4.18 )。实验结果见下表。
)。实验结果见下表。| 序号 | 反应试剂 | 体系温度/℃ | ||
| 反应前 | 反应后 | |||
| ⅰ | 100mL 0.20  溶液 溶液 | 1.36g Zn粉 | a | b |
| ⅱ | 0.62g Zn粉 | a | c | |

 (用含a、c的代数式表示)。
(用含a、c的代数式表示)。(3)已知298 K,101 kPa时,
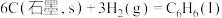
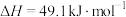 ,相关物质的摩尔燃烧焓数据如表:
,相关物质的摩尔燃烧焓数据如表:| 物质 |  | 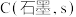 |  |
摩尔燃烧焓 | -285.8 | -393.5 | a |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知X、Y、Z、W、Q、R、E七种元素中,原子序数X<Y<Z<W<Q<R<E,其结构或性质信息如下表。
请根据信息回答有关问题:
(1)元素X的原子核外共有____ 种不同运动状态的电子,有____ 种不同能级的电子。
(2)元素Y原子中能量最高的是____ 电子。
(3)Q的基态原子核外电子排布式为________ ,R的元素符号为____ ,E元素原子的价电子排布式为_____ 。
(4)含有元素W的盐的焰色反应为____ 色,许多金属形成的盐都可以发生焰色反应,其原因是__________________________________________ 。
| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数 |
| Y | 元素的原子最外层电子排布式为nsnnpn+1 |
| Z | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子 |
| W | 元素的正一价离子的电子层结构与氩相同 |
| Q | 元素的核电荷数为Y和Z之和 |
| R | 元素的正三价离子的3d能级半充满 |
| E | 元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
请根据信息回答有关问题:
(1)元素X的原子核外共有
(2)元素Y原子中能量最高的是
(3)Q的基态原子核外电子排布式为
(4)含有元素W的盐的焰色反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W为四种常见的短周期元素。其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如图所示:
请回答以下问题:
(1)W在周期表中位置_____ ;
(2)X和氢能够构成+1价阳离子,其电子式是_____ ,Y的气态氢化物比Z的气态氢化物的沸点高,缘故是_____ ;
(3)X的最高价氧化物的水化物与其氢化物能化合生成M,M的水溶液显酸性的缘故是_____ (用离子方程式表示)。
(4)①Y和Z可组成一种气态化合物Q,Q能与W的单质在潮湿环境中反应,反应的化学方程式是_____ 。
②在一定条件下,化合物Q与Y的单质反应达平衡时有三种气态物质,反应时,每转移4mol电子放热190.0kJ,该反应的热化学方程式是_____ 。
| X | Y | |
| Z | W |
请回答以下问题:
(1)W在周期表中位置
(2)X和氢能够构成+1价阳离子,其电子式是
(3)X的最高价氧化物的水化物与其氢化物能化合生成M,M的水溶液显酸性的缘故是
(4)①Y和Z可组成一种气态化合物Q,Q能与W的单质在潮湿环境中反应,反应的化学方程式是
②在一定条件下,化合物Q与Y的单质反应达平衡时有三种气态物质,反应时,每转移4mol电子放热190.0kJ,该反应的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有部分短周期(即原子序数为1~18号)元素的性质或原子结构如下表:
(1)按要求用有关的化学用语填充:
T元素的离子符号:______ ;Y离子的电子式__________ ;Z离子的结构示意图_______________ ;
(2)元素Y与氢元素能形成一种10电子的阳离子,该微粒符号是____________ ;
(3)写出元素T的最高价含氧酸与X的最高价含氧酸对应的钠盐反应的化学方程式____
(4)元素Z与某一活泼金属元素组成的盐是重要的化工原料,写出其作为该原料在化工生产上电解的一个重要反应:______________ 。
| 元素编号 | 元素性质或原子结构 |
| T | M层上的电子数等于其内层电子数的差值 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下其单质为双原子分子,且占空气中的含量最大 |
| Z | 该元素的某种含氧酸具有漂白性 |
T元素的离子符号:
(2)元素Y与氢元素能形成一种10电子的阳离子,该微粒符号是
(3)写出元素T的最高价含氧酸与X的最高价含氧酸对应的钠盐反应的化学方程式
(4)元素Z与某一活泼金属元素组成的盐是重要的化工原料,写出其作为该原料在化工生产上电解的一个重要反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化合物KHSO4有关问题。
(1)组成该化合物的四种元素各自所能形成的简单离子中,核外电子排布相同的是_____ (填离子符号)。
(2)与K同周期的基态原子Fe未成对电子数有_____ 个。
(3)基态S原子的价层电子排布式_____ 。
(1)组成该化合物的四种元素各自所能形成的简单离子中,核外电子排布相同的是
(2)与K同周期的基态原子Fe未成对电子数有
(3)基态S原子的价层电子排布式
您最近一年使用:0次
【推荐2】太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:
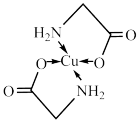
(1)铜位于周期表中___________ 区。
(2)基态二价铜离子的电子排布式为___________ ,已知高温下Cu2O比CuO更稳定,试从核外电子排布角度解释___________ 。
(3)硼核外电子的运动状态的概率密度分布可用___________ 形象化描述。
(4)Fe3+的价电子排布图为___________ 。
(5)N、O、Se三种元素中的第一电离能最大的为:___________ 。

(1)铜位于周期表中
(2)基态二价铜离子的电子排布式为
(3)硼核外电子的运动状态的概率密度分布可用
(4)Fe3+的价电子排布图为
(5)N、O、Se三种元素中的第一电离能最大的为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】近日,比亚迪宣布推出基于磷酸铁锂技术的“刀片电池”,刀片电池能量密度大,安全性高。电池的正极活性材料是LiFePO4。
(1)铁元素位于周期表第四周期第___________ 族;基态Fe2+的最外层电子排布式为 ___________ 。
(2)正极材料LiFePO4的阴离子PO 的空间构型为
的空间构型为 ___________ ,磷原子采取的杂化方式为___________ 。
(3)Fe原子或离子外围有较多能量相近的空轨道,能与SCN -、CN-、C2O 等形成配合物。
等形成配合物。
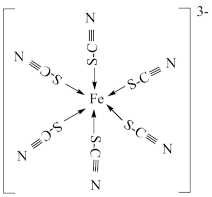
①[Fe(SCN)6]3-的结构简式如图所示,其结构中σ键和π键的个数比为___________ ;[Fe(SCN)6]3- 中含有的化学键类型是___________ (填字母) 。
a.极性共价键 b. 离子键 c.配位键 d.金属键
②K3Fe (C2O4)3·3H2O为可溶于水的晶体,某同学欲检验该晶体中Fe元素的价态,取少量晶体放入试管中,加蒸馏水使其充分溶解,再向试管中滴入几滴0.1mol·L-1KSCN溶液。
已知: i.[Fe (SCN)]2+ (aq)为血红色:
ii.25°C时,[Fe(C2O4)3]3-+SCN- [Fe(SCN)]2++3C2O
[Fe(SCN)]2++3C2O K=6. 31 × 10-17mol2·L-2上述实验方案
K=6. 31 × 10-17mol2·L-2上述实验方案___________ (填“可行”或“不可行”),并解释其原因___________ 。
(1)铁元素位于周期表第四周期第
(2)正极材料LiFePO4的阴离子PO
 的空间构型为
的空间构型为 (3)Fe原子或离子外围有较多能量相近的空轨道,能与SCN -、CN-、C2O
 等形成配合物。
等形成配合物。①[Fe(SCN)6]3-的结构简式如图所示,其结构中σ键和π键的个数比为
a.极性共价键 b. 离子键 c.配位键 d.金属键

②K3Fe (C2O4)3·3H2O为可溶于水的晶体,某同学欲检验该晶体中Fe元素的价态,取少量晶体放入试管中,加蒸馏水使其充分溶解,再向试管中滴入几滴0.1mol·L-1KSCN溶液。
已知: i.[Fe (SCN)]2+ (aq)为血红色:
ii.25°C时,[Fe(C2O4)3]3-+SCN-
 [Fe(SCN)]2++3C2O
[Fe(SCN)]2++3C2O K=6. 31 × 10-17mol2·L-2上述实验方案
K=6. 31 × 10-17mol2·L-2上述实验方案
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语 回答下列问题:
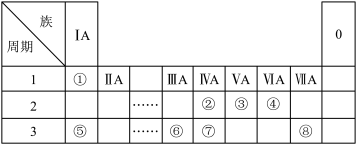
(1)上述八种元素中,最高价氧化物的水化物酸性最强的化合物是___________ (填化学式),③的基态原子核外电子的运动状态有___________ 种。
(2)④、⑤、⑥、⑧的简单离子半径由小到大的顺序是___________ (填离子符号)。②③④三种元素中第一电离能最大的是___________ (填元素符号)
(3)单质④有两种同素异形体,其中沸点高的是___________ (填化学式),原因是___________ ;④和⑤的氢化物所属的晶体类型分别为___________ 和___________ 。

(1)上述八种元素中,最高价氧化物的水化物酸性最强的化合物是
(2)④、⑤、⑥、⑧的简单离子半径由小到大的顺序是
(3)单质④有两种同素异形体,其中沸点高的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素第一电离能变化规律

(1)每个周期的第一种元素的第一电离能_______ ,最后一种元素的第一电离能_______ ,即一般来说,随着核电荷数的递增,元素的第一电离能呈_______ 趋势。
(2)同一族,从上到下第一电离能逐渐_______ 。

(1)每个周期的第一种元素的第一电离能
(2)同一族,从上到下第一电离能逐渐
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)氟原子激发态的电子排布式有_______ (填标号,后同),其中能量较高的是_______ 。
a. b.
b. c.
c. d.
d.
(2)某元素原子位于周期表的第四周期,该原子的最外层只有一个电子,其次外层内的所有轨道电子均成对。写出该基态原子电子排布式为_______ 。
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是图_______ (填标号),判断的根据是_______ ;第三电离能的变化图是图_______ (填标号)。

(4)短周期元素X、Y、Z、W的原子序数依次增大。
①元素的电负性:Z_______ (填“大于”“小于”或“等于”)W。
②简单离子半径:W_______ (填“大于”“小于”或“等于”)Y。
③氢化物的稳定性:X_______ (填“大于”“小于”或“等于”)Z。
(1)氟原子激发态的电子排布式有
a.
 b.
b. c.
c. d.
d.
(2)某元素原子位于周期表的第四周期,该原子的最外层只有一个电子,其次外层内的所有轨道电子均成对。写出该基态原子电子排布式为
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是图

(4)短周期元素X、Y、Z、W的原子序数依次增大。
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | 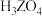 | |||
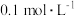 溶液对应的 溶液对应的 | 1.00 | 13.00 | 1.57 | 0.70 |
②简单离子半径:W
③氢化物的稳定性:X
您最近一年使用:0次



