超重元素的假设预言自然界中可能存在114号的稳定同位素X,请根据原子结构理论和元素周期律预测:
(1)X元素位于周期表中第____ 周期,_____ 族,为_____ 元素(金属或非金属)
(2)写出其最高价氧化物及其水化物的化学式分别为___________ 、__________ ,并估计后者为________ 性(填“酸”或“碱”)
(1)X元素位于周期表中第
(2)写出其最高价氧化物及其水化物的化学式分别为
9-10高一下·西藏拉萨·期末 查看更多[2]
更新时间:2016-12-09 00:51:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】如图是元素周期表的一部分,其中每个数字序号代表一种 短周期元素。根据表中所列①~⑩元素,请按要求回答下列问题:

(1)元素⑤形成的氧化物的电子式为_______ ;①、⑦两种元素的最高价氧化物的熔点较高的是________ (填化学式)。
(2)①~⑨元素的最高价氧化物的水化物中酸性最强的是_______ (填化学式)。
(3)由③④⑩三种元素组成的离子化合物中所含有的化学键有______ 。
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为_________ 。
(5)下列事实能说明③非金属性比⑧强的有___________ (填字母)。
a.通常状况下,③的单质是无色气体,⑧的单质是固体
b.③的单质与⑧的氢化物溶液反应,溶液变浑浊
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.常温常压下,③与⑧两元素的简单氢化物的沸点,前者高

(1)元素⑤形成的氧化物的电子式为
(2)①~⑨元素的最高价氧化物的水化物中酸性最强的是
(3)由③④⑩三种元素组成的离子化合物中所含有的化学键有
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为
(5)下列事实能说明③非金属性比⑧强的有
a.通常状况下,③的单质是无色气体,⑧的单质是固体
b.③的单质与⑧的氢化物溶液反应,溶液变浑浊
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.常温常压下,③与⑧两元素的简单氢化物的沸点,前者高
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
(1)第117号元素Ts在周期表中的位置是___________ 。
(2)下图表示铷(Rb)及其化合物的产业链,回答相应问题。___________ (填“小于”或“大于”)钾的离子半径。
②写出由氧化铷制备氢氧化铷的化学方程式___________ 。
③离子推进火箭是通过电离原子气体,转化为阳离子,然后离子被电场力作用加速,通过排气口射出推进器,产生反作用力推动火箭。单质铷适合用于离子推进火箭的原因是___________ 。
(3)阅读短文,回答问题。
硅元素在地壳中的含量仅次于氧。人类很早就利用硅酸盐烧陶制瓷、获得玻璃制品。
1824年,人类成功提炼出硅单质。由石英砂制高纯硅的过程如下:
整个芯片制造过程需要许多高精密度的专业设备,其中不乏我国目前还未完全掌握而被“卡脖子”的技术。我国科学家正开发“碳基”芯片来替代硅基芯片,习近平主席评价此项研究“另辟蹊径,柳暗花明”。
①请依据以上短文,下列说法正确是___________ 。
A.硅元素在自然界中以游离态(单质)形式存在,石英砂的主要成分是SiO2
B.单晶硅做芯片的基底材料与硅元素储量丰富,单晶硅导电性好、耐腐蚀性能优异有关
C.制备单质硅的过程中焦炭过多容易生成副产物金刚砂
D.碳和硅在周期表中位于同一主族,性质相似,因此“碳基”芯片有望替代硅基芯片
②制备高纯硅过程必须严格控制无水无氧,因为SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式___________ 。
③有一类组成最简单的有机硅化合物叫硅烷,硅烷的组成、结构与相应的烷烃相似,化学性质活泼,可在空气中自燃,写出乙硅烷在空气中自燃的化学方程式___________ 。
(1)第117号元素Ts在周期表中的位置是
(2)下图表示铷(Rb)及其化合物的产业链,回答相应问题。
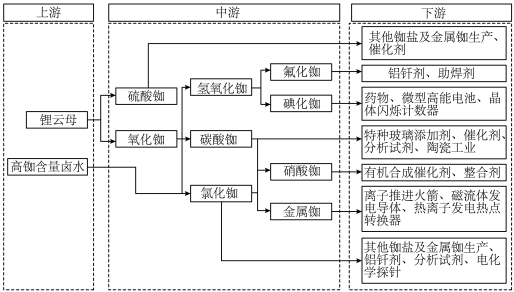
②写出由氧化铷制备氢氧化铷的化学方程式
③离子推进火箭是通过电离原子气体,转化为阳离子,然后离子被电场力作用加速,通过排气口射出推进器,产生反作用力推动火箭。单质铷适合用于离子推进火箭的原因是
(3)阅读短文,回答问题。
硅元素在地壳中的含量仅次于氧。人类很早就利用硅酸盐烧陶制瓷、获得玻璃制品。
1824年,人类成功提炼出硅单质。由石英砂制高纯硅的过程如下:
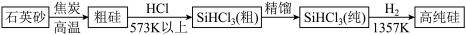
整个芯片制造过程需要许多高精密度的专业设备,其中不乏我国目前还未完全掌握而被“卡脖子”的技术。我国科学家正开发“碳基”芯片来替代硅基芯片,习近平主席评价此项研究“另辟蹊径,柳暗花明”。
①请依据以上短文,下列说法正确是
A.硅元素在自然界中以游离态(单质)形式存在,石英砂的主要成分是SiO2
B.单晶硅做芯片的基底材料与硅元素储量丰富,单晶硅导电性好、耐腐蚀性能优异有关
C.制备单质硅的过程中焦炭过多容易生成副产物金刚砂
D.碳和硅在周期表中位于同一主族,性质相似,因此“碳基”芯片有望替代硅基芯片
②制备高纯硅过程必须严格控制无水无氧,因为SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式
③有一类组成最简单的有机硅化合物叫硅烷,硅烷的组成、结构与相应的烷烃相似,化学性质活泼,可在空气中自燃,写出乙硅烷在空气中自燃的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)二氯化二硫(S2Cl2)是一种琥珀色液体,是合成硫化染料的重要原料。
a.S2Cl2分子中所有原子都满足8电子稳定结构,写出它的电子式____________ ;
b.指出它分子内的键型_________ 。
(2)硒的原子序数为34,硒的单质及其化合物用途非常广泛。
a.硒在元素周期表中的位置是___________ 。
b.硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是________ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
a.S2Cl2分子中所有原子都满足8电子稳定结构,写出它的电子式
b.指出它分子内的键型
(2)硒的原子序数为34,硒的单质及其化合物用途非常广泛。
a.硒在元素周期表中的位置是
b.硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素化学性质最不活泼的是______ ,只有负价而无正价的是__________ ,
(2)最高价氧化物的水化物碱性最强的是__________ ,呈两性的是__________ ;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的__________ ;
(4)在B、C、D、E、F、G、H中,原子半径最大的是__________ .
(5)A和E形成化合物的化学式____________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(1)表中元素化学性质最不活泼的是
(2)最高价氧化物的水化物碱性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在B、C、D、E、F、G、H中,原子半径最大的是
(5)A和E形成化合物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】卤素都是典型的非金属元素,其单质(X2)都具有氧化性。
(1)卤素易形成X-的原因是___________ 。
(2)X2与H2化合的化学方程式是___________ ,其反应条件难易规律是___________ 。
(3)将氯气通入碘化钾溶液中反应的离子方程式是___________ 。
(4)举例说明氯气的氧化性比单质溴的氧化性强:___________ 。
(5)砹(At)属于卤族元素,下列关于砹(At)及其化合物具有的性质推测不正确的是___________(填字母)。
(1)卤素易形成X-的原因是
(2)X2与H2化合的化学方程式是
(3)将氯气通入碘化钾溶液中反应的离子方程式是
(4)举例说明氯气的氧化性比单质溴的氧化性强:
(5)砹(At)属于卤族元素,下列关于砹(At)及其化合物具有的性质推测不正确的是___________(填字母)。
| A.单质砹易溶于某些有机溶剂 |
| B.AgAt是难溶于水的有色固体 |
| C.HAtO4的酸性比HClO4的弱 |
| D.HAt难溶于水,且受热很难分解 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。
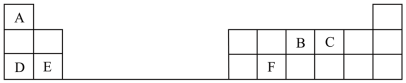
请填写下列空白:
(1)A与B形成 的电子式为
的电子式为________ ;C的原子结构示意图为________ 。
(2)B的最高价氧化物对应的水化物的化学式为_______ ;D、E的最高价氧化物对应的水化物中碱性较弱的是_______  用化学式表示
用化学式表示 ;
;
(3)F的氧化物与氢氧化钠溶液反应的离子方程式为______________ 。

请填写下列空白:
(1)A与B形成
 的电子式为
的电子式为(2)B的最高价氧化物对应的水化物的化学式为
 用化学式表示
用化学式表示 ;
; (3)F的氧化物与氢氧化钠溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期律反映了元素性质的周期性变化规律。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最弱的是_____ (填化学式)。
(2)氮氧化铝(AlON)是一种高硬度、耐高温的防弹材料,Al、O、N三种元素的简单离子半径由大到小的排列顺序是_____ 。
(3)锡为主族元素,其原子结构示意图: 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是_____ ,SnO2能与NaOH溶液反应生成钠盐(Na2SnO3)和水,写出发生反应的化学方程式:_____ 。
(4)硒(34Sn)是与人类的健康密切相关的一种元素,工业上用浓H2SO4焙烧CuSe的方法提取硒(其中Cu转化为CuSO4),且有SO2、H2O和SeO2(固体)生成,写出发生反应的化学方程式:_____ 。理论上该反应每转移1mol电子,可得到的SeO2的质量为_____ g。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最弱的是
(2)氮氧化铝(AlON)是一种高硬度、耐高温的防弹材料,Al、O、N三种元素的简单离子半径由大到小的排列顺序是
(3)锡为主族元素,其原子结构示意图:
 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是(4)硒(34Sn)是与人类的健康密切相关的一种元素,工业上用浓H2SO4焙烧CuSe的方法提取硒(其中Cu转化为CuSO4),且有SO2、H2O和SeO2(固体)生成,写出发生反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表列出了①~⑩十种元素在周期表中的位置:
请按要求回答下列问题:
(1)上述元素中,金属性最强的是___________ (填元素名称),最高价氧化物对应水化物酸性最强的是___________ (写出酸的化学式)。
(2)由元素③形成的单质的电子式为___________ ,由元素⑥和⑨形成化合物乙,请用电子式表示物质乙的形成过程___________ 。
(3)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为___________ 。
(4)可以比较⑤、⑥两元素金属性强弱的实验是___________。
| 族周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ | |||||||
(1)上述元素中,金属性最强的是
(2)由元素③形成的单质的电子式为
(3)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
(4)可以比较⑤、⑥两元素金属性强弱的实验是___________。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】A,B,C,D,E五种短周期元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍。A的一种原子中,质量数与质子数之差为零。D元素原子的最外层电子数为m,次外层电子数为n。E元素原子的L层上电子数为(m+n),M层上电子数为  。请回答下列问题:
。请回答下列问题:
(1)B元素是________ (填元素名称)D元素在周期表中的位置是_______
(2)C与E形成的化合物E3C属于________ (填“原子”“离子”或“分子”)晶体。
(3)由A,D,E元素组成的化合物中存在的化学键类型是________
(4)写出一个E和D形成的化合物与水发生氧化还原反应的离子方程式:________
(5)已知:甲+H2O→丙+丁,该反应不是氧化还原反应。若甲是由N和Cl元素组成的化合物,其分子结构模型如图所示,丁与H2O有相同的电子总数,则丙的电子式为________
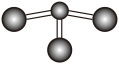
(6)与D同主族且上下相邻的元素M、N,原子电子层数M>N>D,三种元素的氢化物的沸点由大到小的顺序是________ (填化学式)
 。请回答下列问题:
。请回答下列问题:(1)B元素是
(2)C与E形成的化合物E3C属于
(3)由A,D,E元素组成的化合物中存在的化学键类型是
(4)写出一个E和D形成的化合物与水发生氧化还原反应的离子方程式:
(5)已知:甲+H2O→丙+丁,该反应不是氧化还原反应。若甲是由N和Cl元素组成的化合物,其分子结构模型如图所示,丁与H2O有相同的电子总数,则丙的电子式为

(6)与D同主族且上下相邻的元素M、N,原子电子层数M>N>D,三种元素的氢化物的沸点由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据要求填空(所涉及元素均为前20号)
(1)A元素的原子M层有5个电子,则其原子结构示意图为__________________ ;最高价氯化物的化学式_______________________ 。
(2)C元素原子最外层电子是最内层电子的3倍,其形成的离子与Ar元素有相同的电子结构,请写出C离子的结构示意图和电子式:________________ 、_________ 。
(3)标出下列反应的电子转移方向和数目,并填写有关内容:
KClO3+6HCl→3Cl2↑+3H2O+KCl、___________
氧化剂______________ ;氧化产物______________ ;还原剂______________ ;还原产物______________ ;被氧化的元素______________ ;HCl的作用______________ .
(1)A元素的原子M层有5个电子,则其原子结构示意图为
(2)C元素原子最外层电子是最内层电子的3倍,其形成的离子与Ar元素有相同的电子结构,请写出C离子的结构示意图和电子式:
(3)标出下列反应的电子转移方向和数目,并填写有关内容:
KClO3+6HCl→3Cl2↑+3H2O+KCl、
氧化剂
您最近一年使用:0次




