SO2是重要的大气污染物,大量SO2的来源是________________________ 。SO2不仅本身污染大气,而且它在大气中经尘粒催化能与水、氧气作用形成危害更大的酸雨,反应的化学方程式是______________________ 、_____________________ 。
为了降低硫的氧化物造成的污染,所采用的一种方法是在含硫燃料(如煤)中加入生石灰,这种方法称为“钙基固硫”,采用这种方法在燃烧过程中“固硫”反应的化学方程式为_________________________ 。
为了降低硫的氧化物造成的污染,所采用的一种方法是在含硫燃料(如煤)中加入生石灰,这种方法称为“钙基固硫”,采用这种方法在燃烧过程中“固硫”反应的化学方程式为
更新时间:2016-12-09 15:27:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ、直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO₂制得,该反应的离子方程式是:_________________ 。
(2)吸收液吸收SO₂的过程中,pH随n( ):n(
):n( )变化关系如下表:
)变化关系如下表:
①上表判断NaHSO₃溶液显__________ 性,用化学平衡原理解释:____________________ 。
②当吸收液呈中性时,溶液中离子浓度关系正确的是__________ (选填字母)。
a.c(Na+)=2c( )+c(
)+c( )
)
b. c(Na+)>c( )>c(
)>c( )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
c.c(Na+)+ c(H+)=c( )+c(
)+c( )+c(OH-)
)+c(OH-)
Ⅱ. 将0.2 mol·L-1 HA溶液与0.2 mol·L-1 NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则(用“>”、“<”或“=”填写下列空白):
(1)混合溶液中c(HA)________ c(A-);
(2)混合溶液中c(HA)+c(A-)________ 0.1 mol·L-1;
(3)混合溶液由水电离出的c(OH-)______ 0.2 mol·L-1 HA溶液由水电离出的c(H+);
(4)25℃时,如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度________ NaA的水解程度。
(1)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO₂制得,该反应的离子方程式是:
(2)吸收液吸收SO₂的过程中,pH随n(
 ):n(
):n( )变化关系如下表:
)变化关系如下表:n( ):n( ):n( ) ) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO₃溶液显
②当吸收液呈中性时,溶液中离子浓度关系正确的是
a.c(Na+)=2c(
 )+c(
)+c( )
)b. c(Na+)>c(
 )>c(
)>c( )>c(H+)=c(OH-)
)>c(H+)=c(OH-)c.c(Na+)+ c(H+)=c(
 )+c(
)+c( )+c(OH-)
)+c(OH-)Ⅱ. 将0.2 mol·L-1 HA溶液与0.2 mol·L-1 NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则(用“>”、“<”或“=”填写下列空白):
(1)混合溶液中c(HA)
(2)混合溶液中c(HA)+c(A-)
(3)混合溶液由水电离出的c(OH-)
(4)25℃时,如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】为消除燃煤烟气中的SO2、NOx,研究者提出了烟气“脱硫”、“脱硝”的方法。
(1)将烟气与空气按一定比例通入含Fe2+的溶液中,可实现“脱硫”,其过程表示如下:
i:2Fe2++O2+SO2=2Fe3++
ii:2H2O+2Fe3++SO2=2Fe2++ +4H+
+4H+
“脱硫”过程的总反应方程式为_______ 。
(2)在催化剂作用下,用NH3将烟气中NO还原,进行无害化处理,可实现“脱硝”,反应方程式为_______ 。
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”,将烟气中的SO2、NO转化为 、
、 。当烟气中SO2和NO的体积比为4:1时,得到的吸收液中烟气转化生成的
。当烟气中SO2和NO的体积比为4:1时,得到的吸收液中烟气转化生成的 和Cl-的物质的量之比为
和Cl-的物质的量之比为_______ 。
(1)将烟气与空气按一定比例通入含Fe2+的溶液中,可实现“脱硫”,其过程表示如下:
i:2Fe2++O2+SO2=2Fe3++

ii:2H2O+2Fe3++SO2=2Fe2++
 +4H+
+4H+“脱硫”过程的总反应方程式为
(2)在催化剂作用下,用NH3将烟气中NO还原,进行无害化处理,可实现“脱硝”,反应方程式为
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”,将烟气中的SO2、NO转化为
 、
、 。当烟气中SO2和NO的体积比为4:1时,得到的吸收液中烟气转化生成的
。当烟气中SO2和NO的体积比为4:1时,得到的吸收液中烟气转化生成的 和Cl-的物质的量之比为
和Cl-的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知: 为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:
为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:
(1)若镁条在 中燃烧生成黑色粉末(单质)和白色粉末,则
中燃烧生成黑色粉末(单质)和白色粉末,则 的化学式为
的化学式为_______ 。
(2)若常温下, 能与氢氟酸反应生成一种气体和一种液态化合物。
能与氢氟酸反应生成一种气体和一种液态化合物。 和纯碱混合在铁坩埚中熔融生成R的含氧酸盐,
和纯碱混合在铁坩埚中熔融生成R的含氧酸盐, 和纯碱反应的化学方程式为
和纯碱反应的化学方程式为_______ 。
(3)若向酸性 溶液、含酚酞的烧碱溶液中分别通入无色气体
溶液、含酚酞的烧碱溶液中分别通入无色气体 ,两溶液颜色均逐渐褪去。酸性
,两溶液颜色均逐渐褪去。酸性 溶液吸收
溶液吸收 的离子方程式为
的离子方程式为_______ ;向烧碱溶液中通入过量 的离子方程式为
的离子方程式为_______ 。
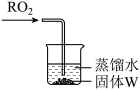
(4)设NA为阿伏加德罗常数的值。若烧杯中固体W为银粉,向该烧杯中通入 ,固体W逐渐溶解(如图所示),则
,固体W逐渐溶解(如图所示),则 的化学式为
的化学式为_______ ,向某密闭容器中充入 和
和 ,则产物的分子数
,则产物的分子数_______ (填“大于”、“小于”或“等于”)2NA。
(5)若 是一种绿色饮用水消毒剂,则
是一种绿色饮用水消毒剂,则 具有
具有_______ 性而能杀菌消毒;工业上,常用+5价R的含氧酸的钠盐和HR的浓溶液在常温下反应制备气态 ,同时还有R单质和水生成,该反应的离子方程式为
,同时还有R单质和水生成,该反应的离子方程式为_______ 。
 为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:
为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:(1)若镁条在
 中燃烧生成黑色粉末(单质)和白色粉末,则
中燃烧生成黑色粉末(单质)和白色粉末,则 的化学式为
的化学式为(2)若常温下,
 能与氢氟酸反应生成一种气体和一种液态化合物。
能与氢氟酸反应生成一种气体和一种液态化合物。 和纯碱混合在铁坩埚中熔融生成R的含氧酸盐,
和纯碱混合在铁坩埚中熔融生成R的含氧酸盐, 和纯碱反应的化学方程式为
和纯碱反应的化学方程式为(3)若向酸性
 溶液、含酚酞的烧碱溶液中分别通入无色气体
溶液、含酚酞的烧碱溶液中分别通入无色气体 ,两溶液颜色均逐渐褪去。酸性
,两溶液颜色均逐渐褪去。酸性 溶液吸收
溶液吸收 的离子方程式为
的离子方程式为 的离子方程式为
的离子方程式为(4)设NA为阿伏加德罗常数的值。若烧杯中固体W为银粉,向该烧杯中通入
 ,固体W逐渐溶解(如图所示),则
,固体W逐渐溶解(如图所示),则 的化学式为
的化学式为 和
和 ,则产物的分子数
,则产物的分子数
(5)若
 是一种绿色饮用水消毒剂,则
是一种绿色饮用水消毒剂,则 具有
具有 ,同时还有R单质和水生成,该反应的离子方程式为
,同时还有R单质和水生成,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】煤是一种常用的燃料,由于煤燃烧产生的废气中含有SO2、NO2和NO等多种有害气体和烟尘,会对环境造成污染,因此需要对煤进行加工后再燃烧或将废气净化后再排放。
(1)将煤直接进行燃烧,造成环境污染的主要原因之一是形成硝酸型酸雨。
①写出煤燃烧废气中有关物质转化为硝酸的化学方程式:_______ 、_______ 。
②下列关于硝酸型酸雨的说法,其中没有道理的是_______ ( 填序号) 。
a.使水中的浮游生物致死,减少鱼类食物来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.破坏臭氧层
d.硝酸与土壤中的矿物质发生作用转化为硝酸盐,向植物提供氮肥
(2)对煤燃烧产生的废气进行常温脱硫处理的基本流程示意图如图,试结合图中信息分别写出废气脱硫并形成副产物(CaSO3、CaSO4和石膏)的过程中所发生的主要化学反应的化学方程式:
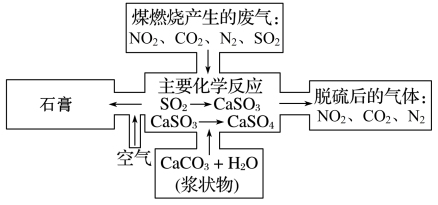
①_______ ;
②_______ ;
③_______ 。
(3)脱硫以后,在废气中含量明显增加的气体是_______ (写物质名称),它对环境的负面影响是_______ 。
(4)检验脱硫后废气中是否含有SO2的简单方法是_______ 。
(1)将煤直接进行燃烧,造成环境污染的主要原因之一是形成硝酸型酸雨。
①写出煤燃烧废气中有关物质转化为硝酸的化学方程式:
②下列关于硝酸型酸雨的说法,其中没有道理的是
a.使水中的浮游生物致死,减少鱼类食物来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.破坏臭氧层
d.硝酸与土壤中的矿物质发生作用转化为硝酸盐,向植物提供氮肥
(2)对煤燃烧产生的废气进行常温脱硫处理的基本流程示意图如图,试结合图中信息分别写出废气脱硫并形成副产物(CaSO3、CaSO4和石膏)的过程中所发生的主要化学反应的化学方程式:

①
②
③
(3)脱硫以后,在废气中含量明显增加的气体是
(4)检验脱硫后废气中是否含有SO2的简单方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式:__ 。
(2)NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
①用酸性(NH2)2CO水溶液吸收NOx,吸收过程中存在HNO2与(NH2)2CO生成N2和CO2的反应。写出该反应的化学方程式:__ 。
②在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。NH3与NO2生成N2的反应中,当生成1molN2时,转移的电子为__ mol。
(2)NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
①用酸性(NH2)2CO水溶液吸收NOx,吸收过程中存在HNO2与(NH2)2CO生成N2和CO2的反应。写出该反应的化学方程式:
②在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。NH3与NO2生成N2的反应中,当生成1molN2时,转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.材料的不断发展可以促进社会进步.
(1)钢铁是制造航母的主要材料,钢铁在潮湿空气中易发生________ 腐蚀,其负极反应是________ .请列举一种防止钢铁腐蚀的方法:________ .
(2)不锈钢丝与棉纤维可织成一种防辐射布料.这种布料属于________ (填字母).
a.合金材料 b.复合材料 c.陶瓷材料
(3)氮化硅是一种新型高温材料,可用于制造汽车发动机.请写出高纯硅和氮气在1300℃时反应制备氮化硅的化学方程式:________ .
II.我国新修订的《环境保护法》,使环境保护有了更严格的法律依据.
(1)往燃煤中加入________ (填化学式),可大大减少产物中的SO2 .
(2)漂白粉用于生活用水的杀菌消毒,漂白粉的有效成分是________ (填化学式).治理废水中的重金属污染物可用沉淀法.例如,往含铬(Cr3+)废水中加入石灰乳使Cr3+转变为________ (填化学式)沉淀而除去.
(1)钢铁是制造航母的主要材料,钢铁在潮湿空气中易发生
(2)不锈钢丝与棉纤维可织成一种防辐射布料.这种布料属于
a.合金材料 b.复合材料 c.陶瓷材料
(3)氮化硅是一种新型高温材料,可用于制造汽车发动机.请写出高纯硅和氮气在1300℃时反应制备氮化硅的化学方程式:
II.我国新修订的《环境保护法》,使环境保护有了更严格的法律依据.
(1)往燃煤中加入
(2)漂白粉用于生活用水的杀菌消毒,漂白粉的有效成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学与生活息息相关。请根据你所学知识回答下列问题。
(1)在葡萄酒酸制过程中添加适量二氧化硫不仅能杀菌,还能防止葡萄酒中的一些成分被氧化,起到保质的作用。这是利用了二氧化硫___________ 、能杀菌消毒和___________ 的性质。
(2)一些化工生产以及煤、石油的燃烧都可能生成二氧化硫,若任由其排放会造成大气污染,还可能形成___________ ,危害地面生物。在煤中加入适量生石灰可有效防止二氧化硫的排放,原因是___________ (用化学方程式表示)。某化学兴趣小组的同学收集到我市某电厂的尾气,将其___________ (填操作及现象),说明尾气中无二氧化硫。
(3)为早日实现“碳达峰、碳中和”的目标,我国大力发展光伏发电代替火力发电。光伏电池所用材料是___________ ;“碳达峰、碳中和”中的“碳”指的是___________ 。北京冬奥会亮相的氢燃料电动汽车是典型的绿色环保车,电池采用碱性电解质,工作时的负极反应方程式为___________ 。
(1)在葡萄酒酸制过程中添加适量二氧化硫不仅能杀菌,还能防止葡萄酒中的一些成分被氧化,起到保质的作用。这是利用了二氧化硫
(2)一些化工生产以及煤、石油的燃烧都可能生成二氧化硫,若任由其排放会造成大气污染,还可能形成
(3)为早日实现“碳达峰、碳中和”的目标,我国大力发展光伏发电代替火力发电。光伏电池所用材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处。
(1)煤燃烧产生的SO2所形成的酸雨中,SO2 最终转化成的酸是________ (填化学式),在煤中加入适量石灰石,可以大大减少煤燃烧时SO2的排放,发生反应的化学方程式:__________________________ 。
(2)垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有________ (填字母)标志的垃圾筒内。

(3)工业废水需处理达标后才能排放。下列废水处理的方法合理的是________ (填字母)。
a.用中和法除去废水中的酸
b.用混凝剂除去废水中的重金属离子
c.用氯气除去废水中的悬浮物
(4)下列做法会加剧温室效应的是____________ (填字母)。
a.植树造林 b.燃煤供暖 c.风力发电
(5)空气质量报告的各项指标可以反映出各地空气的质量。下列气体已纳入我国空气质量报告的是________ (填字母)。
a.CO2 b.N2 c.NO2
(6)选择环保的装修材料可以有效地减少居室污染。劣质胶合板释放的主要污染物是_______ (填字母)。
a.NO b.CO c.甲醛
(1)煤燃烧产生的SO2所形成的酸雨中,SO2 最终转化成的酸是
(2)垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有

(3)工业废水需处理达标后才能排放。下列废水处理的方法合理的是
a.用中和法除去废水中的酸
b.用混凝剂除去废水中的重金属离子
c.用氯气除去废水中的悬浮物
(4)下列做法会加剧温室效应的是
a.植树造林 b.燃煤供暖 c.风力发电
(5)空气质量报告的各项指标可以反映出各地空气的质量。下列气体已纳入我国空气质量报告的是
a.CO2 b.N2 c.NO2
(6)选择环保的装修材料可以有效地减少居室污染。劣质胶合板释放的主要污染物是
a.NO b.CO c.甲醛
您最近一年使用:0次



