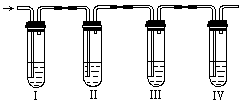
某学生发现氯水能使有色布条褪色,氯水的成分比较复杂,那么氯水中究竟什么成分具有漂白性呢?带着疑问,他做了如下探究:
(1)查找资料后得知氯水的成分有____ 、___ 、____ 、____ 、____ 、____ 、____ 。
(2)根据资料查阅和实验结果分析, 新制的氯水呈____ 色,氯水中含有多种微粒.将紫色石蕊试液滴入其中,溶液显红色.起作用的微粒是___ ;过一会儿,溶液的颜色逐渐褪去,起作用的微粒是___ 。该物质之所以具有漂白性,与它的_______ (填性质)有关。往氯水中滴入硝酸银溶液,产生白色沉淀,起作用的微粒是____ 。氯水能使淀粉碘化钾试纸变蓝,起作用的是____ .(本小题中除第一个外,其余每个空格处都请填写微粒的符号)
(3)从以上过程可看出,该学生的探究活动体现了最基本的科学研究方法,即:
提出问题→________ →________ →分析归纳→得出结论
(1)查找资料后得知氯水的成分有
(2)根据资料查阅和实验结果分析, 新制的氯水呈
(3)从以上过程可看出,该学生的探究活动体现了最基本的科学研究方法,即:
提出问题→
10-11高一上·上海·期中 查看更多[1]
(已下线)2010年上海市吴淞中学高一上学期期中考试化学试卷
更新时间:2016-12-09 01:19:07
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】新制氯水的成分多样,某研究性学习小组欲检验新制氯水的成分来确定氯气与水是否反应。该小组设计下列实验及表格,请帮助他们完成实验及表格,并分析氯气与水是否反应。
氯气与水____________ (填“反应”或“不反应”);若反应,其反应方程式为____________
| 实验目的 | 操作或试剂 | 现象及结论 |
| 检验Cl2 | 观察溶液颜色 | (1) |
| 检验H+ | 铁粉 | (2) |
| 检验Cl- | AgNO3溶液 | (3) |
| 检验HClO | 将稀盐酸滴到干燥的红色纸条上 | (4) |
| 在干燥的氯气中放入干燥的红色纸条 | (5) | |
| 将新制氯水滴到干燥的红色纸条上 | (6) |
氯气与水
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】氯元素是生产生活中常见的非金属元素。某同学探究Cl2及其化合物的性质。
(1)氯气能溶于水,氯气的水溶液称为氯水,写出Cl2与水反应的化学方程式___________ 。
(2)某同学把品红试纸(染有品红的纸)伸入氯水中,品红试纸褪色。
发现问题:氯水中的哪些成分使品红试纸褪色?
猜想:
猜想1:溶液中的H2O使品红试纸褪色;
猜想2:溶液中的___________ (填化学式)使品红褪色;
猜想3:盐酸使品红试纸褪色;
猜想4:溶液中的HClO使品红试纸褪色。
实验探究:
综合分析:氯水中的___________ (填化学式)使品红试纸褪色,具有漂白作用。
(3)向氯水中加入NaOH溶液,氯水浅黄绿色褪去。原因是(用相关化学方程式解释)___________ 。
(4)久置氯水最终变成了稀盐酸,原因是___________ 。
(1)氯气能溶于水,氯气的水溶液称为氯水,写出Cl2与水反应的化学方程式
(2)某同学把品红试纸(染有品红的纸)伸入氯水中,品红试纸褪色。
发现问题:氯水中的哪些成分使品红试纸褪色?
猜想:
猜想1:溶液中的H2O使品红试纸褪色;
猜想2:溶液中的
猜想3:盐酸使品红试纸褪色;
猜想4:溶液中的HClO使品红试纸褪色。
实验探究:
| 实验操作 | 实验现象 | 过程分析 |
| ①把品红试纸伸入水中 | 没有褪色 | 猜想1不成立 |
| ②把品红试纸伸入 | 没有褪色 | 猜想2不成立 |
| ③ | 没有褪色 | 猜想3不成立 |
(3)向氯水中加入NaOH溶液,氯水浅黄绿色褪去。原因是(用相关化学方程式解释)
(4)久置氯水最终变成了稀盐酸,原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.如图所示装置可用于二氧化锰与浓盐酸在加热条件下制取氯气,并利用产物进行后续实验,请填写下列空白:

(1)写出二氧化锰与浓盐酸反应的化学方程式:____ 。
(2)在该反应中,HCl充当的是____ (填“氧化剂”或“还原剂”)。
(3)洗气瓶B中盛有饱和食盐水,洗气瓶C中盛有品红溶液,在洗气瓶D中盛有石灰乳,则洗气瓶C中观察到的现象是____ ;洗气瓶D中发生反应的化学方程式是____ 。
Ⅱ.氯水中含有多种成分,因而具有多重性质。根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。

(4)能证明氯水具有漂白性的是____ (填“a”“b”“c”或“d”)。
(5)c过程中的现象是____ 。
(6)b过程中的离子方程式为_____ 。

(1)写出二氧化锰与浓盐酸反应的化学方程式:
(2)在该反应中,HCl充当的是
(3)洗气瓶B中盛有饱和食盐水,洗气瓶C中盛有品红溶液,在洗气瓶D中盛有石灰乳,则洗气瓶C中观察到的现象是
Ⅱ.氯水中含有多种成分,因而具有多重性质。根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。

(4)能证明氯水具有漂白性的是
(5)c过程中的现象是
(6)b过程中的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)鉴别新制的氯水与久置的氯水_______________________________________________ 。
(2)次氯酸不稳定,见光易分解生成氯化氢和氧气。请设计实验证明有氧气生成________ 。
(1)鉴别新制的氯水与久置的氯水
(2)次氯酸不稳定,见光易分解生成氯化氢和氧气。请设计实验证明有氧气生成
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某学习小组验证氯水中具有漂白性的物质是HClO,实验如下(装置的气密性已检验)。

(1)NaOH溶液的作用是______ 。
(2)实验Ⅰ,试剂a为H2O,制得氯水。氯水呈黄绿色是由于其中含有______ 。Cl2与H2O反应的化学方程式为______ 。
(3)实验Ⅱ,试剂a为CCl4,制得Cl2的CCl4溶液(Cl2与CCl4不反应)。取稀盐酸、新制氯水和Cl2的CCl4溶液,分别滴在三张红色纸条上,可观察到______ ,证实氯水中具有漂白性的物质是HClO。

(1)NaOH溶液的作用是
(2)实验Ⅰ,试剂a为H2O,制得氯水。氯水呈黄绿色是由于其中含有
(3)实验Ⅱ,试剂a为CCl4,制得Cl2的CCl4溶液(Cl2与CCl4不反应)。取稀盐酸、新制氯水和Cl2的CCl4溶液,分别滴在三张红色纸条上,可观察到
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某化学兴趣小组用如图装置制取并探究氯气的性质。[A装置中发生反应的化学方程式: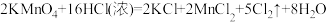 ]
]

(1)A装置中a仪器的名称是_____________________ 。
(2)实验室制氯气也可用 MnO2与浓盐酸反应,化学方程式为_____________________ 。
(3)实验进行一段时间后,可观察到_____________________ (填“B”或“C”)装置中有色布条褪色,请用化学方程式表示其褪色原因_____________________ 。
(4)当氯气进入D装置后,可观察到溶液颜色变为_____________________ (填“红色”或“蓝色”)。
(5)E装置的作用是_____________________ 。
(6)用 31.6g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下_____________________ L氯气。
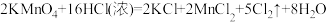 ]
]
(1)A装置中a仪器的名称是
(2)实验室制氯气也可用 MnO2与浓盐酸反应,化学方程式为
(3)实验进行一段时间后,可观察到
(4)当氯气进入D装置后,可观察到溶液颜色变为
(5)E装置的作用是
(6)用 31.6g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】实验室制取的乙烯中常混有少量的 ,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:

(1)图中a、b、c、d装置盛放的试剂依次是___________________ (填序号)。
A.品红溶液 B. 溶液 C.浓硫酸 D.酸性高锰酸钾溶液
溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明 存在的实验现象是
存在的实验现象是______________________________________ 。
(3)使用装置b的目的是________________________ 。
(4)使用装置c的目的是________________________ 。
(5)能说明混合气体中含有乙烯的现象是____________________________________________________ 。
 ,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
(1)图中a、b、c、d装置盛放的试剂依次是
A.品红溶液 B.
 溶液 C.浓硫酸 D.酸性高锰酸钾溶液
溶液 C.浓硫酸 D.酸性高锰酸钾溶液(2)能说明
 存在的实验现象是
存在的实验现象是(3)使用装置b的目的是
(4)使用装置c的目的是
(5)能说明混合气体中含有乙烯的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某校化学实验兴趣小组欲采用如图所示的实验装置制备Cl2,同时进行与氯气有关的某些实验,按要求回答问题。
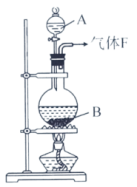
(1)A是浓盐酸,B是二氧化锰,将A滴入B中时发生反应的离子方程式为___ 。
(2)某同学组装仪器时发现没有酒精灯,于是选择了另一种方式制备,写出该反应原理的化学反应方程式:___ 。
(3)甲同学用一定量的浓盐酸与足量的MnO2反应制Cl2,结果制得的Cl2体积比理论上应制得的体积小,这是由于反应过程中盐酸浓度变小造成的。请列举2条导致盐酸浓度变小的原因:___ 。
(4)在实验室中,乙同学欲用如图的装置净化氯气,则瓶①②中应盛放的试剂分别是①___ ,②___ (填试剂名称)。
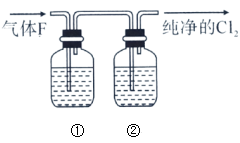
(5)氯气通入饱和溶液能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有___ 。(填“盐酸”或“次氯酸”)
(6)将新制氯水逐滴滴入到含有酚酞氢氧化钠溶液中,红色褪去,其原因可能是:
①氢氧化钠溶液中的氢氧根被氯水中的酸中和,溶液不再显碱性;
②___ 。
取褪色后的溶液,加入___ ,若溶液不能恢复红色,说明原因是___ (填“①”或“②”)。

(1)A是浓盐酸,B是二氧化锰,将A滴入B中时发生反应的离子方程式为
(2)某同学组装仪器时发现没有酒精灯,于是选择了另一种方式制备,写出该反应原理的化学反应方程式:
(3)甲同学用一定量的浓盐酸与足量的MnO2反应制Cl2,结果制得的Cl2体积比理论上应制得的体积小,这是由于反应过程中盐酸浓度变小造成的。请列举2条导致盐酸浓度变小的原因:
(4)在实验室中,乙同学欲用如图的装置净化氯气,则瓶①②中应盛放的试剂分别是①

(5)氯气通入饱和溶液能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有
(6)将新制氯水逐滴滴入到含有酚酞氢氧化钠溶液中,红色褪去,其原因可能是:
①氢氧化钠溶液中的氢氧根被氯水中的酸中和,溶液不再显碱性;
②
取褪色后的溶液,加入
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】如图是实验室制备氯气并进行一系列相关实验的装置。请回答下列问题:
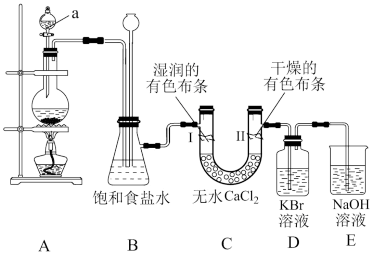
(1)仪器a的名称是_______ 。
(2)按图组装好装置后,首先应进行的操作是_______ 。
(3)实验开始后,I、II处的有色布条褪色的是_______ 处。(填“I”或“II”)
(4)装置A的烧瓶中发生反应的化学方程式为_______ 。
(5)反应进行一段时间后D中的现象是_______ ,发生反应的离子方程式为_______ 。
(6)装置E的作用是_______ 。
(7)若在E中得到NaCl、NaClO、NaClO3的混合液,其中 和
和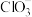 的物质的量之比为4:1,则Cl2与NaOH溶液反应时,被还原的氯原子与被氧化的氯原子的个数比为
的物质的量之比为4:1,则Cl2与NaOH溶液反应时,被还原的氯原子与被氧化的氯原子的个数比为_______ 。

(1)仪器a的名称是
(2)按图组装好装置后,首先应进行的操作是
(3)实验开始后,I、II处的有色布条褪色的是
(4)装置A的烧瓶中发生反应的化学方程式为
(5)反应进行一段时间后D中的现象是
(6)装置E的作用是
(7)若在E中得到NaCl、NaClO、NaClO3的混合液,其中
 和
和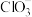 的物质的量之比为4:1,则Cl2与NaOH溶液反应时,被还原的氯原子与被氧化的氯原子的个数比为
的物质的量之比为4:1,则Cl2与NaOH溶液反应时,被还原的氯原子与被氧化的氯原子的个数比为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】SO2和焦亚硫酸钠(Na2S2O5)可作食品添加剂。某小组进行如下探究:
I. 制备SO2
(1)①实验室用 NaHSO3和70%H2SO4制取SO2,反应的化学方程式为___________ 。
②欲收集干燥的SO2,选择下列必要 的装置,按气流方向连接顺序为___________ (填仪器接口的字母编号)。

Ⅱ. 探究焦亚硫酸钠的性质
(2)焦亚硫酸钠易被氧化而变质。该小组设计实验方案,检验焦亚硫酸钠样品氧化变质的程度,完成下列表中的内容。
已知: 2NaHSO3=Na2S2O5+H2O
(3)为检验某白葡萄酒中是否含有Na2S2O5,甲同学设计的实验方案是用酸性KMnO4溶液进行检验, 乙同学认为该方案不可行, 乙同学的理由是___________ 。
Ⅲ.该小组利用下列装置测定空气中SO2的含量。

(4)①通空气样品的导管末端是带许多小孔的玻璃球泡, 其主要作用是___________ ;
②若空气流速为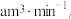 当观察到
当观察到___________ 时,结束计时,测定耗时为tmin。假定样品中的SO2可被溶液充分吸收,该空气样品中SO2,的含量为___________ mg·m-3。
I. 制备SO2
(1)①实验室用 NaHSO3和70%H2SO4制取SO2,反应的化学方程式为
②欲收集干燥的SO2,选择下列

Ⅱ. 探究焦亚硫酸钠的性质
(2)焦亚硫酸钠易被氧化而变质。该小组设计实验方案,检验焦亚硫酸钠样品氧化变质的程度,完成下列表中的内容。
已知: 2NaHSO3=Na2S2O5+H2O
| 实验编号 | 实验步骤 | 现象 | 结论 |
| i | 取少量样品于试管中,加入除氧蒸馏水 | 固体溶解,得到无色溶液 | / |
| ii | 取少量i的溶液于试管中,加入 | | 样品已氧化变质 |
| iii | 另取少量i的溶液于试管中,加入酸性KMnO4溶液,振荡 | | 样品未完全氧化变质 |
(3)为检验某白葡萄酒中是否含有Na2S2O5,甲同学设计的实验方案是用酸性KMnO4溶液进行检验, 乙同学认为该方案不可行, 乙同学的理由是
Ⅲ.该小组利用下列装置测定空气中SO2的含量。

(4)①通空气样品的导管末端是带许多小孔的玻璃球泡, 其主要作用是
②若空气流速为
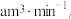 当观察到
当观察到
您最近一年使用:0次