已知A、B、C、D、E、F 6种物质的转化关系如下
(1) A+B→C+H2O
(2) C+KOH→D↓(蓝色)+E
(3) B+D→C+H2O
(4) E+BaCl2→KCl + F↓(白色,不溶于稀硝酸)
(5)G+B→CO2↑+ F↓+ H2O,反应中B与CO2的物质的量之比为1:2
根据上述变化关系填空:
(1)请写出下列物质的化学式:B_______ ;C _______ ;G __________ 。
(2)检验E中的阴离子的实验是______________________________________________
(3)往G的溶液中滴加过量的KOH,反应的离子方程式为__________________
(1) A+B→C+H2O
(2) C+KOH→D↓(蓝色)+E
(3) B+D→C+H2O
(4) E+BaCl2→KCl + F↓(白色,不溶于稀硝酸)
(5)G+B→CO2↑+ F↓+ H2O,反应中B与CO2的物质的量之比为1:2
根据上述变化关系填空:
(1)请写出下列物质的化学式:B
(2)检验E中的阴离子的实验是
(3)往G的溶液中滴加过量的KOH,反应的离子方程式为
10-11高一上·四川成都·期中 查看更多[1]
(已下线)2010年四川省成都九中高一上学期期中考试化学试卷
更新时间:2016/12/09 01:20:46
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
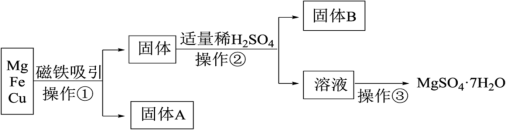
【推荐1】有Mg、Fe、Cu的混合粉末,分离得到MgSO4·7H2O过程如下:___________ 。
(2)操作②的名称是___________ ,需要用到的主要玻璃仪器有 ___________ 、玻璃棒,其中玻璃棒的作用是___________ 。
(3)操作②发生的离子反应方程式为___________ ,属于___________ 反应。(填基本反应类型)
(4)实验中可选用适量的下列试剂中的代替稀H2SO4___________ (填标号)。
A. CuSO4溶液 B.FeSO4溶液 C.稀盐酸
(5)操作③主要包含蒸发浓缩、___________ 、过滤、洗涤烘干等。
(2)操作②的名称是
(3)操作②发生的离子反应方程式为
(4)实验中可选用适量的下列试剂中的代替稀H2SO4
A. CuSO4溶液 B.FeSO4溶液 C.稀盐酸
(5)操作③主要包含蒸发浓缩、
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】已知:单质 为目前人类使用最广泛的金属,氧化物
为目前人类使用最广泛的金属,氧化物 为具有磁性的黑色晶体,根据下列转化关系填空。
为具有磁性的黑色晶体,根据下列转化关系填空。

(1)试判断: 的
的名称 为______________ ,写出 的化学反应方程式
的化学反应方程式______________ 。
(2)实验室检验 溶液中的阳离子时,可加入氢氧化钠溶液,若先产生
溶液中的阳离子时,可加入氢氧化钠溶液,若先产生__________ 色沉淀,该沉淀在空气中迅速变为灰绿色,最终变为________ 色,则含该离子。
(3)实验室检验 溶液中的阳离子时,通常可滴加
溶液中的阳离子时,通常可滴加________ (填写化学式),若溶液变为红色,则含该离子。
(4)写出固体 与过量盐酸反应的
与过量盐酸反应的离子方程式 ________________ 。
(5)写出 的
的离子方程式 __________________________________ 。
 为目前人类使用最广泛的金属,氧化物
为目前人类使用最广泛的金属,氧化物 为具有磁性的黑色晶体,根据下列转化关系填空。
为具有磁性的黑色晶体,根据下列转化关系填空。 
(1)试判断:
 的
的 的化学反应方程式
的化学反应方程式(2)实验室检验
 溶液中的阳离子时,可加入氢氧化钠溶液,若先产生
溶液中的阳离子时,可加入氢氧化钠溶液,若先产生(3)实验室检验
 溶液中的阳离子时,通常可滴加
溶液中的阳离子时,通常可滴加(4)写出固体
 与过量盐酸反应的
与过量盐酸反应的(5)写出
 的
的
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】茫茫大海是化学元素溴的“故乡”,海水中溴的含量约为67 mg/L。从海水中提取溴的工业流程如下:
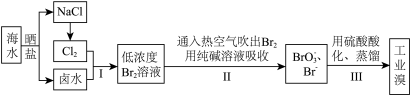
(1)步骤I中已获得了游离态的溴,步骤II中又将之转变成化合态的溴,其目的是_______ 。
(2)步骤II中通入热空气或水蒸气吹出Br2,利用了溴的______(填字母)。
(3)上述流程中吹出的溴蒸气也可先用SO2水溶液吸收,反应生成HBr和H2SO4,该反应中的氧化剂是________ , 还原剂是_______ ,然后用氯气氧化上述反应的产物后蒸馏,写出氯气氧化HBr的离子方程式:____________ 。

(1)步骤I中已获得了游离态的溴,步骤II中又将之转变成化合态的溴,其目的是
(2)步骤II中通入热空气或水蒸气吹出Br2,利用了溴的______(填字母)。
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
(3)上述流程中吹出的溴蒸气也可先用SO2水溶液吸收,反应生成HBr和H2SO4,该反应中的氧化剂是
您最近一年使用:0次
【推荐1】有一包白色固体,可能含有Na2CO3、KNO3、NaCl、BaSO4、AgNO3 、CuSO4。按下列步骤实验:①取少量固体溶于水,得到无色溶液;②在所得的溶液中滴加硝酸银溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解,并有气体产生。根据上述实验现象判断:
(1)一定存在的物质是___________ ;
(2)一定不存在的物质是___________ ;
(3)可能存在的物质是___________ ;如何检验该物质___________
(1)一定存在的物质是
(2)一定不存在的物质是
(3)可能存在的物质是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】现有一包固体粉末,其中可能含有如下五种物质:CaCO3、K2CO3、Na2SO4、NaCl、CuSO4。现进行如下实验:①溶于水得无色溶液,溶液中无沉淀出现;②向溶液中加入BaCl2溶液生成白色沉淀,再加盐酸时沉淀消失。根据上述实验现象推断:
(1)一定不存在的物质是_____________________ ;
(2)写出加入盐酸时沉淀消失的离子反应方程式___________________________ ;
(3)可能存在的物质是___________ ;
(4)写出下列物质在水溶液中的电离方程式
H2CO3:___________________________ ;
NH4HCO3 :___________________________ ;
Ca(OH)2:___________________________ 。
(1)一定不存在的物质是
(2)写出加入盐酸时沉淀消失的离子反应方程式
(3)可能存在的物质是
(4)写出下列物质在水溶液中的电离方程式
H2CO3:
NH4HCO3 :
Ca(OH)2:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】某溶液中只可能存在Br-、CO 、SO
、SO 、Cl-、K+、Ca2+、Na+七种离子中的某几种。现取该溶液进行下列实验:
、Cl-、K+、Ca2+、Na+七种离子中的某几种。现取该溶液进行下列实验:
①向溶液中滴加足量的氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量的BaCl2溶液,无沉淀生成;
③用洁净的铂丝蘸取原溶液,在酒精灯外焰上灼烧,火焰呈黄色。
据此可以回答下列问题:
(1)由实验现象①可知:溶液中肯定含有的离子是__ ;溶液变橙色的原因(用离子方程式表示):__ 。
(2)由实验现象②可知:溶液中肯定没有的离子是___ 。
(3)综合上述分析可知:溶液中可能含有的离子是__ ;一定不含有的离子是__ 。
 、SO
、SO 、Cl-、K+、Ca2+、Na+七种离子中的某几种。现取该溶液进行下列实验:
、Cl-、K+、Ca2+、Na+七种离子中的某几种。现取该溶液进行下列实验:①向溶液中滴加足量的氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量的BaCl2溶液,无沉淀生成;
③用洁净的铂丝蘸取原溶液,在酒精灯外焰上灼烧,火焰呈黄色。
据此可以回答下列问题:
(1)由实验现象①可知:溶液中肯定含有的离子是
(2)由实验现象②可知:溶液中肯定没有的离子是
(3)综合上述分析可知:溶液中可能含有的离子是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】磺酰氯( )是锂电池正极活性物质,熔点
)是锂电池正极活性物质,熔点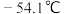 ,沸点
,沸点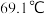 ,遇到潮湿的空气易水解。实验室可依据反应
,遇到潮湿的空气易水解。实验室可依据反应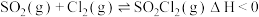 制备磺酰氯,实验装置如图
制备磺酰氯,实验装置如图 夹持装置均未画出
夹持装置均未画出 。
。
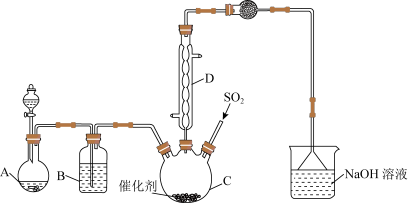
请回答下列问题:
(1)装置 可制取氯气,反应的离子方程式为
可制取氯气,反应的离子方程式为______ 。
(2)装置 中的试剂是
中的试剂是______ ,仪器 的名称是
的名称是______ ,仪器 的作用是
的作用是______ 。
(3)为了提高装置 中反应物的转化率,反应条件最好选择
中反应物的转化率,反应条件最好选择______  填标号
填标号 。
。
a.冰水浴 b.常温 c.加热至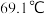
(4) 遇到潮湿的空气易产生大量白雾,该反应的化学方程式为
遇到潮湿的空气易产生大量白雾,该反应的化学方程式为______ 。
(5)磺酰氯 应储存于阴凉、干燥、通风的库房,但久置后会呈现黄色,原因是
应储存于阴凉、干燥、通风的库房,但久置后会呈现黄色,原因是______ 。
(6)氯磺酸(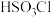 )分解也可得到磺酰氯
)分解也可得到磺酰氯 ,方程式为
,方程式为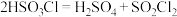 ,此方法得到的产品中混有硫酸。
,此方法得到的产品中混有硫酸。
 从分解产物中分离磺酰氯的方法是
从分解产物中分离磺酰氯的方法是______ 。
 氯磺酸(
氯磺酸(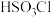 )水解产物中检验氯离子的实验操作是
)水解产物中检验氯离子的实验操作是______ 。
 )是锂电池正极活性物质,熔点
)是锂电池正极活性物质,熔点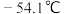 ,沸点
,沸点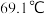 ,遇到潮湿的空气易水解。实验室可依据反应
,遇到潮湿的空气易水解。实验室可依据反应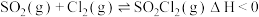 制备磺酰氯,实验装置如图
制备磺酰氯,实验装置如图 夹持装置均未画出
夹持装置均未画出 。
。
请回答下列问题:
(1)装置
 可制取氯气,反应的离子方程式为
可制取氯气,反应的离子方程式为(2)装置
 中的试剂是
中的试剂是 的名称是
的名称是 的作用是
的作用是(3)为了提高装置
 中反应物的转化率,反应条件最好选择
中反应物的转化率,反应条件最好选择 填标号
填标号 。
。a.冰水浴 b.常温 c.加热至
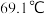
(4)
 遇到潮湿的空气易产生大量白雾,该反应的化学方程式为
遇到潮湿的空气易产生大量白雾,该反应的化学方程式为(5)磺酰氯
 应储存于阴凉、干燥、通风的库房,但久置后会呈现黄色,原因是
应储存于阴凉、干燥、通风的库房,但久置后会呈现黄色,原因是(6)氯磺酸(
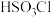 )分解也可得到磺酰氯
)分解也可得到磺酰氯 ,方程式为
,方程式为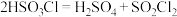 ,此方法得到的产品中混有硫酸。
,此方法得到的产品中混有硫酸。 从分解产物中分离磺酰氯的方法是
从分解产物中分离磺酰氯的方法是 氯磺酸(
氯磺酸(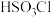 )水解产物中检验氯离子的实验操作是
)水解产物中检验氯离子的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
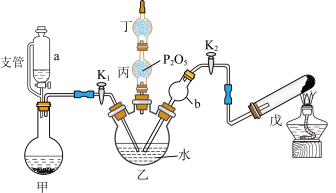
【推荐2】亚硫酸氢铵(NH4HSO3)是一种重要的化工原料,常用作棉织物和有机物的漂白剂、食品药品的防腐剂、水处理领域的脱氧剂、染料、造纸、制革、化学合成等工业中的还原剂。某化学兴趣小组设计如图装置(夹持装置已省略)利用二氧化硫和氨气反应制备亚硫酸氢铵,实验步骤如下:
①组装好仪器,_______;
②在各装置中加入相应的试剂;
③调节活塞K1、K2的开关顺序,先后通入气体,充分反应得到亚硫酸氢铵溶液;
④再将溶液冷却结晶、离心分离得到产品。
(1)请将实验步骤①补充完整_______ 。
(2)甲装置中仪器a的支管作用是_______ 。
(3)乙装置中仪器b的作用是_______ ,丁装置中的试剂为_______ 。
(4)戊装置的试管内发生反应的化学方程式为_______ 。
(5)下列关于该实验的叙述正确的是_______ (填字母)。
A.实验步骤③中应先关闭K2、打开活塞K1,通入一种气体;一段时间后关闭K1、打开K2,通入另一种气体
B.实验步骤③中应先关闭K1、打开活塞K2,通入一种气体;一段时间后关闭K2、打开K1,通入另一种气体
C.实验步骤④中若将溶液蒸发结晶,产品的产率可能会降低
(6)亚硫酸氢铵有较强的还原性,设计实验检验制备的亚硫酸氢铵样品是否被氧化的方法是:取适量样品于试管中,加水溶解,_______ (请完成实验操作、现象和结论)。
①组装好仪器,_______;
②在各装置中加入相应的试剂;
③调节活塞K1、K2的开关顺序,先后通入气体,充分反应得到亚硫酸氢铵溶液;
④再将溶液冷却结晶、离心分离得到产品。
(1)请将实验步骤①补充完整
(2)甲装置中仪器a的支管作用是
(3)乙装置中仪器b的作用是
(4)戊装置的试管内发生反应的化学方程式为
(5)下列关于该实验的叙述正确的是
A.实验步骤③中应先关闭K2、打开活塞K1,通入一种气体;一段时间后关闭K1、打开K2,通入另一种气体
B.实验步骤③中应先关闭K1、打开活塞K2,通入一种气体;一段时间后关闭K2、打开K1,通入另一种气体
C.实验步骤④中若将溶液蒸发结晶,产品的产率可能会降低
(6)亚硫酸氢铵有较强的还原性,设计实验检验制备的亚硫酸氢铵样品是否被氧化的方法是:取适量样品于试管中,加水溶解,
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】硫的化合物在生产、生活中应用广泛。
Ⅰ.某兴趣小组探究SO2气体还原Fe3+、I2。
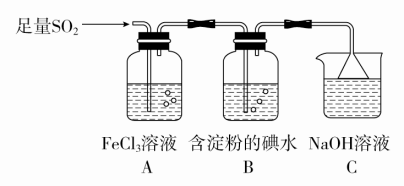
(1)通入足量SO2后,装置B中的现象是__________ ;装置C的作用是_________ 。
(2)该小组同学认为SO2与FeCl3溶液发生的是氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:________________ 。
②请设计实验方案验证有Fe2+生成:________________________ 。
Ⅱ.(3)铬是环境中的一种主要污染物,可以用焦亚硫酸钠(Na2S2O5)处理含铬酸性废水(含有 ),利用氧化还原反应,将六价铬还原为三价铬,
),利用氧化还原反应,将六价铬还原为三价铬,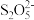 被氧化为
被氧化为 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为__________ 。
(4)已知: Na2S2O5溶于水会生成NaHSO3。检验Na2S2O5晶体在空气中已被氧化的实验方法是______ 。
Ⅰ.某兴趣小组探究SO2气体还原Fe3+、I2。

(1)通入足量SO2后,装置B中的现象是
(2)该小组同学认为SO2与FeCl3溶液发生的是氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:
②请设计实验方案验证有Fe2+生成:
Ⅱ.(3)铬是环境中的一种主要污染物,可以用焦亚硫酸钠(Na2S2O5)处理含铬酸性废水(含有
 ),利用氧化还原反应,将六价铬还原为三价铬,
),利用氧化还原反应,将六价铬还原为三价铬,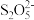 被氧化为
被氧化为 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为(4)已知: Na2S2O5溶于水会生成NaHSO3。检验Na2S2O5晶体在空气中已被氧化的实验方法是
您最近一年使用:0次



