(1)课本设计了如图一所示实验,其目的是通过比较H2O2的分解速率来比较______ ,可通过观察______ 来定性比较。有同学提出将CuSO4改为CuCl2更为合理,其理由是______ 。

(2)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是______ 的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是______
A.硫酸钾 B.硫酸锰 C.水 D.氯化锰

(2)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是
A.硫酸钾 B.硫酸锰 C.水 D.氯化锰
11-12高二上·黑龙江大庆·期末 查看更多[1]
(已下线)2010—2011学年黑龙江省大庆实验中学高二上学期期末考试化学试卷
更新时间:2016-12-09 01:34:49
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】实验
(1)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快。由此判断,影响化学反应速率的因素有___ 和___ 。
(2)锌与盐酸的反应速率可以通过观察___ 进行判断,也可通过实验测定锌与盐酸反应速率,除测量反应时间外,还需要测量的物理量是___ 或___ 。
(3)为探究锌与盐酸反应过程的速率变化,某同学的实验测定方法:在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(氢气体积已换算为标准状况下):
①反应速率最快的时间段是____ (填“0~1min”“1~2min”“2~3min”“3~4min”或“4~5min”)。
②试分析1~3min时间段里,反应速率变快的主要原因是____ 。
(1)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快。由此判断,影响化学反应速率的因素有
(2)锌与盐酸的反应速率可以通过观察
(3)为探究锌与盐酸反应过程的速率变化,某同学的实验测定方法:在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(氢气体积已换算为标准状况下):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 体积/mL | 50 | 120 | 232 | 290 | 310 |
②试分析1~3min时间段里,反应速率变快的主要原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】为比较 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
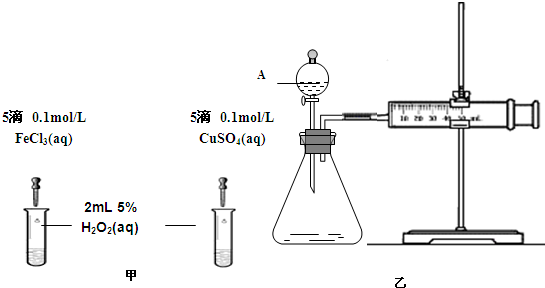
(1)定性分析:如图甲可通过观察_______ 的快慢,定性比较得出结论。有同学提出将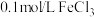 改为
改为_______  更为合理,其理由是
更为合理,其理由是_______ ;
(2)定量分析。如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是_______ ;
(3)查阅资料得知:将作为催化剂的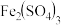 溶液加入
溶液加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,试从
均参加了反应,试从催化剂的角度 分析,这两个氧化还原反应的离子方程式分别是: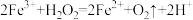 和
和_______ 。
II.欲用下图所示实验来证明 是
是 分解反应的催化剂。
分解反应的催化剂。
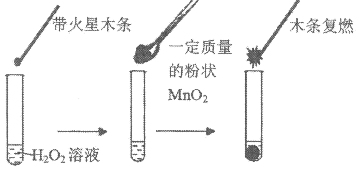
(1)该实验不能达到目的,若想证明 是催化剂还需要确认
是催化剂还需要确认_______ ;
(2)加入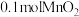 粉末于
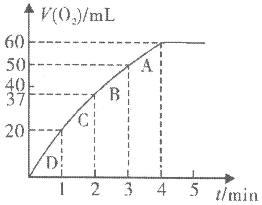
粉末于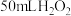 溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
①写出 在二氧化锰作用下发生反应的化学方程式
在二氧化锰作用下发生反应的化学方程式_______ ;
②A、B、C、D各点反应速率快慢的顺序为_______ >_______ >_______ >_______ 。
 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
(1)定性分析:如图甲可通过观察
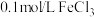 改为
改为 更为合理,其理由是
更为合理,其理由是(2)定量分析。如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是
(3)查阅资料得知:将作为催化剂的
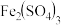 溶液加入
溶液加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,试从
均参加了反应,试从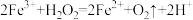 和
和II.欲用下图所示实验来证明
 是
是 分解反应的催化剂。
分解反应的催化剂。
(1)该实验不能达到目的,若想证明
 是催化剂还需要确认
是催化剂还需要确认(2)加入
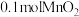 粉末于
粉末于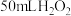 溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
①写出
 在二氧化锰作用下发生反应的化学方程式
在二氧化锰作用下发生反应的化学方程式②A、B、C、D各点反应速率快慢的顺序为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】对下列探究反应速率和化学平衡影响因素的四个实验,回答下列问题:
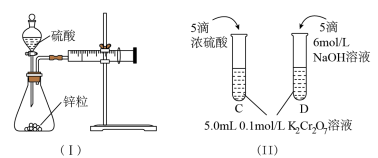
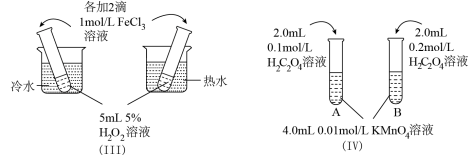
(1)利用实验(Ⅰ)探究锌与1mol/L硫酸和4mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(至少写出两项):______________________ 。
(2)实验(Ⅱ)已知:Cr2O72-(橙色)+ H2O 2CrO42-(黄色)+ 2H+。D试管中实验现象为
2CrO42-(黄色)+ 2H+。D试管中实验现象为______________ ,用平衡移动原理解释原因:_______________
(3)实验(Ⅲ)中实验目的是探究____________________ 。
(4)在室温下进行实验(Ⅳ)溶液褪色的时间:t(A)________ t(B)(填>、<或= )


(1)利用实验(Ⅰ)探究锌与1mol/L硫酸和4mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(至少写出两项):
(2)实验(Ⅱ)已知:Cr2O72-(橙色)+ H2O
 2CrO42-(黄色)+ 2H+。D试管中实验现象为
2CrO42-(黄色)+ 2H+。D试管中实验现象为(3)实验(Ⅲ)中实验目的是探究
(4)在室温下进行实验(Ⅳ)溶液褪色的时间:t(A)
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】取等体积、等物质的量浓度H2O2溶液分别进行下列实验,研究外界条件对反应速率的影响。
(1)实验1、2研究的是___________ 对H2O2分解速率的影响; 实验3、4研究的是________ 对H2O2分解速率的影响。
(2)实验中可以判断该反应速率快慢的现象是__________ 。
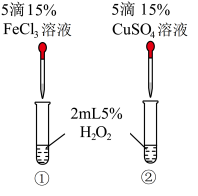
(3)有同学认为,若把实验3中的催化剂改成CuSO4进行下图操作,看到反应速率为①>②,则一定可以说明Fe3+比Cu2+对H2O2分解催化效果好。你认为此同学的结论是否正确?____ (填“正确”或“不正确”),理由是_____ 。
序号 | 条件 | |
温度/℃ | 催化剂 | |
1 | 40 | FeCl3溶液 |
2 | 20 | FeCl3溶液 |
3 | 20 | MnO2 |
4 | 20 | 无 |
(2)实验中可以判断该反应速率快慢的现象是
(3)有同学认为,若把实验3中的催化剂改成CuSO4进行下图操作,看到反应速率为①>②,则一定可以说明Fe3+比Cu2+对H2O2分解催化效果好。你认为此同学的结论是否正确?

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】研究化学反应中能量变化,能更好地利用化学反应为生产和生活服务。
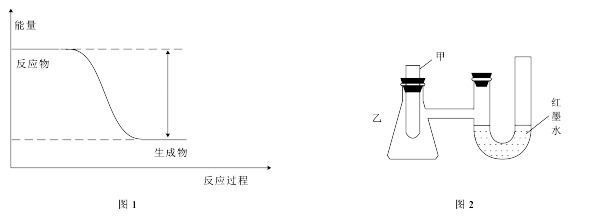
(1)反应Fe+H2SO4=FeSO4+H2↑的能量变化如图1所示。
①该反应为__________ (填“吸热”或“放热”)反应。
②为了探究化学能与热能的转化,某实验小组设计了图2实验装置,在甲试管里先加入适量铁片,再加入稀硫酸,U形管中可观察到的现象是__________ 。
③若要使该反应的反应速率加快,下列措施可行的是__________ (填字母)。
A.铁片改为铁粉B.稀硫酸改为98%的浓硫酸C.升高温度
(2)若将上述反应设计成原电池,装置如图3所示。
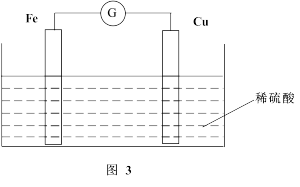
①铜为__________ (填“正”或“负”)极;负极的电极反应式为______ 。
②若该电池反应过程中共转移0.3 mol电子,则生成的H2在标准状况下的体积是__________ L。

(1)反应Fe+H2SO4=FeSO4+H2↑的能量变化如图1所示。
①该反应为
②为了探究化学能与热能的转化,某实验小组设计了图2实验装置,在甲试管里先加入适量铁片,再加入稀硫酸,U形管中可观察到的现象是
③若要使该反应的反应速率加快,下列措施可行的是
A.铁片改为铁粉B.稀硫酸改为98%的浓硫酸C.升高温度
(2)若将上述反应设计成原电池,装置如图3所示。

①铜为
②若该电池反应过程中共转移0.3 mol电子,则生成的H2在标准状况下的体积是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某学习小组对硝酸工业活性炭脱硝工艺进行探究。回答下列问题:
Ⅰ.硝酸工业产生的烟气中含有大量 ,工艺如图所示:
,工艺如图所示:
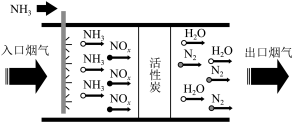
(1)该流程中活性炭是催化剂,加入催化剂的目的是___________ 。
(2)若要使 和
和 恰好充分反应。则反应混合物中
恰好充分反应。则反应混合物中 与
与 的体积比为
的体积比为___________ (用含x的式子表示)。
Ⅱ.某同学为了探究干燥条件下 与
与 的反应,设计如图所示实验装置进行实验。
的反应,设计如图所示实验装置进行实验。

(3)装置A为氨气的发生装置,应选用___________ (填“X”或“Y”)为此实验制备氨气的装置,相关反应的化学方程式为___________ 。
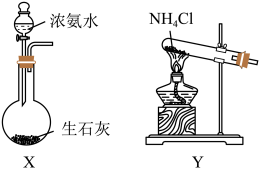
(4)该实验设计中存在缺陷,请写出解决方案:___________ 。
(5)装置D用于制备 气体。
气体。
①有同学推测反应过程中有可能产生NO,该同学做此推测的理由为___________ 。
②装置D中发生反应的实验现象为___________ 。
③ 能与碱液反应,故在拆装置之前,应该怎么操作
能与碱液反应,故在拆装置之前,应该怎么操作___________ 。
Ⅰ.硝酸工业产生的烟气中含有大量
 ,工艺如图所示:
,工艺如图所示:
(1)该流程中活性炭是催化剂,加入催化剂的目的是
(2)若要使
 和
和 恰好充分反应。则反应混合物中
恰好充分反应。则反应混合物中 与
与 的体积比为
的体积比为Ⅱ.某同学为了探究干燥条件下
 与
与 的反应,设计如图所示实验装置进行实验。
的反应,设计如图所示实验装置进行实验。
(3)装置A为氨气的发生装置,应选用

(4)该实验设计中存在缺陷,请写出解决方案:
(5)装置D用于制备
 气体。
气体。①有同学推测反应过程中有可能产生NO,该同学做此推测的理由为
②装置D中发生反应的实验现象为
③
 能与碱液反应,故在拆装置之前,应该怎么操作
能与碱液反应,故在拆装置之前,应该怎么操作
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B的键能。下表列出了一些化学键的键能(E):
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应_______ (填“吸收”或“放出”)_______ kJ能量(用含有a、b的关系式表示)。 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=_______ 。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为_______ 。
Ⅱ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(4)该实验探究的是_______ 因素对化学反应速率的影响。如下图一,相同时间内针筒中所得的CO2体积大小关系是_______ (填实验序号)。 =
=_______ (假设混合液体积为50mL)。
(6)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定_______ 来比较化学反应速率。
(7)小组同学发现反应速率总是如上图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②_______ 。
| 化学键 | H—H | Cl—Cl | O=O | C—Cl | C—H | O—H | H—Cl |
| E/(kJ·mol-1) | 436 | 247 | x | 330 | 413 | 463 | 431 |
(1)如图表示某反应的能量变化关系,则此反应
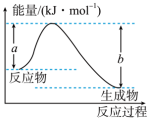
 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为
Ⅱ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.1 mol·L-1KMnO4溶液 |
| ② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.1mol·L-1KMnO4溶液 |
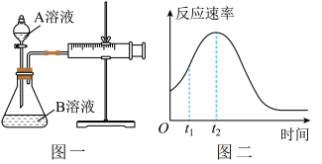
 =
=(6)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(7)小组同学发现反应速率总是如上图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】用块状碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如图所示,分析判断:(填“OE”、“EF”或“FG”,下同)___ 段化学反应速率最大,___ 段收集的二氧化碳气体最多。

(2)ag块状碳酸钙与足量盐酸反应,碳酸钙消耗的质量随时间的变化曲线用实线表示,在相同的条件下,将bg(a>b)粉末状碳酸钙与足量的相同浓度的盐酸反应,碳酸钙消耗的质量随时间的变化曲线用虚线表示。则图中最符合实际情况的图像是___ (填序号)。
A. B.
B. C.
C. D.
D.
(3)为了减缓题述反应的速率,下列措施中,你认为可行的是___ (填序号)
A.加入蒸馏水
B.加入氯化钠固体
C.加入硝酸钾溶液
D.加入浓盐酸
E.降温
F.加入MnO2粉末
(1)实验过程如图所示,分析判断:(填“OE”、“EF”或“FG”,下同)

(2)ag块状碳酸钙与足量盐酸反应,碳酸钙消耗的质量随时间的变化曲线用实线表示,在相同的条件下,将bg(a>b)粉末状碳酸钙与足量的相同浓度的盐酸反应,碳酸钙消耗的质量随时间的变化曲线用虚线表示。则图中最符合实际情况的图像是
A.
 B.
B. C.
C. D.
D.
(3)为了减缓题述反应的速率,下列措施中,你认为可行的是
A.加入蒸馏水
B.加入氯化钠固体
C.加入硝酸钾溶液
D.加入浓盐酸
E.降温
F.加入MnO2粉末
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)某探究小组用 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验
浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验 的用量为25.00mL,大理石用量为10.00g。请完成以下实验设计表:
的用量为25.00mL,大理石用量为10.00g。请完成以下实验设计表:
(2)化学反应的能量变化通常表现为热量的变化,因此反应热的研究对于化学学科发展具有重要意义。利用如图所示装置测定中和热的实验步骤如下:

步骤一:用量筒量取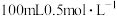 盐酸倒入小烧杯中,测出盐酸温度;
盐酸倒入小烧杯中,测出盐酸温度;
步骤二:用另一量筒量取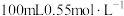 的氢氧化钠溶液,并用同一温度计测出其温度;
的氢氧化钠溶液,并用同一温度计测出其温度;
步骤三:将NaOH和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
①仪器a的作用是_______ ,烧杯间填满碎泡沫塑料的作用是_______ 。
②配制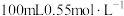 的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒、胶头滴管以及
的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒、胶头滴管以及_______ 。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是_______ 。
a.实验装置保温、隔热效果差
b.一次性把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定 溶液的温度
溶液的温度
(1)某探究小组用
 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验
浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验 的用量为25.00mL,大理石用量为10.00g。请完成以下实验设计表:
的用量为25.00mL,大理石用量为10.00g。请完成以下实验设计表:| 实验编号 | 温度(℃) | 大理石规格 |  浓度(mol/L) 浓度(mol/L) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响; (Ⅱ)实验①和③探究温度对反应速率的影响; (Ⅲ)实验①和④探究 |
| ② | 25 | 粗颗粒 | ||
| ③ | 粗颗粒 | 2.00 | ||
| ④ | 细颗粒 |

步骤一:用量筒量取
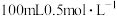 盐酸倒入小烧杯中,测出盐酸温度;
盐酸倒入小烧杯中,测出盐酸温度;步骤二:用另一量筒量取
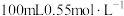 的氢氧化钠溶液,并用同一温度计测出其温度;
的氢氧化钠溶液,并用同一温度计测出其温度;步骤三:将NaOH和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
①仪器a的作用是
②配制
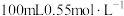 的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒、胶头滴管以及
的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒、胶头滴管以及③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.一次性把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定
 溶液的温度
溶液的温度
您最近一年使用:0次



