元素周期表的形式多种多样,如下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,下列说法正确的是
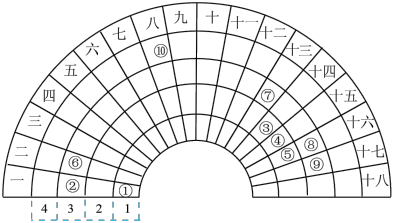

| A.②、⑧、⑨对应简单离子半径依次减小 |
| B.⑤的三种核素化学性质不同 |
| C.元素⑩处于常见周期表第四周期第VIIIB族 |
| D.④的最高价氧化物对应的水化物能与其氢化物反应,生成离子化合物 |
15-16高一下·山西朔州·期末 查看更多[5]
2015-2016学年山西省怀仁一中高一下期末化学试卷(已下线)第一章 原子结构与性质【过关测试提高卷】-2020-2021学年高二化学单元复习(新教材人教版选择性必修2)(已下线)【浙江新东方】高中化学20210304-014湖南省雅礼中学2022-2023学年高二上学期第三次月考化学试题河南省焦作市第一中学2022-2023学年高二下学期3月份教学质量检测 化学试题
更新时间:2016-07-22 16:41:48
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01 )的
)的 和原子半径、原子序数的关系如图所示。下列说法错误的是
和原子半径、原子序数的关系如图所示。下列说法错误的是

 )的
)的 和原子半径、原子序数的关系如图所示。下列说法错误的是
和原子半径、原子序数的关系如图所示。下列说法错误的是
A.电负性: |
| B.W和X形成的化合物XW3中含有离子键和共价键 |
C.简单氢化物的沸点: |
D.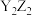 为非极性分子, 为非极性分子, 为极性分子,二者中的Y原子都是 为极性分子,二者中的Y原子都是 杂化 杂化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】几种短周期元素的原子半径和主要化合价见下表,下列有关说法中,正确的是
| 元素符号 | X | Y | Z | L | M | Q |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.066 |
| 主要化合价 | +2 | +3 | +6、-2 | +7、﹣1 | +4、﹣4 | -2 |
| A.离子半径大小:r(X2+)>r(Q2-) |
| B.Y与Q形成的化合物不能跟氢氧化钠溶液反应 |
| C.最高价氧化物的水化物的酸性:L>Z |
| D.Z的单质可在氧气中燃烧生成ZO3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
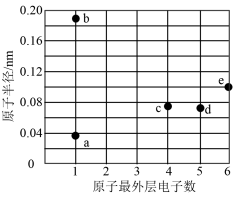
【推荐1】a、b、c、d、e、f 为六种短周期元素, a、b、e 、f 位于同一周期,c、d 也是同一周期, 且 d、e 同一主族,原子半径 d<e,a、b、c、d、f原子最外层电子依次增多,则下列说法中正确的是( )
| A.e 的非金属性比 f 强 |
| B.d 元素可能是第一周期元素 |
| C.六种元素中,a 元素最高价氧化物对应水化物碱性最强 |
| D.a、b、c、d 的原子序数逐渐增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列叙述与对应图式正确的是
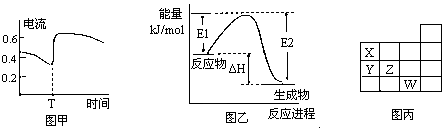

A.由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强
| ||||||||||||||||||||||||||
| B.图甲表示Zn—Cu原电池反应过程中的电流强度的变化。T时可能加入了H2O2 | ||||||||||||||||||||||||||
| C.图乙表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变 | ||||||||||||||||||||||||||
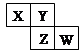
| D.图丙表示元素周期表的一部分,元素X、Y、Z、W中X的氢化物酸性最强 |
您最近一年使用:0次