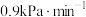在密闭容器中进行N2+3H2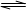 2NH3反应,起始时N2和H2分别为10mol和30mol,当达到平衡时N2的转化率为30%。若以NH3作为起始反应物,反应条件与上述反应相同时,要使其反应达到平衡时各组成成分的物质的量分数与前者相同,则NH3的起始物质的量和它的转化率正确的是( )
2NH3反应,起始时N2和H2分别为10mol和30mol,当达到平衡时N2的转化率为30%。若以NH3作为起始反应物,反应条件与上述反应相同时,要使其反应达到平衡时各组成成分的物质的量分数与前者相同,则NH3的起始物质的量和它的转化率正确的是( )
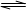 2NH3反应,起始时N2和H2分别为10mol和30mol,当达到平衡时N2的转化率为30%。若以NH3作为起始反应物,反应条件与上述反应相同时,要使其反应达到平衡时各组成成分的物质的量分数与前者相同,则NH3的起始物质的量和它的转化率正确的是( )
2NH3反应,起始时N2和H2分别为10mol和30mol,当达到平衡时N2的转化率为30%。若以NH3作为起始反应物,反应条件与上述反应相同时,要使其反应达到平衡时各组成成分的物质的量分数与前者相同,则NH3的起始物质的量和它的转化率正确的是( )| A.40mol、35% | B.20mol、30% | C.20mol、70% | D.10mol、50% |
11-12高二下·云南玉溪·期末 查看更多[5]
吉林省延边第二中学2018届高三上学期第三次月考化学试题2015-2016学年山东省东平一中高二下期6月月考化学试卷2015-2016学年河北大名县第一中学高二上学期第一次月考试化学试卷2015-2016学年河南省三门峡市陕州中学高二上学期入学考试化学试卷(已下线)2011-2012学年云南省玉溪一中高二下学期期末考试化学试卷
更新时间:2016-08-22 16:19:31
|
【知识点】 化学平衡
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列生产生活的实际应用中,不能用勒夏特列原理解释的是
| A.用饱和食盐水除去Cl2中的HCl |
| B.使用更有效的催化剂,提高可逆反应的转化率 |
| C.工业合成NH3是放热反应,为提高NH3的产率,理论上应采取低温的措施 |
D.工业生产硫酸的过程中,使用过量的空气,以提高二氧化硫的利用率(2SO2+O2  2SO3) 2SO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】CH4与CO2催化重整可以同时利用两种温室气体,其工艺过程中涉及如下反应:
反应I:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH1=247.4kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=41.2kJ·mol-1
反应Ⅲ:CH4(g)+ O2(g)⇌CO(g)+2H2(g) ΔH3=-35.6 kJ·mol-1
O2(g)⇌CO(g)+2H2(g) ΔH3=-35.6 kJ·mol-1
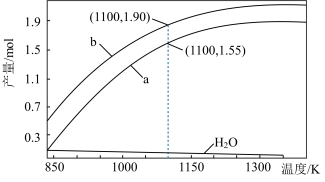
一定条件下,向体积为VL的密闭容器中通入CH4、CO2各1.0mol及少量O2,测得不同温度下反应平衡时各产物产量如图所示。下列说法正确的是
反应I:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH1=247.4kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2=41.2kJ·mol-1
反应Ⅲ:CH4(g)+
 O2(g)⇌CO(g)+2H2(g) ΔH3=-35.6 kJ·mol-1
O2(g)⇌CO(g)+2H2(g) ΔH3=-35.6 kJ·mol-1一定条件下,向体积为VL的密闭容器中通入CH4、CO2各1.0mol及少量O2,测得不同温度下反应平衡时各产物产量如图所示。下列说法正确的是

| A.图中曲线b表示H2的平衡产量随温度的变化曲线 |
B.1100K时,CH4与CO2的转化率分别为95%、90%,反应I的平衡常数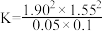 |
| C.反应CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH=206.2kJ·mol-1 |
| D.若选用其它催化剂可能使平衡时H2O的产量随着温度升高而增加 |
您最近一年使用:0次

 常用于检验样品中的微量水。一水硫酸铜失水的反应为
常用于检验样品中的微量水。一水硫酸铜失水的反应为
 。不同温度下,在体积为
。不同温度下,在体积为 的恒容密闭容器中加入足量的一水硫酸铜粉末,发生上述反应。测得蒸气压与温度、时间的关系如下表所示:
的恒容密闭容器中加入足量的一水硫酸铜粉末,发生上述反应。测得蒸气压与温度、时间的关系如下表所示:
 ,
,
 ℃,
℃, 内用
内用 的分压表示的反应速率为
的分压表示的反应速率为