在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) 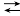 2NO2(g) △H,随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g) △H,随温度升高,混合气体的颜色变深。回答下列问题:
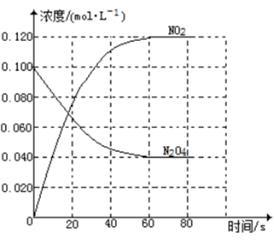
(1)反应的△H_______ 0(填“>”或“<”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(NO2)为______ mol·L-1·s-1,反应的平衡常数K为_________ 。
(2)100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。则T________ 100℃(填“大于”或“小于”)。
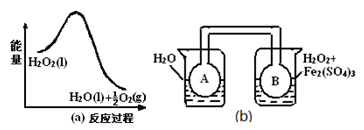
(3)利用图(a)和(b)中的信息,按图(b)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的__________ (填“深”或“浅”),其原因是_________ 。
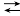 2NO2(g) △H,随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g) △H,随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的△H
(2)100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。则T

(3)利用图(a)和(b)中的信息,按图(b)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的
更新时间:2016-12-09 08:40:48
|
【知识点】 化学平衡
相似题推荐
填空题
|
较难
(0.4)
【推荐1】已知:
又已知不同温度下, 、
、 的值如下:
的值如下:
(1)若 时进行反应①,
时进行反应①, 的起始浓度为
的起始浓度为 ,
, 后建立平衡,则
后建立平衡,则 的转化率为
的转化率为__________ ,用 表示的反应速率为
表示的反应速率为__________ 。
(2) 进行反应③,其平衡常数为
进行反应③,其平衡常数为 为
为__________ (求具体数值),焓变
__________ (填“>”“=”或“<”)0,若已知该反应仅在高温时正反应自发,则
__________ (填“>”“=”或“<”)0。
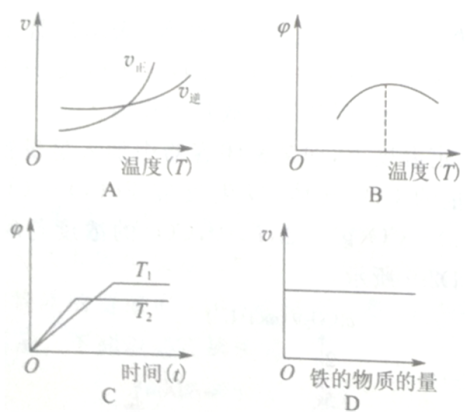
(3)下列图象符合反应②的是__________ (填序号)。(图中v是速率, 为混合物中
为混合物中 的体积分数)
的体积分数)
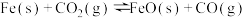 |  | ① |
 |  | ② |
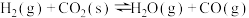 |  | ③ |
 、
、 的值如下:
的值如下:| 温度/℃ |  |  |
| 500 |  |  |
| 700 | 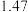 | 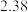 |
| 900 | 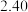 | 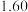 |
 时进行反应①,
时进行反应①, 的起始浓度为
的起始浓度为 ,
, 后建立平衡,则
后建立平衡,则 的转化率为
的转化率为 表示的反应速率为
表示的反应速率为(2)
 进行反应③,其平衡常数为
进行反应③,其平衡常数为 为
为

(3)下列图象符合反应②的是
 为混合物中
为混合物中 的体积分数)
的体积分数)
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】向2.0L恒容密闭容器中充入1.0mol PCl5,在温度为T时发生如下反应PCl5(g)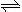 PCl3(g)+ Cl2(g)△H=" +124" kJ•mol-1。反应过程中测定的部分数据见下表:
PCl3(g)+ Cl2(g)△H=" +124" kJ•mol-1。反应过程中测定的部分数据见下表:

回答下列问题:
(1)反应在前50s的平均速率v(PCl5)=__________ ,该反应的△S___ 0(填“<”、“>”或“=”).
(2)温度为T时,该反应的化学平衡常数=_____________ 。
(3)上述反应到达平衡状态时,PCl3的体积分数为________ 。
要提高平衡时PCl3的体积分数,可采取的措施有_____________ 。
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a=___________ 。
(5)在热水中,五氯化磷完全水解,生成磷酸(H3PO4),该反应的化学方程式是____________________ 。
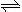 PCl3(g)+ Cl2(g)△H=" +124" kJ•mol-1。反应过程中测定的部分数据见下表:
PCl3(g)+ Cl2(g)△H=" +124" kJ•mol-1。反应过程中测定的部分数据见下表:
回答下列问题:
(1)反应在前50s的平均速率v(PCl5)=
(2)温度为T时,该反应的化学平衡常数=
(3)上述反应到达平衡状态时,PCl3的体积分数为
要提高平衡时PCl3的体积分数,可采取的措施有
| A.温度不变,压缩容器体积增大压强 | B.使用高效催化剂 |
| C.温度和体积不变,减小PCl5的起始量 | D.体积不变,提高反应温度 |
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a=
(5)在热水中,五氯化磷完全水解,生成磷酸(H3PO4),该反应的化学方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机。
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇(CH3OH)蒸汽和水蒸气CO2(g)+3H2(g) CH3OH(g)+H2O(g)。下图表示恒压容器中充入1mol CO2和3 mol H2,转化率达50%时的能量变化示意图。写出该反应的热化学方程式:
CH3OH(g)+H2O(g)。下图表示恒压容器中充入1mol CO2和3 mol H2,转化率达50%时的能量变化示意图。写出该反应的热化学方程式:______________________________________ 。

(2)另外工业上还可用CO和H2制备甲醇。 反应为CO(g)+2H2(g) CH3OH(g),
CH3OH(g),
某温度下,在容积为2L的恒容密闭容器中进行该反应,其相关数据见下图:
① t min至2t min时速率变化的原因可能是______________________________ ;
② 3t min时对反应体系采取了一个措施,至4t min时CO的物质的量为0.5mol,请完成上图CO的曲线。___________________
(3)CO2在一定条件下,还可以与H2合成二甲醚:
2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)。
CH3OCH3(g)+3H2O(g)。
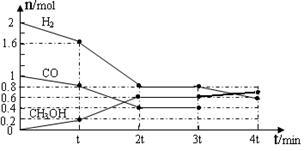
将2.5 mol H2与b mol CO2置于容积为1 L的密闭容器中,发生上述反应,达到平衡状态时,测得实验数据如下表:
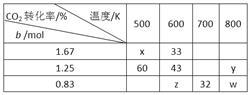
① 降温时,上述平衡向_________ 方向移动(填“正反应”或“逆反应”)。
②表中x、y的大小关系为_________ 。
③表中x、y、z、w对应的平衡常数分别为Kx、Ky、Kz、Kw,它们之间的大小关系为___________________ 。
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇(CH3OH)蒸汽和水蒸气CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。下图表示恒压容器中充入1mol CO2和3 mol H2,转化率达50%时的能量变化示意图。写出该反应的热化学方程式:
CH3OH(g)+H2O(g)。下图表示恒压容器中充入1mol CO2和3 mol H2,转化率达50%时的能量变化示意图。写出该反应的热化学方程式:
(2)另外工业上还可用CO和H2制备甲醇。 反应为CO(g)+2H2(g)
 CH3OH(g),
CH3OH(g),某温度下,在容积为2L的恒容密闭容器中进行该反应,其相关数据见下图:

① t min至2t min时速率变化的原因可能是
② 3t min时对反应体系采取了一个措施,至4t min时CO的物质的量为0.5mol,请完成上图CO的曲线。
(3)CO2在一定条件下,还可以与H2合成二甲醚:
2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g)。
CH3OCH3(g)+3H2O(g)。将2.5 mol H2与b mol CO2置于容积为1 L的密闭容器中,发生上述反应,达到平衡状态时,测得实验数据如下表:

① 降温时,上述平衡向
②表中x、y的大小关系为
| A.x=y | B.x>y | C.x<y | D.无法判断 |
③表中x、y、z、w对应的平衡常数分别为Kx、Ky、Kz、Kw,它们之间的大小关系为
您最近一年使用:0次



