已知水在25℃和95℃时,其电离平衡曲线如图所示,下列说法错误的是
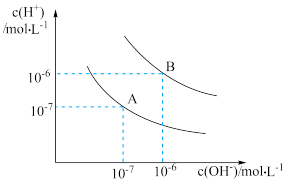

| A.95℃时,pH=4的H2SO4溶液中,由水电离出的c(OH-)=1×10-10mol/L |
| B.15℃时,pH=7的溶液呈酸性 |
| C.AB连线上的点均表示中性溶液 |
| D.B点对应的温度高于A点对应的温度 |
更新时间:2016-11-15 16:12:44
|
【知识点】 水溶液中水的电离程度及的计算解读
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,下列指定溶液中一定能大量共存的是
A.水电离出来的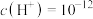 mol/L的溶液中: mol/L的溶液中: 、 、 、 、 、 、 |
B.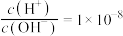 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.澄清透明溶液中: 、 、 、 、 、 、 |
D.与Al反应能放出 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,某浓度的NaHSO4溶液pH=2,对于该溶液,下列叙述中不正确的是
| A.该NaHSO4溶液的物质的量浓度为0.01 mol/L |
| B.水电离出的c(H+)=1×10-2 mol/L |
| C.c(H+)=c(OH-)+c(SO42—) |
| D.该温度下加入等体积pH=12的NaOH溶液,反应后溶液恰好呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】25℃时CH3COOH的 、HF的
、HF的 ,下列说法正确的是
,下列说法正确的是
 、HF的
、HF的 ,下列说法正确的是
,下列说法正确的是A.分别测定某HF溶液、醋酸溶液的pH,前者小于后者,可以证明HF的 |
B.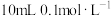 的HF溶液中加入 的HF溶液中加入 的NaOH溶液,溶液中水的电离程度与纯水相同,V(NaOH)可能小于或大于10mL 的NaOH溶液,溶液中水的电离程度与纯水相同,V(NaOH)可能小于或大于10mL |
C.向 的HF溶液中加入 的HF溶液中加入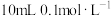 的NaOH溶液充分反应,所得溶液中 的NaOH溶液充分反应,所得溶液中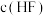  |
D.将 的HF溶液与 的HF溶液与 的醋酸混合,HF的电离度增大 的醋酸混合,HF的电离度增大 |
您最近一年使用:0次



