CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
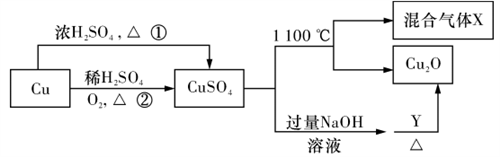

| A.相对于途径①,途径②更好地体现了绿色化学思想 |
| B.Y可以是葡萄糖溶液 |
| C.CuSO4在1100℃分解所得气体X是SO2和SO3的混合气体 |
| D.将CuSO4溶液蒸发浓缩、冷却结晶可制得胆矾晶体 |
更新时间:2016-11-17 09:33:49
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】将6.4g铜投入30mL一定浓度的硝酸中,恰好完全反应,产生标准状况下的NO和NO2混合气体共2.24L。则下列叙述正确的是
| A.NO体积为0.56L | B.原硝酸浓度10.0mol/L |
| C.反应中失去电子数0.2mol | D.体现酸性的硝酸为0.1mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体2.24L(标准状况),这些气体与一定体积O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入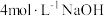 溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL,下列说法正确的是
溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL,下列说法正确的是
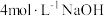 溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL,下列说法正确的是
溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL,下列说法正确的是| A.参加反应的硝酸是0.2mol |
| B.消耗氧气的体积为1.68L(标准状况) |
| C.此反应过程中转移的电子为0.3mol |
D.混合气体中含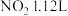 (标准状况) (标准状况) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法正确的是
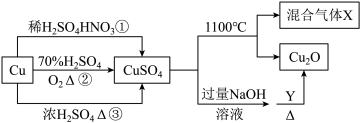

| A.途径①、②和③都体现了硫酸的酸性和氧化性 |
| B.Y可以是甲醛溶液 |
| C.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D.将CuSO4溶液蒸发浓缩、冷却结晶,因Cu2+水解得不到胆矾晶体 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】向2mL0.2mol/LCuSO4溶液中滴加0.2mol/LNa2SO3溶液时溶液变绿,继续滴加产生棕黄色沉淀,经检验棕黄色沉淀中不含 。通过实验探究棕黄色沉淀的成分。
。通过实验探究棕黄色沉淀的成分。
实验1:向棕黄色沉淀中加入稀硫酸,观察到溶液变蓝,产生红色固体
实验2: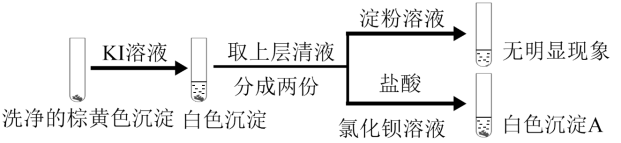
已知: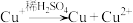 ,
,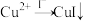 (白色)
(白色)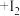 。
。
下列同学对实验现象的分析正确的是
 。通过实验探究棕黄色沉淀的成分。
。通过实验探究棕黄色沉淀的成分。实验1:向棕黄色沉淀中加入稀硫酸,观察到溶液变蓝,产生红色固体
实验2:

已知:
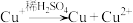 ,
,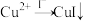 (白色)
(白色)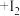 。
。下列同学对实验现象的分析正确的是
A.实验1中加入稀 后溶液变蓝可证实棕黄色沉淀中含有 后溶液变蓝可证实棕黄色沉淀中含有 |
B.实验2中加入KI溶液后产生白色沉淀,可证实棕黄色沉淀中含有 |
C.实验2中加入淀粉溶液后无明显现象,说明不存在 |
D.在 的存在下, 的存在下, 与 与 发生了氧化还原反应,产生CuI沉淀和 发生了氧化还原反应,产生CuI沉淀和 ,说明棕黄色沉淀中含有 ,说明棕黄色沉淀中含有 和 和 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】氯化亚铜(CuC1)广泛应用于化工、印染、电镀等行业。CuC1难溶于水,可溶于氯离子浓度较大的体系,易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,生产CuC1的工艺如下:
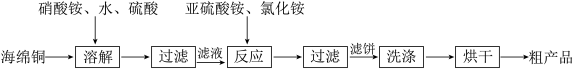
下列说法错误的是

下列说法错误的是
A.“溶解”过程发生氧化还原反应的离子方程式是3Cu+8H++2 =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
B.“反应”过程发生反应的离子方程式是2Cu2++ +2C1-+H2O=2CuC1↓+ +2C1-+H2O=2CuC1↓+ +2H+ +2H+ |
| C.“溶解”过程中硫酸可用浓盐酸代替 |
| D.“烘干”需在隔绝空气的环境中进行 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】利用某钒废渣(主要成分为 以及铁、铝、硅的氧化物)制备
以及铁、铝、硅的氧化物)制备 的工艺流程如下:
的工艺流程如下:
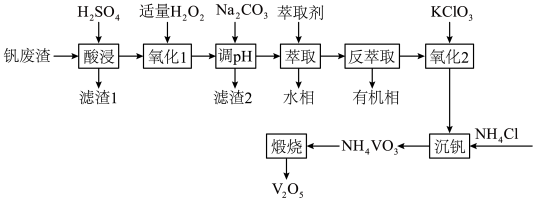
已知:Ⅰ. 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;
Ⅱ.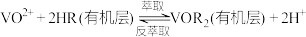 ;
;
Ⅲ.溶液中 与
与 可相互转化:
可相互转化: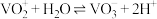 。
。
下列说法错误的是
 以及铁、铝、硅的氧化物)制备
以及铁、铝、硅的氧化物)制备 的工艺流程如下:
的工艺流程如下:
已知:Ⅰ.
 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;Ⅱ.
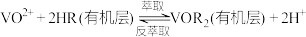 ;
;Ⅲ.溶液中
 与
与 可相互转化:
可相互转化: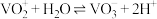 。
。下列说法错误的是
| A.“氧化1”中,可通过搅拌、加热加快转化速率 |
B.“滤渣2”的主要成分为 和 和 |
| C.有机萃取剂可循环使用 |
D.“沉钒”时还需通 调节溶液的酸碱性 调节溶液的酸碱性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列关于下列元素及其化合物的说法正确的是
| A.将等物质的量的①Na②Na2O③Na2O2④NaOH⑤Na2CO3露置于空气中,最后质量变化由小到大的顺序⑤<④<③<①<② |
| B.Na、Al、Cu可以分别用电解冶炼法、热还原法和热分解法得到 |
| C.将澄清石灰水分别加入Na2CO3和NaHCO3溶液中,前者产生沉淀,后者无明显现象 |
| D.在反应4FeCl2+4 Na2O2+6H2O=4 Fe(OH)3+O2↑+8NaCl中,做氧化剂的过氧化钠和做还原剂的过氧化钠物质的量之比为1:3 |
您最近一年使用:0次


 、SiO
、SiO


