T℃时,体积均为0.5 L的两个恒容密闭容器中发生可逆反应:2A(g)+B(g)  2C(g) △H=-Q kJ/mol(Q>0)。保持温度不变,实验测得起始和平衡时的有关数据如下表:
2C(g) △H=-Q kJ/mol(Q>0)。保持温度不变,实验测得起始和平衡时的有关数据如下表:
下列叙述中正确的是( )
 2C(g) △H=-Q kJ/mol(Q>0)。保持温度不变,实验测得起始和平衡时的有关数据如下表:
2C(g) △H=-Q kJ/mol(Q>0)。保持温度不变,实验测得起始和平衡时的有关数据如下表:容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
A | B | C | ||
① | 2 | 1 | 0 | 放热 0.75 Q kJ |
② | 0.4 | 0.2 | 1.6 | |
| A.容器①、②中反应的平衡常数均为4 |
| B.容器②中达到平衡时放出的热量为0.05Q kJ |
| C.向容器①中通入氦气,平衡时A的转化率不变 |
| D.其他条件不变,若容器②保持恒容绝热,则达到平衡时C的体积分数小于2/3 |
更新时间:2016-12-09 17:25:39
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】已知下列两个热化学方程式:2H2(g) + O2(g) = 2H2O(1) ΔH= -571.6 kJ•mol-1,C3H8(g) + 5O2(g)= 3CO2(g) + 4H2O(l) ΔH= -2220 kJ•mol-1,下列说法正确的是
| A.C3H8的热值比H2高 |
| B.C3H8 完全燃烧生成1mol H2O(g)放出的热量为555 kJ |
| C.l mol H2和2 molC3H8 组成的混合气体完全燃烧放出的热量为4725.8 kJ |
| D.氢气作为新能源具有热值高,无污染、资源丰富等优点,但不可再生。 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知1mol白磷完全转化为红磷放出29.2kJ热量,且P4(白,s)+5O2(g)=2P2O5(s)放出热量为Q1,4P(红,s)+5O2(g)=2P2O5(s)放出的热量为Q2,则Q1和Q2的关系为
| A.Q1>Q2 | B.Q12 | C.Q1=Q2 | D.无法判断 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】用CH4催化还原NOx,可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol-1
下列说法不正确的是( )
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol-1
下列说法不正确的是( )
| A.若用标况下4.48LCH4还原NO2生成N2和水蒸气,放出的热量为173.4kJ |
| B.由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l)ΔH<-574kJ·mol-1 |
| C.反应①②转移的电子数不同 |
| D.反应①②均为放热反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】一定条件下存在反应:2SO2(g)+O2(g) 2SO3(g),其正反应放热。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
2SO3(g),其正反应放热。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
 2SO3(g),其正反应放热。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
2SO3(g),其正反应放热。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是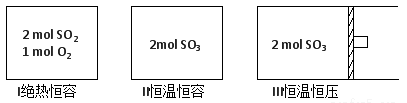
| A.容器I、Ⅲ中平衡常数相同 |
| B.容器II、Ⅲ中正反应速率相同 |
| C.容器Ⅱ、Ⅲ中的反应达平衡时,SO3的体积分数:II 〈 III |
| D.容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知2SO2(g)+O2(g) 2SO3(g) ΔH =-197kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲)2molSO2和1molO2;(乙)1molSO2和0.5molO2;(丙)2molSO3和1molO2。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3(g) ΔH =-197kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲)2molSO2和1molO2;(乙)1molSO2和0.5molO2;(丙)2molSO3和1molO2。恒温、恒容下反应达平衡时,下列关系一定正确的是
 2SO3(g) ΔH =-197kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲)2molSO2和1molO2;(乙)1molSO2和0.5molO2;(丙)2molSO3和1molO2。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3(g) ΔH =-197kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲)2molSO2和1molO2;(乙)1molSO2和0.5molO2;(丙)2molSO3和1molO2。恒温、恒容下反应达平衡时,下列关系一定正确的是| A.容器内压强P:P丙>P甲=2P乙 |
| B.气体的总物质的量n:n丙>n甲>n乙 |
| C.SO3的体积分数∮:∮甲=∮丙>∮乙 |
| D.反应热量的数值Q:197>Q丙>Q甲>Q乙 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g) xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
 xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )| A.平衡时甲中A的体积分数为0.4 |
| B.平衡时甲、乙两容器中A、B的物质的量之比不相等 |
| C.若平衡时两容器中的压强不相等,则两容器中压强之比为8:5 |
| D.若平衡时甲、乙两容器中A的物质的量相等,则x=4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某温度下, 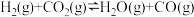 的平衡常数
的平衡常数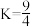 。该温度下,在①、②两个恒容容器中投入
。该温度下,在①、②两个恒容容器中投入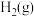 和
和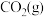 ,起始浓度如下表所示。下列判断不正确的是
,起始浓度如下表所示。下列判断不正确的是
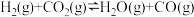 的平衡常数
的平衡常数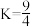 。该温度下,在①、②两个恒容容器中投入
。该温度下,在①、②两个恒容容器中投入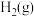 和
和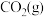 ,起始浓度如下表所示。下列判断不正确的是
,起始浓度如下表所示。下列判断不正确的是| 容器编号 | 起始浓度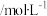 | |
 | 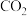 | |
| ① | 0.1 | 0.1 |
| ② | 0.2 | 0.1 |
| A.反应开始时,反应速率:②>① |
B.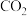 的平衡转化率:②>① 的平衡转化率:②>① |
C.平衡时,①中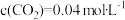 |
D.①中 的平衡转化率为40% 的平衡转化率为40% |
您最近一年使用:0次
【推荐2】一定温度下,向四个体积不等的恒容密闭容器中(a<b<c<d)分别通入2 mol NOCl(g),发生如下反应:2NOCl(g) 2NO(g)+Cl2(g)。t min时,四个容器中NOCl的转化率如图中A、B、C、D所示。下列叙述正确的是
2NO(g)+Cl2(g)。t min时,四个容器中NOCl的转化率如图中A、B、C、D所示。下列叙述正确的是

 2NO(g)+Cl2(g)。t min时,四个容器中NOCl的转化率如图中A、B、C、D所示。下列叙述正确的是
2NO(g)+Cl2(g)。t min时,四个容器中NOCl的转化率如图中A、B、C、D所示。下列叙述正确的是
| A.若延长A点反应时间,一定能提高NOCl转化率 |
| B.C、D两点的压强之比为28:25 |
| C.若体积为b L的容器中t min时达到平衡,再通入1mol NOCl和1mol NO,平衡不发生移动 |
| D.当四个容器中反应都达到平衡状态时,体积为c L的容器中NOCl的转化率最高 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】在温度相同、容积均为2L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下。
已知N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.4kJ·mol-1。下列说法正确的是
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molN2、3molH2 | 2molN2、6molH2 | 2molNH3 |
| NH3的浓度/mol·L-1 | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1kJ | 放出Q2kJ | 吸收Q3kJ |
| 体系压强/Pa | P1 | P2 | P3 |
| 反应物转化率 | α1 | α2 | α3 |
| A.2p1=2p3<p2 |
| B.达到平衡时丙容器中NH3的体积分数最大 |
| C.α2+α3>1 |
| D.Q1+Q3<92.4 |
您最近一年使用:0次



