下列说法中正确的是
①活化分子间的碰撞一定能发生化学反应 ②普通分子间的碰撞有时也能发生化学反应 ③增大反应物浓度,可增大活化分子百分数,从而使有效碰撞次数增多 ④有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大 ⑤化学反应的实质是旧化学键断裂和新化学键形成的过程 ⑥催化剂能增大活化分子百分数,从而成千成万倍地增大化学反应速率
①活化分子间的碰撞一定能发生化学反应 ②普通分子间的碰撞有时也能发生化学反应 ③增大反应物浓度,可增大活化分子百分数,从而使有效碰撞次数增多 ④有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大 ⑤化学反应的实质是旧化学键断裂和新化学键形成的过程 ⑥催化剂能增大活化分子百分数,从而成千成万倍地增大化学反应速率
| A.①⑤⑥ | B.②③⑤ | C.⑤⑥ | D.①⑤ |
更新时间:2016-12-09 17:27:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】纯净的碳酸钙与稀盐酸反应,不同时间收集到CO2的量如图所示。下列分析不合理的是
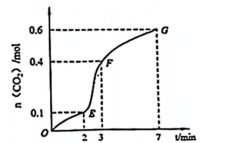

| A.EF段反应速率最快 |
| B.FG段生成的CO2最多 |
| C.用CO2物质的量变化表示OE段的反应速率为0.05mol/min |
| D.为降低该反应速率,可向稀盐酸中加入适量的NaCl溶液 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】汽车尾气里的 和
和 都是有害物质,有人提出通过以下反应来处理尾气:
都是有害物质,有人提出通过以下反应来处理尾气: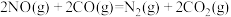 。对上述反应,下列说法正确的是
。对上述反应,下列说法正确的是
 和
和 都是有害物质,有人提出通过以下反应来处理尾气:
都是有害物质,有人提出通过以下反应来处理尾气: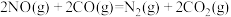 。对上述反应,下列说法正确的是
。对上述反应,下列说法正确的是| A.使用催化剂能改变反应速率 |
| B.改变压强(改变容器体积)对反应速率没有影响 |
| C.升高温度,反应速率降低 |
| D.无论外界条件怎样改变,均对此化学反应的速率无影响 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于可逆反应2SO2(g) + O2(g)  2SO3 (g) △H< 0 的说法中正确的是
2SO3 (g) △H< 0 的说法中正确的是
 2SO3 (g) △H< 0 的说法中正确的是
2SO3 (g) △H< 0 的说法中正确的是| A.活化分子之间的碰撞一定是有效碰撞 |
| B.增大反应物的浓度,可使单位体积内活化分子百分数增多,反应速率加快 |
| C.升高反应体系温度,可使单位体积内活化分子增多,反应速率加快 |
| D.催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加,反应速率加快 |
您最近半年使用:0次
单选题
|
适中
(0.65)
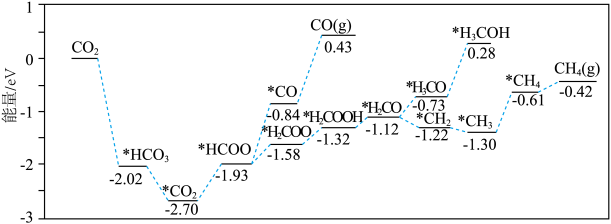
【推荐2】我国某科研团队开发催化剂用于光热催化 加氢制
加氢制 。其反应历程如图所示(*表示吸附在催化剂表面)。
。其反应历程如图所示(*表示吸附在催化剂表面)。 的选择性等于
的选择性等于 的物质的量与
的物质的量与 转化的物质的量之比。下列叙述正确的是
转化的物质的量之比。下列叙述正确的是
 加氢制
加氢制 。其反应历程如图所示(*表示吸附在催化剂表面)。
。其反应历程如图所示(*表示吸附在催化剂表面)。 的选择性等于
的选择性等于 的物质的量与
的物质的量与 转化的物质的量之比。下列叙述正确的是
转化的物质的量之比。下列叙述正确的是
A.在 历程中能垒最大为 历程中能垒最大为 |
B.该反应历程中, 的选择性为100% 的选择性为100% |
C.催化剂表面上 、CO脱附都会放出能量 、CO脱附都会放出能量 |
| D.反应历程中有极性键的断裂与形成 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知完全分解1molH2O2放出热量为98kJ,在含有少量I-的溶液中H2O2分解的机理为
反应Ⅰ:H2O2(aq)+I-(aq) IO-(aq)+H2O(l) △H1
IO-(aq)+H2O(l) △H1
反应Ⅱ:H2O2(aq)+IO-(aq) O2(g)+I-(aq)+H2O(l) △H2
O2(g)+I-(aq)+H2O(l) △H2
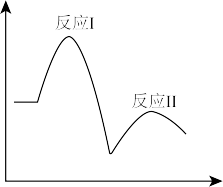
在一定温度下,其反应过程能量变化如图所示,下列有关该反应的说法不正确的是
反应Ⅰ:H2O2(aq)+I-(aq)
 IO-(aq)+H2O(l) △H1
IO-(aq)+H2O(l) △H1反应Ⅱ:H2O2(aq)+IO-(aq)
 O2(g)+I-(aq)+H2O(l) △H2
O2(g)+I-(aq)+H2O(l) △H2在一定温度下,其反应过程能量变化如图所示,下列有关该反应的说法不正确的是

| A.反应Ⅱ高温下能自发进行 |
| B.H2O2分解产生氧气的速率是由反应I决定的 |
| C.I-、IO-都是催化剂 |
| D.△H1+△H2=-196kJ•mol-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】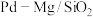 催化剂上
催化剂上 甲烷化反应机理如图所示,下列说法不正确的是
甲烷化反应机理如图所示,下列说法不正确的是
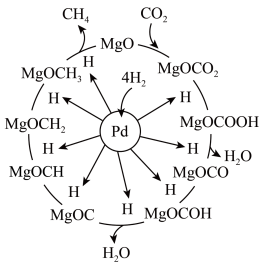
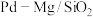 催化剂上
催化剂上 甲烷化反应机理如图所示,下列说法不正确的是
甲烷化反应机理如图所示,下列说法不正确的是
A.增大 的浓度,能增大活化分子百分含量,加快反应速率 的浓度,能增大活化分子百分含量,加快反应速率 |
B.整个甲烷化过程真正起催化作用的物质为 和MgO 和MgO |
C.上述甲烷化过程总反应可表示为 |
D.经过一个加氢循环后MgO再次与 结合形成碳酸盐,继续一个新的加氢循环 结合形成碳酸盐,继续一个新的加氢循环 |
您最近半年使用:0次




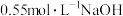 溶液分别与等体积、等浓度的
溶液分别与等体积、等浓度的 溶液、盐酸反应,测得反应热依次为
溶液、盐酸反应,测得反应热依次为 、
、 ,
,
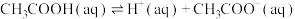

 溶液,产生气体的速率加快
溶液,产生气体的速率加快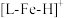 表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:下列说法错误的是
表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:下列说法错误的是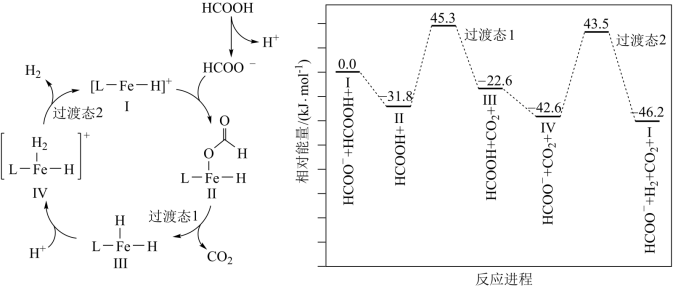

 浓度过大或者过小,均导致反应速率降低
浓度过大或者过小,均导致反应速率降低

