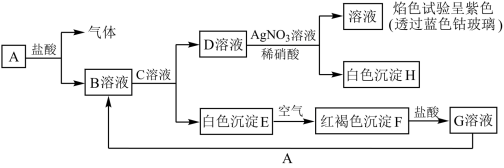
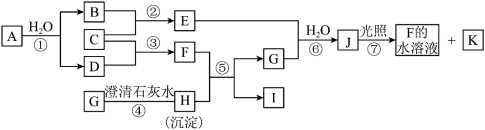
现有金属单质A和气体甲、乙、丙及物质B、C、D、E、F、G,它们之间能发生如下反应,其中乙是黄绿色气体(图中有些反应的产物和反应的条件没有全部标出)。
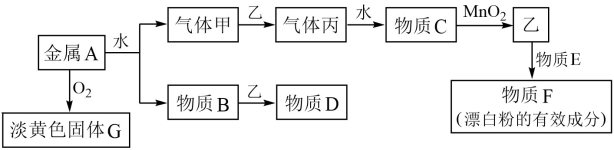
请根据以上信息回答下列问题:
(1)写出下列物质的名称:丙-_______________ ;
(2)写出下列物质的化学式:F________________ ;
(3)气体乙是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请你根据所学
知识回答下列问题:
① 把气体乙通入紫色石蕊溶液中,可以观察到的现象是:__________ ,请你解释其中的原因__________________ 。
② 某化学兴趣小组计划用气体乙和物质B制取简易消毒液D。其反应原理为:(用化学方程式
表示)______________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的名称:丙-
(2)写出下列物质的化学式:F
(3)气体乙是一种重要的化工原料,在工农业生产、生活中有着重要的应用。请你根据所学
知识回答下列问题:
① 把气体乙通入紫色石蕊溶液中,可以观察到的现象是:
② 某化学兴趣小组计划用气体乙和物质B制取简易消毒液D。其反应原理为:(用化学方程式
表示)
更新时间:2016-12-09 17:30:39
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知A~H均为中学化学常见的物质,转化关系如下图。其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、F、G、H的焰色反应均为黄色,E为两性化合物。

(1)写出C与水反应的离子方程式_____________________________________ ,假设温度不变,该反应会使水的电离程度________ (填写“变大”“变小”“不变”)
(2)B的水溶液呈_________ 性,用离子方程式解释原因______________
(3)将A~H中易溶于水的化合物溶于水,会抑制水的电离的是____________ (填序号)
(4)常温下,pH均为10的D、F溶液中,水电离出的c(OH-)之比为___________________ 向D的稀溶液中通入CO2至溶液呈中性,所得溶液中离子物质的量浓度由大到小的顺序为:_______________

(1)写出C与水反应的离子方程式
(2)B的水溶液呈
(3)将A~H中易溶于水的化合物溶于水,会抑制水的电离的是
(4)常温下,pH均为10的D、F溶液中,水电离出的c(OH-)之比为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下图为一些常见物质的转化关系图(部分反应物与生成物未标出)。A、C、E、G为单质,其中A、C、G为金属,E为气体。B为常见无色液体,L为红褐色固体,I的焰色反应呈紫色。常温下A、G投入J的浓溶液无明显现象,K是反应①所得溶液中的唯一溶质。
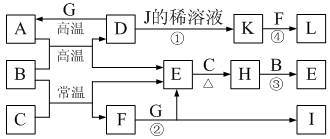
⑴A在元素周期表中的位置为_______ ,H的电子式为________ 。
⑵写出有关反应的离子方程式:
反应①的离子方程式为__________ 。
反应②的离子方程式为__________ 。
⑶反应③中每生成1 mol E,转移电子的物质的量为__________ 。

⑴A在元素周期表中的位置为
⑵写出有关反应的离子方程式:
反应①的离子方程式为
反应②的离子方程式为
⑶反应③中每生成1 mol E,转移电子的物质的量为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】印刷铜制电路板蚀刻液的选取和回收再利用一直是研究的热点。常用的蚀刻液主要有传统的FeCl3型(HCl–FeCl3)、酸性的过氧化氢型(HCl-H2O2)等。
I.某兴趣小组模拟FeCl3型蚀刻液的蚀刻过程,并回收Cu和蚀刻液(FeCl3溶液)的流程如图所示:
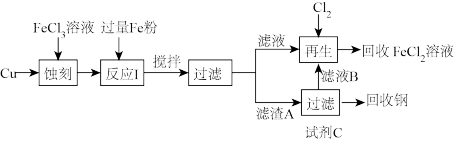
回答下列问题:
(1)“蚀刻”时发生反应的化学方程式为_______ 。
(2)“滤渣A”的成分为_______ ,“试剂C”是_______ (填写名称)。
(3)“滤液B”与氯气“再生”时发生反应的离子方程式为_______ 。
Ⅱ.应用酸性过氧化氢型(HCl-H2O2)蚀刻液,产生的蚀刻废液处理方法如图所示:
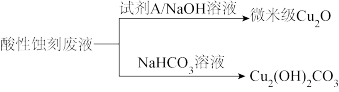
(4)用酸性过氧化氢型蚀刻液蚀刻铜板主要反应的离子方程式为_______ 。
(5)试剂A可以选择葡萄糖,获得微米级Cu2O的反应中利用了葡萄糖的_______ 性。
(6)回收Cu2(OH)2CO3的过程中需控制反应的温度,当温度高于80℃时,产品颜色发暗,其原因可能是_______ 。
I.某兴趣小组模拟FeCl3型蚀刻液的蚀刻过程,并回收Cu和蚀刻液(FeCl3溶液)的流程如图所示:

回答下列问题:
(1)“蚀刻”时发生反应的化学方程式为
(2)“滤渣A”的成分为
(3)“滤液B”与氯气“再生”时发生反应的离子方程式为
Ⅱ.应用酸性过氧化氢型(HCl-H2O2)蚀刻液,产生的蚀刻废液处理方法如图所示:
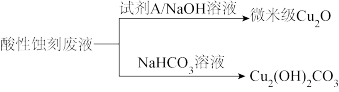
(4)用酸性过氧化氢型蚀刻液蚀刻铜板主要反应的离子方程式为
(5)试剂A可以选择葡萄糖,获得微米级Cu2O的反应中利用了葡萄糖的
(6)回收Cu2(OH)2CO3的过程中需控制反应的温度,当温度高于80℃时,产品颜色发暗,其原因可能是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上生产氯化铁有多种方法、如氯化法、熔融法、复分解法等。其中氯化法以废铁屑和氯气为原料,在一立式反应炉里反应,得到的氯化铁蒸气和尾气[用氯化亚铁溶液吸收可制得副产品(氯化铁溶液)]由炉顶排出,氯化铁蒸汽进入捕集器中冷凝为固体结晶,即是成品。某同学设计的氯化法制备氯化铁的装置如图。
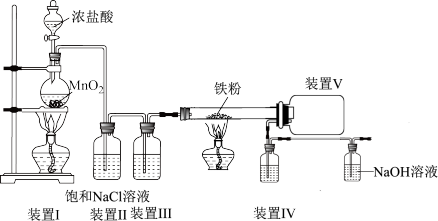
查阅资料:
①FeCl3易溶于水并且有强吸水性,吸收空气里的水分,易潮解;
②直接将FeCl3溶液加热蒸干,得到的固体是Fe(OH)3而不是FeCl3晶体。
请回答下列问题:
(1)实验前,需进行的操作是检查装置的____ 性;装置中滴加浓盐酸的仪器的名称是___ 。
(2)装置Ⅱ的作用是____ ,装置Ⅲ中盛放的试剂是___ (填名称),装置Ⅳ的作用是___ 。
(3)盛放NaOH溶液的装置的作用是___ 。
(4)氯化法制氯化铁时,得到副产品的反应的离子方程式为___ ;若向某200mL1mol·L-1FeCl2溶液中通入足量Cl2,充分反应后将所得溶液直接蒸干,并将所得固体灼烧至质量不再变化,则灼烧后残留固体的质量为___ g。

查阅资料:
①FeCl3易溶于水并且有强吸水性,吸收空气里的水分,易潮解;
②直接将FeCl3溶液加热蒸干,得到的固体是Fe(OH)3而不是FeCl3晶体。
请回答下列问题:
(1)实验前,需进行的操作是检查装置的
(2)装置Ⅱ的作用是
(3)盛放NaOH溶液的装置的作用是
(4)氯化法制氯化铁时,得到副产品的反应的离子方程式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯气广泛应用于杀菌、消毒及化工领域。某化学实验小组设计如图装置制取氯气,并探究其化学性质。
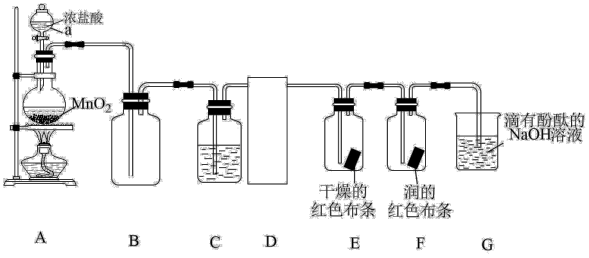
已知:氯气易溶于 等有机溶剂。回答下列问题:
等有机溶剂。回答下列问题:
(1)仪器a的名称是___________ 。
(2)用装置D收集纯净、干燥的氯气,观察其物理性质。
①推测装置B的作用是___________ ;装置C中的试剂是___________ (填名称)。
②装置D可选用___________ (填序号)。

(3)写出G中发生反应的离子方程式___________ 。
(4)装置G中溶液的红色逐渐褪去,得到无色溶液。小组同学认为溶液红色褪去的原因可能有两种:一种是氯气与水反应产生的HClO具有漂白性,使红色褪去;另一种是___________ (请用简要文字回答)。

已知:氯气易溶于
 等有机溶剂。回答下列问题:
等有机溶剂。回答下列问题:(1)仪器a的名称是
(2)用装置D收集纯净、干燥的氯气,观察其物理性质。
①推测装置B的作用是
②装置D可选用

(3)写出G中发生反应的离子方程式
(4)装置G中溶液的红色逐渐褪去,得到无色溶液。小组同学认为溶液红色褪去的原因可能有两种:一种是氯气与水反应产生的HClO具有漂白性,使红色褪去;另一种是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海洋中有丰富的资源,从中可以制取氯溴碘的单质及其化合物
Ⅰ氯气是一种重要的化工原料,是氯碱工业的主要产品之一,它是一种常用的消毒剂。由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上利用氯气和石灰乳生产漂白粉的主要化学方程式是___________________________ ,在空气中漂白粉长期存放会变质而失效的原理是(用化学方程式说明)________ 、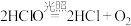 。
。
Ⅱ海水中溴元素以 形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:

请回答下列问题。
(1)将海水浓缩的方法是________ 。
(2)步骤①反应的化学方程式是________________________________ 。
(3)步骤②通入热空气吹出 ,利用了
,利用了 的
的________ (填字母)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
Ⅲ碘及其化合物在科研、生活等方面有广泛用途。如图所示为从海带中制取碘的工艺流程。
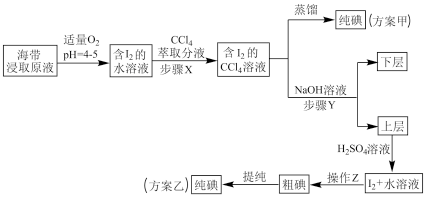
已知: 。
。
(1)步骤X中,萃取后分液漏斗内观察到的现象是__________________ 。
(2)下列有关步骤Y的说法中正确的是_______ (填字母)。
A.应控制 溶液的浓度和体积 B.将碘单质转化成碘离子进入水层
溶液的浓度和体积 B.将碘单质转化成碘离子进入水层
C.主要是除去海带浸取原液中的有机杂质 D. 溶液可以用乙醇代替
溶液可以用乙醇代替
(3)向上层清液中加入 溶液,发生反应的化学方程式为
溶液,发生反应的化学方程式为_______________________ ,由于碘单质在水中的溶解度较小,且通过富集后得到的碘单质浓度较大,操作Z的名称为___________ 。
Ⅰ氯气是一种重要的化工原料,是氯碱工业的主要产品之一,它是一种常用的消毒剂。由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上利用氯气和石灰乳生产漂白粉的主要化学方程式是
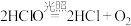 。
。Ⅱ海水中溴元素以
 形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
请回答下列问题。
(1)将海水浓缩的方法是
(2)步骤①反应的化学方程式是
(3)步骤②通入热空气吹出
 ,利用了
,利用了 的
的A.氧化性 B.还原性 C.挥发性 D.腐蚀性
Ⅲ碘及其化合物在科研、生活等方面有广泛用途。如图所示为从海带中制取碘的工艺流程。

已知:
 。
。(1)步骤X中,萃取后分液漏斗内观察到的现象是
(2)下列有关步骤Y的说法中正确的是
A.应控制
 溶液的浓度和体积 B.将碘单质转化成碘离子进入水层
溶液的浓度和体积 B.将碘单质转化成碘离子进入水层C.主要是除去海带浸取原液中的有机杂质 D.
 溶液可以用乙醇代替
溶液可以用乙醇代替(3)向上层清液中加入
 溶液,发生反应的化学方程式为
溶液,发生反应的化学方程式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】(1)如图所示,将CL2依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是____________________________________ 。
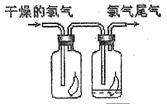
(2)为防止 Cl2,尾气污染空气,可用氢氧化钠溶液吸收多余的Cl2,原理是 (用化学方程式表示 )________________________________
根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_________________ (填化学式),
长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_____ (填字母代号)。
A.O2 B.Cl2 C.CO2 D.HCIO
(3)2004年4月15日至16日,位于重厌市江北区的天原化工总厂相继发生氯气泄漏和爆炸事故。当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是______ 。
A.NaOH B.NaCI C.KBr D.Na2CO3

(2)为防止 Cl2,尾气污染空气,可用氢氧化钠溶液吸收多余的Cl2,原理是 (用化学方程式表示 )
根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是
长期露置于空气中的漂白粉,加稀盐酸后产生的气体是
A.O2 B.Cl2 C.CO2 D.HCIO
(3)2004年4月15日至16日,位于重厌市江北区的天原化工总厂相继发生氯气泄漏和爆炸事故。当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
A.NaOH B.NaCI C.KBr D.Na2CO3
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如下装置进行实验。

请按要求回答下列问题:
(1)盛装浓盐酸仪器的名称为_______ ,圆底烧瓶中发生反应的离子方程式为_______
(2)KI溶液中观察到的现象是_______ ,反应的化学方程式为_______ 。
(3)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放的是_______ (填名称)。
(4)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液(主要成分是NaClO)而发生氯气中毒事件。请写出两者发生反应的离子方程式:_______ 。
(5)该兴趣小组用 与足量的浓盐酸制备氯气,则理论上产生的气体在标况下的体积为
与足量的浓盐酸制备氯气,则理论上产生的气体在标况下的体积为_______ L。

请按要求回答下列问题:
(1)盛装浓盐酸仪器的名称为
(2)KI溶液中观察到的现象是
(3)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放的是
(4)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液(主要成分是NaClO)而发生氯气中毒事件。请写出两者发生反应的离子方程式:
(5)该兴趣小组用
 与足量的浓盐酸制备氯气,则理论上产生的气体在标况下的体积为
与足量的浓盐酸制备氯气,则理论上产生的气体在标况下的体积为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间的转化关系如图所示(部分产物和反应条件省略).

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B______ 、丙______ .
(2)写出下列反应的离子方程式:
反应①______ ;
反应④______ .
(3)黄绿色气体乙的用途______ (列举一例即可)

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B
(2)写出下列反应的离子方程式:
反应①
反应④
(3)黄绿色气体乙的用途
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】在“比较钠、镁、铝金属活泼性”实验中,甲、乙两组的实验如下:
(1)写出钠和水反应的化学方程式___________ 。
(2)下列实验依据可判断某元素的金属性强弱的是___________。
(3)钠、镁、铝金属活泼性由强到弱顺序是___________ ;甲、乙两组实验中,组___________ 的实验更可靠,另一组不可靠的原因可能是___________ 。
(4)下列性质比较中错误的是___________。
(5)运用元素周期律分析下面的推断,其中错误的是___________。
| 甲组 | 乙组 | ||
| 实验步骤 | 实验现象 | 实验步骤 | 实验现象 |
1.取两支试管,加入 水,各滴入2滴酚酞试液,分别加入一小粒金属钠和少量镁粉,观察现象。 水,各滴入2滴酚酞试液,分别加入一小粒金属钠和少量镁粉,观察现象。将加入镁粉的试管加热至沸腾,观察现象。 | 钠:在冷水中,浮于水面,熔成小球,四处游动,逐渐缩小,溶液很快变红色。 镁:在冷水中几乎无现象,加热至沸后产生大量气体,溶液变红。 | 1.取两支试管,加入 水,各滴入2滴酚酞试液,分别加入一小粒金属钠和少量镁粉,观察现象。 水,各滴入2滴酚酞试液,分别加入一小粒金属钠和少量镁粉,观察现象。将加入镁粉的试管加热至沸腾,观察现象。 | 钠:在冷水中,浮于水面,熔成小球,四处游动,逐渐缩小,溶液很快变红色。 镁:在冷水中几乎无现象,加热至沸后产生大量气体,溶液变红。 |
2.取一小块铝和一小块镁带,用砂纸擦去表面的氧化膜,分别同时投入盛有 盐酸的两个试管中,观察现象。 盐酸的两个试管中,观察现象。 | 镁:剧烈反应,很快产生大量气体。 铝:也产生大量气体,但反应比镁慢。 | 2.取一小块铝和一小块镁带,分别同时投入盛有 盐酸的两个试管中,观察现象。 盐酸的两个试管中,观察现象。 | 镁:开始时没有现象,过一会儿产生大量气体。 铝:基本没有变化。 |
(2)下列实验依据可判断某元素的金属性强弱的是___________。
| A.导电性的强弱 |
| B.跟非金属反应生成化合物的价态高低 |
C. 该金属跟酸反应放出氢气的多少 该金属跟酸反应放出氢气的多少 |
| D.最高价氧化物对应水化物碱性的强弱 |
(4)下列性质比较中错误的是___________。
| A.元素的非金属性:P>S |
B.离子的还原性: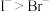 |
C.含氧酸的酸性: |
D.气态氢化物的热稳定性: |
| A.硼的氧化物的水化物可能具有两性 |
B.砹 (87At)为有色固体,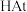 不稳定, 不稳定, 见光容易分解,不溶于水也不溶于稀酸 见光容易分解,不溶于水也不溶于稀酸 |
| C.氢氧化铷(37RbOH)易溶于水 |
D.硒化氢 (34Se)是无色、有毒、比 稳定的气体 稳定的气体 |
您最近半年使用:0次