工业上用CO生产燃料甲醇。一定条件下发生反应:
CO(g)+2 H2(g) CH3OH(g)
CH3OH(g)

(1)甲图是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=_____________;
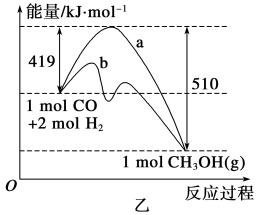
(2)乙图表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。该反应的焓变是________(填“ΔH<0”或“ΔH>0”)反应,写出反应的热化学方程式:______ _;选择适宜的催化剂__________(填“能”或“不能”)改变该反应的反应热。
(3)恒容条件下,下列措施中能使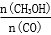 增大的有____________。
增大的有____________。
a.升高温度 b.充入1mol He气
c.再充入1 mol CO和2 mol H2 d.使用催化剂
CO(g)+2 H2(g)
 CH3OH(g)
CH3OH(g)

(1)甲图是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=_____________;
(2)乙图表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。该反应的焓变是________(填“ΔH<0”或“ΔH>0”)反应,写出反应的热化学方程式:______ _;选择适宜的催化剂__________(填“能”或“不能”)改变该反应的反应热。
(3)恒容条件下,下列措施中能使
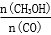 增大的有____________。
增大的有____________。a.升高温度 b.充入1mol He气
c.再充入1 mol CO和2 mol H2 d.使用催化剂
更新时间:2016-12-13 08:58:44
|
【知识点】 化学平衡
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】2SO2(g)+O2(g)) 2SO3(g)反应过程的能量变化如图所示,已知1molSO2(g)被氧化为1molSO3(g)的ΔH=-akJ/mol(a﹥0)。回答下列问题:
2SO3(g)反应过程的能量变化如图所示,已知1molSO2(g)被氧化为1molSO3(g)的ΔH=-akJ/mol(a﹥0)。回答下列问题:
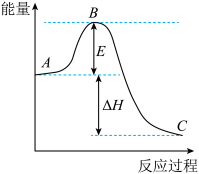
(1)图中A表示:__ ,E的大小对该反应的反应热ΔH__ (填“是”或“否”)有影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点__ (填“升高”或“降低”),理由是__ 。
(2)图中ΔH=__ kJ/mol。
(3)在一定温度下,将2molSO2和1molO2放在一密闭容器中,在催化剂作用下充分反应。测得反应放出的热量__ (填“等于”、“大于”或“小于”)2akJ。
(4)V2O5的催化循环机理可能为:V2O5氧化SO2时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:
①__ ;②4VO2+O2=2V2O5
(5)已知固态单质硫的燃烧热为bkJ/mol,计算由S(s)生成3molSO3(g)的ΔH=___ 。
 2SO3(g)反应过程的能量变化如图所示,已知1molSO2(g)被氧化为1molSO3(g)的ΔH=-akJ/mol(a﹥0)。回答下列问题:
2SO3(g)反应过程的能量变化如图所示,已知1molSO2(g)被氧化为1molSO3(g)的ΔH=-akJ/mol(a﹥0)。回答下列问题:
(1)图中A表示:
(2)图中ΔH=
(3)在一定温度下,将2molSO2和1molO2放在一密闭容器中,在催化剂作用下充分反应。测得反应放出的热量
(4)V2O5的催化循环机理可能为:V2O5氧化SO2时,自己被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:
①
(5)已知固态单质硫的燃烧热为bkJ/mol,计算由S(s)生成3molSO3(g)的ΔH=
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】气态可逆反应:mA(g)+nB(g)  pC (g)+qD(g),符合下图。试用“>”或“<”填(1)~(3)题。
pC (g)+qD(g),符合下图。试用“>”或“<”填(1)~(3)题。

(1)温度T1___________ T2,
(2)压强p1___________ p2,
(3)m+n____________ p+q,
(4)正反应为___________ 反应(填“放热”或“吸热”)。
 pC (g)+qD(g),符合下图。试用“>”或“<”填(1)~(3)题。
pC (g)+qD(g),符合下图。试用“>”或“<”填(1)~(3)题。
(1)温度T1
(2)压强p1
(3)m+n
(4)正反应为
您最近半年使用:0次
【推荐3】常见的氮氧化物有一氧化氮、二氧化氮、一氧化二氮(N2O)、五氧化二氮(N2O5)等。
(1)在一定条件下,氮气与氧气反应生成1mol一氧化氮气体,吸收90kJ的热量。该反应的热化学方程式为:_____ 。
(2)在2L密闭容器内,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间变化如表:
2NO2(g)体系中,n(NO)随时间变化如表:
①用NO表示0~2s内该反应的平均速率v(NO)=_____ mol·L-1·s-1。
②下列措施能够使该反应速率加快的是______ 。
a.降低温度 b.使用合适的催化剂 c.减小压强
③若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是_____ 。
a.混合气体的颜色保持不变
b.c(NO)∶c(O2)=2∶1
c.每消耗1molO2的同时生成2molNO2
(3)将4molA气体和2molB气体置于1L的密闭容器中,混合后发生反应:2A(g)+B(g) 2C(g),达平衡后测得C的浓度为1.2mol·L-1,求A的转化率
2C(g),达平衡后测得C的浓度为1.2mol·L-1,求A的转化率______ (必须要有“三段式”计算过程,计算过程正确3分,结果正确1分,没有过程仅有结果不得分)。
(1)在一定条件下,氮气与氧气反应生成1mol一氧化氮气体,吸收90kJ的热量。该反应的热化学方程式为:
(2)在2L密闭容器内,800℃时反应2NO(g)+O2(g)
 2NO2(g)体系中,n(NO)随时间变化如表:
2NO2(g)体系中,n(NO)随时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
②下列措施能够使该反应速率加快的是
a.降低温度 b.使用合适的催化剂 c.减小压强
③若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是
a.混合气体的颜色保持不变
b.c(NO)∶c(O2)=2∶1
c.每消耗1molO2的同时生成2molNO2
(3)将4molA气体和2molB气体置于1L的密闭容器中,混合后发生反应:2A(g)+B(g)
 2C(g),达平衡后测得C的浓度为1.2mol·L-1,求A的转化率
2C(g),达平衡后测得C的浓度为1.2mol·L-1,求A的转化率
您最近半年使用:0次



