现有下列物质:①NaHCO3 ②Na2CO3 ③Al2O3 ④Fe(OH)3 ⑤Al(OH)3 ⑥CO2 ⑦FeCl3 ⑧FeCl2 ⑨MgCl2 ⑩N2 ⑪Na2SO4·10 H2O
(1)其中既能跟稀H2SO4反应,又能跟NaOH溶液反应的是______________ (填序号),
(2)除去固体②中的固体①的方法是_______________ ;
(3)在同温同压下,测得⑩与⑥混合气体对氢气的相对密度为18,⑩的⑥体积之比为__________ ;
(4)欲配制250 mL0. 1 mol/L的Na2SO4溶液需要称量⑪的质量为________ g ;
(5)在①④⑤⑧中可以通过化合反应得到的物质有___________ (填序号);
(6)要除去⑦溶液中的少量⑧,可行的办法是( ) 。
(1)其中既能跟稀H2SO4反应,又能跟NaOH溶液反应的是
(2)除去固体②中的固体①的方法是
(3)在同温同压下,测得⑩与⑥混合气体对氢气的相对密度为18,⑩的⑥体积之比为
(4)欲配制250 mL0. 1 mol/L的Na2SO4溶液需要称量⑪的质量为
(5)在①④⑤⑧中可以通过化合反应得到的物质有
(6)要除去⑦溶液中的少量⑧,可行的办法是
| A.滴入KSCN溶液 | B.加入氯水 | C.加入铜粉 | D.加入铁粉 |
更新时间:2017-02-17 14:47:55
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)常温常压下,1.806×1023个CH4与___________ molNH3具有相同数目的氢原子,CH4与NH3的体积比为___________ 。
(2)某气体在标准状况下的密度为1.25g/L,若该气体的分子式为AB型,则其名称是___________ 。
(3)19g某二价金属氯化物中含有0.4molCl-,则该物质的化学式为___________ 。
(4)固体X在一定条件下加热分解,其方程式为2X Y↑+2Z↑+2W↑,测得生成的混合气体的密度是相同状况下H2的a倍,则X的相对分子质量为
Y↑+2Z↑+2W↑,测得生成的混合气体的密度是相同状况下H2的a倍,则X的相对分子质量为___________ 。
(2)某气体在标准状况下的密度为1.25g/L,若该气体的分子式为AB型,则其名称是
(3)19g某二价金属氯化物中含有0.4molCl-,则该物质的化学式为
(4)固体X在一定条件下加热分解,其方程式为2X
 Y↑+2Z↑+2W↑,测得生成的混合气体的密度是相同状况下H2的a倍,则X的相对分子质量为
Y↑+2Z↑+2W↑,测得生成的混合气体的密度是相同状况下H2的a倍,则X的相对分子质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列化学用语:
(1)书写电离方程式:KClO3:_____ ;H2SO4:_____
(2)某金属氯化物 MCl2 40.5g 中含有 0.6mol Cl,则 MCl 2 的摩尔质量为_____
(3)工业上用电解饱和食盐水制 Cl2,写出该反应的化学方程式:_____
(4)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请用双线桥表示其电子转移的方向和数目_____
(5)相同温度和体积的 A 和 B 两容器,A 容器中充满 O2,B 容器中充满 O3,若密度相同,则氧气和臭氧的物质的量之比为:_____ .
(1)书写电离方程式:KClO3:
(2)某金属氯化物 MCl2 40.5g 中含有 0.6mol Cl,则 MCl 2 的摩尔质量为
(3)工业上用电解饱和食盐水制 Cl2,写出该反应的化学方程式:
(4)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请用双线桥表示其电子转移的方向和数目
(5)相同温度和体积的 A 和 B 两容器,A 容器中充满 O2,B 容器中充满 O3,若密度相同,则氧气和臭氧的物质的量之比为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请回答下列问题:
(1)同温同压下,同体积的N2和SO2分子数之比为___ ,物质的量之比为___ ,原子总数之比为____ ,摩尔质量之比为___ ,质量之比为____ ,密度之比为____ 。
(2)现有质量比为11:14的CO2和CO的混合气体,则该混合气体中的CO2和CO物质的量之比为____ ,碳原子和氧原子的个数比为___ ,该混合气体的摩尔质量为____ 。
(3)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是___ ,X的相对原子质量是___ 。
(4)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是___ ,氧气的质量是___ 。
(1)同温同压下,同体积的N2和SO2分子数之比为
(2)现有质量比为11:14的CO2和CO的混合气体,则该混合气体中的CO2和CO物质的量之比为
(3)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是
(4)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】实验室在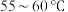 的条件下将
的条件下将 苯(密度为
苯(密度为 )与
)与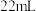 浓硫酸和
浓硫酸和 浓硝酸的混合液共热来制备硝基苯(难溶于水的油状液体),制备原理和装置如下(加热和夹持装置省略):
浓硝酸的混合液共热来制备硝基苯(难溶于水的油状液体),制备原理和装置如下(加热和夹持装置省略):
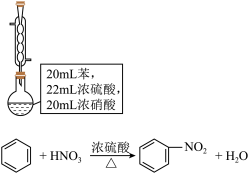
(1)实验所用苯的质量为_________ 。
(2)若该实验制备得到纯硝基苯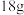 ,计算该实验中硝基苯的产率为
,计算该实验中硝基苯的产率为________ (保留小数点后两位)。
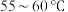 的条件下将
的条件下将 苯(密度为
苯(密度为 )与
)与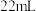 浓硫酸和
浓硫酸和 浓硝酸的混合液共热来制备硝基苯(难溶于水的油状液体),制备原理和装置如下(加热和夹持装置省略):
浓硝酸的混合液共热来制备硝基苯(难溶于水的油状液体),制备原理和装置如下(加热和夹持装置省略):
(1)实验所用苯的质量为
(2)若该实验制备得到纯硝基苯
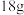 ,计算该实验中硝基苯的产率为
,计算该实验中硝基苯的产率为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是___ ,证明Fe3+存在的现象是___ 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式___ 。
(3)某工程师为了从使用过的腐蚀废液(主要含Fe3+、Fe2+、Cu2+、Cl-)中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:
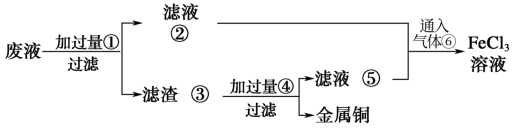
请写出上述实验中加入或生成的有关物质的化学式。
①___ ,④___ 。
(4))写出向②⑤的混合液中通入⑥的离子方程式:___ 。
(5)将铜片放入0.1mol/LFeCl3溶液中,反应一段时间后取出铜片,溶液中c(Fe3+):c(Fe2+)=2:3,则此时溶液中的Cu2+与Fe3+的物质的量之比为___ 。
(1)检验溶液中Fe3+存在的试剂是
(2)写出FeCl3溶液与金属铜发生反应的离子方程式
(3)某工程师为了从使用过的腐蚀废液(主要含Fe3+、Fe2+、Cu2+、Cl-)中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式。
①
(4))写出向②⑤的混合液中通入⑥的离子方程式:
(5)将铜片放入0.1mol/LFeCl3溶液中,反应一段时间后取出铜片,溶液中c(Fe3+):c(Fe2+)=2:3,则此时溶液中的Cu2+与Fe3+的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据所学知识,回答下列问题:
(1)0.5molH2SO4的质量为____ g;200mL含0.6NA个SO 的Al2(SO4)3溶液中溶质的物质的量浓度为
的Al2(SO4)3溶液中溶质的物质的量浓度为____ mol·L-1,溶质的物质的量为____ mol。
(2)用2.0mol·L-1的NaOH溶液吸收0.1molCl2制取简易消毒液,若Cl2恰好被完全吸收,消耗NaOH溶液的体积为____ mL。
(3)某学生欲用10mol·L-1的浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol·L-1的稀盐酸。
①该学生需要量取____ mL上述浓盐酸进行配制。
②某同学观察液面时如图所示,对所配溶液的浓度将有何影响____ ?(填“偏高”、“偏低”或“无影响”,下同)。
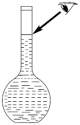
③若出现如下情况,对所配溶液的浓度将有何影响?
没有进行玻璃棒和烧杯的洗涤操作:____ ;加蒸馏水时不慎超过了刻度线:____ 。
(1)0.5molH2SO4的质量为
 的Al2(SO4)3溶液中溶质的物质的量浓度为
的Al2(SO4)3溶液中溶质的物质的量浓度为(2)用2.0mol·L-1的NaOH溶液吸收0.1molCl2制取简易消毒液,若Cl2恰好被完全吸收,消耗NaOH溶液的体积为
(3)某学生欲用10mol·L-1的浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol·L-1的稀盐酸。
①该学生需要量取
②某同学观察液面时如图所示,对所配溶液的浓度将有何影响
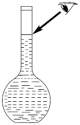
③若出现如下情况,对所配溶液的浓度将有何影响?
没有进行玻璃棒和烧杯的洗涤操作:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】高温下炼铁的主要反应为:Fe2O3(s) + 3CO(g) 2Fe(s) + 3CO2(g) - Q
(1)写出该反应的平衡常数的表达式_____________________ 。当混合气体的________________ (填物理量名称)不变时,表明上述反应已达到平衡。
(2)写出一种能提高上述反应中氧化铁转化率的措施__________________ 。取一定量铝热剂,在高温下进行铝热反应:2Al + Fe2O3  2Fe + Al2O3。
2Fe + Al2O3。
(3)请标出电子转移的方向和数目。若反应中有 1.5 mol 电子转移,可得到铁_______ g。
(4)将铝热剂直接加到足量氢氧化钠溶液中,有气体生成。请写出该现象对应的离子方程式。
_____________________________________________
(5)若将铝热反应后所得固体用足量盐酸溶解,并加入硫氰化钾溶液,溶液不变血红色。据此能否确认固体中已不含氧化铁?说明理由。
______________________________________________________________________
______________________________________________________________________
(1)写出该反应的平衡常数的表达式
(2)写出一种能提高上述反应中氧化铁转化率的措施
 2Fe + Al2O3。
2Fe + Al2O3。(3)请标出电子转移的方向和数目。若反应中有 1.5 mol 电子转移,可得到铁
(4)将铝热剂直接加到足量氢氧化钠溶液中,有气体生成。请写出该现象对应的离子方程式。
(5)若将铝热反应后所得固体用足量盐酸溶解,并加入硫氰化钾溶液,溶液不变血红色。据此能否确认固体中已不含氧化铁?说明理由。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用化学方法除去下列物质中的杂质(括号内为杂质),填写所加试剂和有关离子反应方程式___________________________ 。
| 试剂 | 离子反应方程式 | |
| ①Mg(Al) | ||
| ②FeCl2溶液(FeCl3) | ||
| ③NaHCO3(Na2CO3) |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有下列物质:①NaCl晶体②BaSO4③熔融K2SO4④Fe(OH)3胶体⑤液态氯化氢⑥稀硫酸⑦NaHCO3溶液⑧石墨⑨氨水⑩酒精⑪CO2⑫澄清石灰水。请将序号分别填入下面的横线处:
(1)上述状态下可导电的是___________ ,属于强电解质的是___________ 。
(2)⑦与少量的⑫的离子反应方程式是___________ 。
Ⅱ.选择一种试剂将下列物质中混入的少量杂质除去(括号内为杂质),并写出涉及反应的离子方程式。
Ⅰ.现有下列物质:①NaCl晶体②BaSO4③熔融K2SO4④Fe(OH)3胶体⑤液态氯化氢⑥稀硫酸⑦NaHCO3溶液⑧石墨⑨氨水⑩酒精⑪CO2⑫澄清石灰水。请将序号分别填入下面的横线处:
(1)上述状态下可导电的是
(2)⑦与少量的⑫的离子反应方程式是
Ⅱ.选择一种试剂将下列物质中混入的少量杂质除去(括号内为杂质),并写出涉及反应的离子方程式。
| 物质 | 需加入的试剂 | 离子方程式 |
| CO2(HCl) | ||
| NaCl溶液(Na2CO3) | ||
| NaHCO3溶液(Na2CO3) |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】我国将力争2060年前实现碳中和,CO2的捕捉是减少碳排放的措施之一、
(1)一种利用NaOH溶液捕捉回收CO2的过程如图所示。
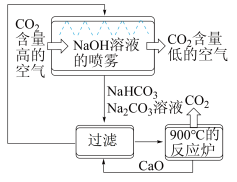
①捕捉室中NaOH溶液常喷成雾状,优点是___________ 。
②整个过程中可以循环利用的物质是___________ 。
(2)实验室模拟捕捉回收CO2,需要 溶液,现进行溶液配制。
溶液,现进行溶液配制。
①配制溶液需要的玻璃仪器是烧杯、玻璃棒和___________ 。根据计算用天平称量NaOH固体___________ g。
②在容量瓶的使用方法中,下列操作正确的是___________ 。
A.使用容量瓶前检验是否漏水
B.容量瓶用蒸馏水洗净,必须干燥后再配制溶液
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线 处,用胶头滴管加蒸馏水至刻度线。
处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线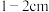 处,用胶头滴管加蒸馏水至刻度线。
处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)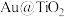 蛋黄型空心球催化剂技术实现了
蛋黄型空心球催化剂技术实现了 封存和能量储存双重效果,其原理如图所示。制得的甲烷(CH4)通过两步法可制取
封存和能量储存双重效果,其原理如图所示。制得的甲烷(CH4)通过两步法可制取 ,原理如图所示。
,原理如图所示。


①已知 中H为+1价,则空心球催化剂技术中获得的
中H为+1价,则空心球催化剂技术中获得的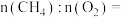
___________ 。
②写出两步法的步骤ii的化学方程式___________ 。
(1)一种利用NaOH溶液捕捉回收CO2的过程如图所示。

①捕捉室中NaOH溶液常喷成雾状,优点是
②整个过程中可以循环利用的物质是
(2)实验室模拟捕捉回收CO2,需要
 溶液,现进行溶液配制。
溶液,现进行溶液配制。①配制溶液需要的玻璃仪器是烧杯、玻璃棒和
②在容量瓶的使用方法中,下列操作正确的是
A.使用容量瓶前检验是否漏水
B.容量瓶用蒸馏水洗净,必须干燥后再配制溶液
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线
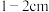 处,用胶头滴管加蒸馏水至刻度线。
处,用胶头滴管加蒸馏水至刻度线。D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线
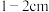 处,用胶头滴管加蒸馏水至刻度线。
处,用胶头滴管加蒸馏水至刻度线。E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)
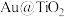 蛋黄型空心球催化剂技术实现了
蛋黄型空心球催化剂技术实现了 封存和能量储存双重效果,其原理如图所示。制得的甲烷(CH4)通过两步法可制取
封存和能量储存双重效果,其原理如图所示。制得的甲烷(CH4)通过两步法可制取 ,原理如图所示。
,原理如图所示。

①已知
 中H为+1价,则空心球催化剂技术中获得的
中H为+1价,则空心球催化剂技术中获得的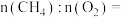
②写出两步法的步骤ii的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示:

请回答下列问题:
(1)上述实验流程中加入过量的Na2CO3的目的是____ 。
(2)按此实验方案得到的溶液3中肯定含有___ (填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___ ,之后若要获得固体NaNO3需进行的实验操作是___ (填操作名称)。
(3)下列是某学生设计NaCl、Na2SO4、NaNO3混合物中Cl-、SO42-的检验步骤请根据内容填空:
①首先检验__ 离子,应加入过量的___ ,检验是否加入过量的方法___ 。
②将所得混合物过滤,然后在溶液中加入___ 试剂检验另一离子。

请回答下列问题:
(1)上述实验流程中加入过量的Na2CO3的目的是
(2)按此实验方案得到的溶液3中肯定含有
(3)下列是某学生设计NaCl、Na2SO4、NaNO3混合物中Cl-、SO42-的检验步骤请根据内容填空:
①首先检验
②将所得混合物过滤,然后在溶液中加入
您最近一年使用:0次



