高温下炼铁的主要反应为:Fe2O3(s) + 3CO(g) 2Fe(s) + 3CO2(g) - Q
(1)写出该反应的平衡常数的表达式_____________________ 。当混合气体的________________ (填物理量名称)不变时,表明上述反应已达到平衡。
(2)写出一种能提高上述反应中氧化铁转化率的措施__________________ 。取一定量铝热剂,在高温下进行铝热反应:2Al + Fe2O3  2Fe + Al2O3。
2Fe + Al2O3。
(3)请标出电子转移的方向和数目。若反应中有 1.5 mol 电子转移,可得到铁_______ g。
(4)将铝热剂直接加到足量氢氧化钠溶液中,有气体生成。请写出该现象对应的离子方程式。
_____________________________________________
(5)若将铝热反应后所得固体用足量盐酸溶解,并加入硫氰化钾溶液,溶液不变血红色。据此能否确认固体中已不含氧化铁?说明理由。
______________________________________________________________________
______________________________________________________________________
(1)写出该反应的平衡常数的表达式
(2)写出一种能提高上述反应中氧化铁转化率的措施
 2Fe + Al2O3。
2Fe + Al2O3。(3)请标出电子转移的方向和数目。若反应中有 1.5 mol 电子转移,可得到铁
(4)将铝热剂直接加到足量氢氧化钠溶液中,有气体生成。请写出该现象对应的离子方程式。
(5)若将铝热反应后所得固体用足量盐酸溶解,并加入硫氰化钾溶液,溶液不变血红色。据此能否确认固体中已不含氧化铁?说明理由。
更新时间:2017-04-19 12:10:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】硫化氢是天然气及石油中含硫杂质,近年来发现H2S可用于高效制取氢气。回答下列问题:
(1)H2S可用FeCl3溶液、NaClO溶液及氨水等吸收。
①FeCl3溶液吸收H2S气体,该反应的还原产物为_________ 。
②NaClO溶液吸收H2S,氧化剂与还原剂的物质的量之比为4:1,则该反应的离子方程式
为___________ 。
(2) Linkkous等学者通过多硫化物作循环液,设计出如下四步反应:
(Ⅰ)H2S+OH-=HS-+H2O (Ⅱ)2HS-+H2O H2↑+S22-
H2↑+S22-
(Ⅲ)H2S+S22-=2HS-+S↓ (Ⅳ)HS-+H2O=H2S+OH-
四步反应的总反应的化学方程式为__________________ ;能量转化方式为______ 。
(3)克劳斯法脱硫包含的反应为:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H1
2H2S(g)+ SO2(g)=3S(s)+ 2H2O(l) △H2
H2S(g)+ O2(g)= S(s)+ 2H2O(l) △H3
O2(g)= S(s)+ 2H2O(l) △H3
①△H3=_________ (用△H1、△H2表示)。
②为了达到较好的脱硫率,除采用多级脱硫外,还可采取的措施是___________________ 。
(4)硫化氢裂解制氢气的反应为2H2S(g) S2 (g)+2H2 (g),设起始时容器中只有H2S,平衡时三种物质的组成与裂解温度关系如图所示。
S2 (g)+2H2 (g),设起始时容器中只有H2S,平衡时三种物质的组成与裂解温度关系如图所示。

①A点时,H2S的转化率为_______________ 。
②B点时,设容器的总压为p Pa,则平衡常数Kp为________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)H2S可用FeCl3溶液、NaClO溶液及氨水等吸收。
①FeCl3溶液吸收H2S气体,该反应的还原产物为
②NaClO溶液吸收H2S,氧化剂与还原剂的物质的量之比为4:1,则该反应的离子方程式
为
(2) Linkkous等学者通过多硫化物作循环液,设计出如下四步反应:
(Ⅰ)H2S+OH-=HS-+H2O (Ⅱ)2HS-+H2O
 H2↑+S22-
H2↑+S22-(Ⅲ)H2S+S22-=2HS-+S↓ (Ⅳ)HS-+H2O=H2S+OH-
四步反应的总反应的化学方程式为
(3)克劳斯法脱硫包含的反应为:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H1
2H2S(g)+ SO2(g)=3S(s)+ 2H2O(l) △H2
H2S(g)+
 O2(g)= S(s)+ 2H2O(l) △H3
O2(g)= S(s)+ 2H2O(l) △H3①△H3=
②为了达到较好的脱硫率,除采用多级脱硫外,还可采取的措施是
(4)硫化氢裂解制氢气的反应为2H2S(g)
 S2 (g)+2H2 (g),设起始时容器中只有H2S,平衡时三种物质的组成与裂解温度关系如图所示。
S2 (g)+2H2 (g),设起始时容器中只有H2S,平衡时三种物质的组成与裂解温度关系如图所示。
①A点时,H2S的转化率为
②B点时,设容器的总压为p Pa,则平衡常数Kp为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在 反应中,
反应中,___________ 是氧化剂;___________ 是还原剂;___________ 元素被氧化;___________ 元素被还原;被还原的 与参加反应的
与参加反应的 物质的量之比是
物质的量之比是___________ 。
 反应中,
反应中, 与参加反应的
与参加反应的 物质的量之比是
物质的量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。如图是硫、氮两元素的价类二维图。请回答下列问题:
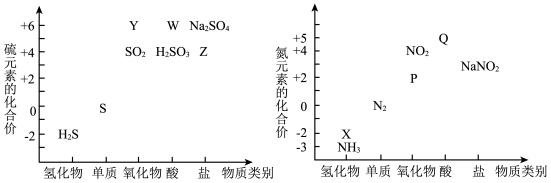
(1)物质Y是 的酸酐,其分子式为
的酸酐,其分子式为___________ 。
(2)大苏打 在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是___________。(填字母)
在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是___________。(填字母)
(3)W的浓溶液具有强氧化性、吸水性和脱水性,常用作干燥剂,则下列气体可用W干燥的是________。(填字母)
(4)在化工生产中,需要考虑控制反应条件。工业合成氨通常选择在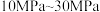 下进行,压强不能过低也不能过高的原因是:
下进行,压强不能过低也不能过高的原因是:___________ 。
(5)已知物质Z是一种可溶性正盐,能被酸性 溶液氧化为
溶液氧化为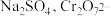 被还原为
被还原为 ,请写出此反应的离子方程式
,请写出此反应的离子方程式___________ 。
(6)将 铜与
铜与 一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质P和二氧化氮混合气体共
一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质P和二氧化氮混合气体共 。待产生的气体全部释放后,向溶液加入
。待产生的气体全部释放后,向溶液加入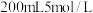 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 全部转化成沉淀,则物质Q的物质的量浓度是
全部转化成沉淀,则物质Q的物质的量浓度是___________  。
。

(1)物质Y是
 的酸酐,其分子式为
的酸酐,其分子式为(2)大苏打
 在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是___________。(填字母)
在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原的角度分析,下列选用的试剂合理的是___________。(填字母)A. | B. | C. | D. |
A. | B. | C. | D. |
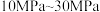 下进行,压强不能过低也不能过高的原因是:
下进行,压强不能过低也不能过高的原因是:(5)已知物质Z是一种可溶性正盐,能被酸性
 溶液氧化为
溶液氧化为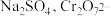 被还原为
被还原为 ,请写出此反应的离子方程式
,请写出此反应的离子方程式(6)将
 铜与
铜与 一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质P和二氧化氮混合气体共
一定浓度的物质Q充分反应,铜完全溶解,产生标准状况下的物质P和二氧化氮混合气体共 。待产生的气体全部释放后,向溶液加入
。待产生的气体全部释放后,向溶液加入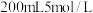 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 全部转化成沉淀,则物质Q的物质的量浓度是
全部转化成沉淀,则物质Q的物质的量浓度是 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)鉴别KCl溶液和K2CO3的试剂是_____ ,离子方程式为_____ 。
(2)除去混入NaCl溶液中少量NaHCO3杂质的试剂是______ ,离子方程式为________ 。
(3)检验未知溶液中是否有Fe3+的试剂是_______ ,实验现象为______ 。
(4)除去铁粉中混有铝粉的试剂是__________ ,化学方程式为_________ 。
(2)除去混入NaCl溶液中少量NaHCO3杂质的试剂是
(3)检验未知溶液中是否有Fe3+的试剂是
(4)除去铁粉中混有铝粉的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)为了防止氯化亚铁溶液氧化变质,常在其中加入____ ,反应的离子方程式是_____ ;
(2)除去铁粉中的铝粉,可用过量的_______ 溶液,然后过滤,反应化学方程式为_________ 。
(2)除去铁粉中的铝粉,可用过量的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】为分离废磷酸亚铁锂电池的正极材料(主要含LiFePO4和铝箔)中的金属,将正极材料粉碎后进行如下流程所示的转化:

已知LiFePO4不溶于水和碱,能溶于强酸。
(1)“碱溶”时的离子方程式为___ 。
(2)向滤液Ⅰ中通入过量CO2会析出Al(OH)3沉淀,写出该反应的离子方程式:____ 。
(3)“酸浸”时溶液中Fe2+发生反应的离子方程式为_____ 。
(4)检验“沉铁”后所得溶液中是否存在Fe3+的方法是____ 。
(5)以Fe(OH)3为原料可以制取FeSO4晶体,还需的试剂有____ 。
(6)“沉锂”时,检验Li+是否沉淀完全的方法是____ 。

已知LiFePO4不溶于水和碱,能溶于强酸。
(1)“碱溶”时的离子方程式为
(2)向滤液Ⅰ中通入过量CO2会析出Al(OH)3沉淀,写出该反应的离子方程式:
(3)“酸浸”时溶液中Fe2+发生反应的离子方程式为
(4)检验“沉铁”后所得溶液中是否存在Fe3+的方法是
(5)以Fe(OH)3为原料可以制取FeSO4晶体,还需的试剂有
(6)“沉锂”时,检验Li+是否沉淀完全的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铝、铁、铜及其化合物在日常生活中应用广泛,根据下列事实回答问题。
(1)铝土矿的主要成分是氧化铝,写出铝土矿与稀硫酸反应的离子方程式:_______ 。
(2)铁矿石主要分为赤铁矿和磁铁矿。写出赤铁矿主要成分的化学式:_______ 。磁铁矿与铝粉在一定条件下发生铝热反应,写出反应的化学方程式:_______ 。
(3)现有一定浓度的FeCl2溶液,检验溶液是否变质的方法是取少量溶液,向其中加入几滴KSCN溶液,如果溶液_______ ,证明溶液变质。
(4)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为_______ 。
(5)向新制的FeCl2溶液中滴加氢氧化钠溶液,可以观察到的现象为_______ 。
(6)Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中通入O2后,溶液很快变蓝色,试写出该反应的离子方程式:_______ 。
(1)铝土矿的主要成分是氧化铝,写出铝土矿与稀硫酸反应的离子方程式:
(2)铁矿石主要分为赤铁矿和磁铁矿。写出赤铁矿主要成分的化学式:
(3)现有一定浓度的FeCl2溶液,检验溶液是否变质的方法是取少量溶液,向其中加入几滴KSCN溶液,如果溶液
(4)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
(5)向新制的FeCl2溶液中滴加氢氧化钠溶液,可以观察到的现象为
(6)Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中通入O2后,溶液很快变蓝色,试写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题。
(1)写出重晶石主要成分的化学式_______ 。
(2)写出用氢氧化钠溶液吸收尾气氯气的化学方程式_______ 。
(3)向氯化铁溶液中滴加硫氰化钾溶液,现象是_______ 。
(1)写出重晶石主要成分的化学式
(2)写出用氢氧化钠溶液吸收尾气氯气的化学方程式
(3)向氯化铁溶液中滴加硫氰化钾溶液,现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁是地壳中占比较高的元素,其化合物在自然界十分常见。
(1)某铁原子可表示为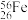 ,其核内中子数是
,其核内中子数是___________ 。
(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为___________ ;设阿伏加德罗常数的值为 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为___________ 。
(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入___________ 溶液并振荡,若滤液变为红色,则药品已变质。
(4)现有甲、乙、丙三名同学分别进行制备 胶体的实验。甲同学向
胶体的实验。甲同学向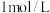 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
①操作正确的同学是___________ 。
②写出制备胶体过程中的离子方程式___________ 。欲除去胶体中混有的 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是___________ 。
③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为___________ 。
(1)某铁原子可表示为
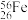 ,其核内中子数是
,其核内中子数是(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为
 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入
(4)现有甲、乙、丙三名同学分别进行制备
 胶体的实验。甲同学向
胶体的实验。甲同学向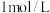 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。①操作正确的同学是
②写出制备胶体过程中的离子方程式
 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) ⇌2NO2(g)。
①随温度升高,混合气体的颜色变深。该反应正向ΔH___________ 0(填“>”或“<”);
②100℃时达平衡后,改变温度为T,c(N2O4)以0.002mol·L-1·s-1的平均速率降低,经10s又达到平衡。T___________ 100℃(填“大于”或“小于”),判断理由是___________ 。
(2)氯化铁净水原理(用离子方程式表示)___________ 。
①随温度升高,混合气体的颜色变深。该反应正向ΔH
②100℃时达平衡后,改变温度为T,c(N2O4)以0.002mol·L-1·s-1的平均速率降低,经10s又达到平衡。T
(2)氯化铁净水原理(用离子方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】向体积为2L的恒容密闭容器中通入2 molX气体和1 molY固体,在一定温度下发生如下反应:2X(g)+Y(s) 2Z(g)。已知该反应在不同温度下的平衡常数如下:
2Z(g)。已知该反应在不同温度下的平衡常数如下:
(1)该反应的平衡常数表达式K=___________ ,ΔH___________ 0(填“>”“<”“=”)。
(2)在100℃时,经10 min后反应达到平衡,此时用X的物质的量浓度变化表示的速率为___________ mol/(L·min)。X的平衡转化率为___________ 。
(3)下列情况能说明在一定条件下反应2X(g)+Y(s) 2Z(g)达到平衡状态的标志是___________。
2Z(g)达到平衡状态的标志是___________。
(4)若200℃上述容器中充入4molX、2molY和2molZ气体,则平衡向___________ (填“左”或“右”或“不移动”)。
 2Z(g)。已知该反应在不同温度下的平衡常数如下:
2Z(g)。已知该反应在不同温度下的平衡常数如下:| 温度/℃ | 100 | 150 | 200 |
| 平衡常数 | 1 | 1.2 | 1.4 |
(1)该反应的平衡常数表达式K=
(2)在100℃时,经10 min后反应达到平衡,此时用X的物质的量浓度变化表示的速率为
(3)下列情况能说明在一定条件下反应2X(g)+Y(s)
 2Z(g)达到平衡状态的标志是___________。
2Z(g)达到平衡状态的标志是___________。| A.容器内,3种物质X、Y、Z共存 |
| B.容器内气体压强不再变化 |
| C.容器内各组分浓度不再变化 |
| D.容器内密度不再变化 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】甲醇是重要的化工原料,利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇时,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1= -99kJ•mol-1
CH3OH(g) △H1= -99kJ•mol-1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2= 58kJ•mol-1
CH3OH(g)+H2O(g) △H2= 58kJ•mol-1
③CO2(g)+H2(g) CO(g)+H2O(g) △H3=+41kJ•mol-1
CO(g)+H2O(g) △H3=+41kJ•mol-1
(1)一定温度下,向体积为2L的密闭容器中加入CO和H2,假设只发生反应①,达平衡后测得各组分浓度如下:
①列式并计算平衡常数K=___ 。
②若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是___ 。
③若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正__ v逆(填“>”、“<”或“=”)。
(2)在实际生产中,当合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率α(CO)与温度和压强的关系如图所示。
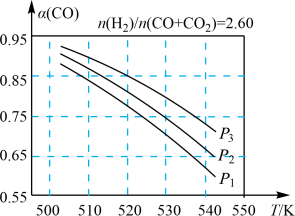
α(CO)值随温度升高而___ (填“增大”或“减小”),其原因是___ 。图中的压强由大到小为___ ,其判断理由是___ 。
①CO(g)+2H2(g)
 CH3OH(g) △H1= -99kJ•mol-1
CH3OH(g) △H1= -99kJ•mol-1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2= 58kJ•mol-1
CH3OH(g)+H2O(g) △H2= 58kJ•mol-1③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3=+41kJ•mol-1
CO(g)+H2O(g) △H3=+41kJ•mol-1(1)一定温度下,向体积为2L的密闭容器中加入CO和H2,假设只发生反应①,达平衡后测得各组分浓度如下:
| 物质 | CO | H2 | CH3OH |
| 浓度(mol•L-1) | 0.9 | 1.0 | 0.6 |
①列式并计算平衡常数K=
②若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是
③若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正
(2)在实际生产中,当合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率α(CO)与温度和压强的关系如图所示。

α(CO)值随温度升高而
您最近一年使用:0次



