已知:A为正盐,常温、常压下,B、C、D、E、G、H、I均为气体,其中D、G、H为单质,气体B能使湿润红色石蕊试纸变蓝,气体E本身为无色气体,但是与空气接触会生成一种红棕色气体I,H为黄绿色气体。F在常温下是一种无色液体。C、J的水溶液分别为两种强酸。图中反应条件(除加热外)均已略去。
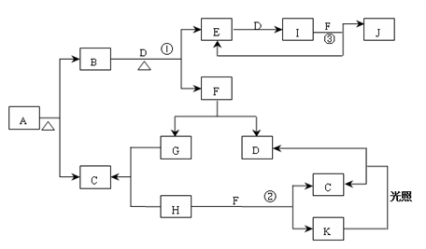
⑴写出它们的化学式: A________ 、C________ 、J________ ;
⑵实验室制备气体B的化学反应方程式为______ ;
⑶写出B+D→E+F的化学反应方程式:______ ;
⑷ J的浓溶液与单质Ag反应的离子方程式为:______ ;

⑴写出它们的化学式: A
⑵实验室制备气体B的化学反应方程式为
⑶写出B+D→E+F的化学反应方程式:
⑷ J的浓溶液与单质Ag反应的离子方程式为:
更新时间:2017-03-29 14:25:17
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】化合物A由两种元素组成,将A按如下流程进行实验。
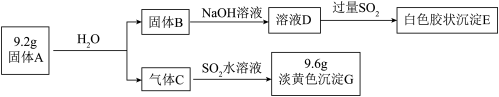
请回答:
(1)组成A的两种元素是______ ,A的化学式是____________ 。
(2)溶液D与过量  反应的离子方程式是
反应的离子方程式是__________ 。
(3)某兴趣小组利用下面实验装置制备气体C,并探究气体C能否与溶液D反应产生白色胶状沉淀:

①装置A是气体C的发生装置,写出该装置中可能发生的化学方程式__________ ,简要描述检查装置A气密性的方法:___________ 。
②该方案还缺少一个尾气吸收装置,下列吸收装置可以选用的是__________ 。
A. B.
B.  C.
C.  D.
D.

请回答:
(1)组成A的两种元素是
(2)溶液D与
 反应的离子方程式是
反应的离子方程式是(3)某兴趣小组利用下面实验装置制备气体C,并探究气体C能否与溶液D反应产生白色胶状沉淀:

①装置A是气体C的发生装置,写出该装置中可能发生的化学方程式
②该方案还缺少一个尾气吸收装置,下列吸收装置可以选用的是
A.
 B.
B.  C.
C.  D.
D.
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系:
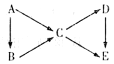
(1)若五种物质的焰色反应均为黄色,其中C、D、E的水溶液均显碱性,且等浓度时碱性C〉D〉E,B可做供氧剂。
①B中含有的化学键类型为__________ (填“离子键”、“极性键”或“非极性键”)。
②B转化成C的离子方程式为:____________________ ;
③D转化成E的离子方程式:____________________ ;
(2) 若常温下B、C、D均为气体,且D为红棕色气体。
①写出B→C的化学方程式为____________________ ;
②将B和CO2气体通入饱和食盐水中有碳酸氢钠晶体析出,反应的离子方程式是:__________ ;
(3)若C为浅绿色溶液,B为黄色溶液,E为红褐色沉淀,写出D转化成E的化学方程式:____________________ ;

(1)若五种物质的焰色反应均为黄色,其中C、D、E的水溶液均显碱性,且等浓度时碱性C〉D〉E,B可做供氧剂。
①B中含有的化学键类型为
②B转化成C的离子方程式为:
③D转化成E的离子方程式:
(2) 若常温下B、C、D均为气体,且D为红棕色气体。
①写出B→C的化学方程式为
②将B和CO2气体通入饱和食盐水中有碳酸氢钠晶体析出,反应的离子方程式是:
(3)若C为浅绿色溶液,B为黄色溶液,E为红褐色沉淀,写出D转化成E的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】新型耐火材料M由三种短周期元素组成,涉及M的转化关系如图所示:

已知:气体E是直线形三原子分子;气体G能使湿润的红色石蕊试纸变蓝;化合物A,C的实验式中的原子总数和电子总数均相等(图中的某些产物未列出)。请回答下列问题:
(1)气体G分子的VSEPR模型为_____ ,空间结构为_____ 。
(2)白色沉淀K是两性氢氧化物,写出其酸式电离的电离方程式_____ 。
(3)组成M的三种元素的第一电离能由大到小的顺序为_____ (用元素符号表示)。
(4)反应①的化学方程式为_____ 。
(5)设计实验确定溶液F中所含溶质的阴离子的方法:_____ 。

已知:气体E是直线形三原子分子;气体G能使湿润的红色石蕊试纸变蓝;化合物A,C的实验式中的原子总数和电子总数均相等(图中的某些产物未列出)。请回答下列问题:
(1)气体G分子的VSEPR模型为
(2)白色沉淀K是两性氢氧化物,写出其酸式电离的电离方程式
(3)组成M的三种元素的第一电离能由大到小的顺序为
(4)反应①的化学方程式为
(5)设计实验确定溶液F中所含溶质的阴离子的方法:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】硫酰氯(SO2Cl2)是一种重要的化工试剂,氯化法是合成硫酰氯(SO2Cl2)的常用方法。实验室合成硫酰氯的实验装置如下图所示(部分夹持装置未画出):
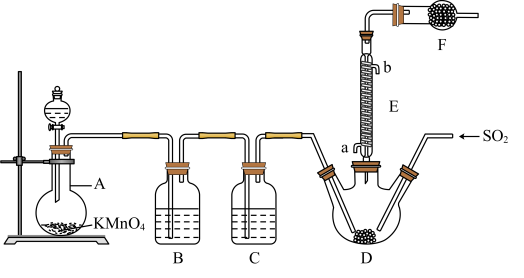
已知:① SO2(g) + Cl2(g)=SO2Cl2(l) ΔH=-97.3 kJ/mol。
② 硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”。
③ 100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。
回答下列问题:
(1) 装置A中发生反应的离子方程式为___________ 。
(2) 装置B的作用为_______________________________ ,若缺少装置C,装置D中SO2与Cl2还可能发生反应的化学方程式为________________________ 。
(3) 仪器F的名称为_________________ ,E中冷凝水的入口是___________ (填“a”或“b”),F的作用为_______________________________________________ 。
(4) 当装置A中排出氯气1.12 L(已折算成标准状况)时,最终得到5.4 g纯净的硫酰氯,则硫酰氯的产率为____________ 。为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有________ (填序号)。
① 先通冷凝水,再通气② 控制气流速率,宜慢不宜快
③ 若三颈烧瓶发烫,可适当降温④ 加热三颈烧瓶
(5) 氯磺酸(ClSO3H)加热分解,也能制得硫酰氯2ClSO3H=SO2Cl2 + H2SO4,分离产物的方法是_____
A.重结晶B.过滤 C.蒸馏D.萃取
(6) 长期存放的硫酰氯会发黄,其原因可能为_______________________ 。

已知:① SO2(g) + Cl2(g)=SO2Cl2(l) ΔH=-97.3 kJ/mol。
② 硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”。
③ 100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。
回答下列问题:
(1) 装置A中发生反应的离子方程式为
(2) 装置B的作用为
(3) 仪器F的名称为
(4) 当装置A中排出氯气1.12 L(已折算成标准状况)时,最终得到5.4 g纯净的硫酰氯,则硫酰氯的产率为
① 先通冷凝水,再通气② 控制气流速率,宜慢不宜快
③ 若三颈烧瓶发烫,可适当降温④ 加热三颈烧瓶
(5) 氯磺酸(ClSO3H)加热分解,也能制得硫酰氯2ClSO3H=SO2Cl2 + H2SO4,分离产物的方法是
A.重结晶B.过滤 C.蒸馏D.萃取
(6) 长期存放的硫酰氯会发黄,其原因可能为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】PCl3是磷的常见氯化物,可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
如图是实验室制备PCl3的装置(部分仪器已省略)。

(1)仪器乙的名称是________________________ 。
(2)实验室用二氧化锰和浓盐酸反应制备Cl2的离子方程式__________________________ 。实验过程中,为减少PCl5的生成,应控制____________________________________ 。
(3)碱石灰的作用:一是防止空气中的水蒸气进入而使PCl3水解;二是吸收多余的Cl2,防止污染环境。写出PCl3遇水反应的化学方程式____________________________________ 。
(4)向仪器甲中通入干燥Cl2之前,应先通入一段时间CO2排尽装置中的空气,其目的是________________________________________________________________________ 。
(5)测定产品中PCl3纯度的方法如下:迅速称取4.100 g产品,水解完全后配成500 mL溶液,取出25.00 mL加入过量的0.1000 mol·L-120.00 mL碘溶液,充分反应后再用0.1000 mol·L-1 Na2S2O3溶液滴定过量的碘,以淀粉溶液作指示剂,终点时消耗12.00 mL Na2S2O3溶液。已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;假设测定过程中没有其它反应。滴定终点的现象是:____________________________________________ 。根据上述数据,该产品中PCl3(相对分子质量为137.5)的质量分数为_________________ 。
| 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其它 | |
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P+3Cl2(少量)  2PCl3 2PCl32P+5Cl2(过量)  2PCl5 2PCl5 |
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl, 遇O2生成POCl3 |

(1)仪器乙的名称是
(2)实验室用二氧化锰和浓盐酸反应制备Cl2的离子方程式
(3)碱石灰的作用:一是防止空气中的水蒸气进入而使PCl3水解;二是吸收多余的Cl2,防止污染环境。写出PCl3遇水反应的化学方程式
(4)向仪器甲中通入干燥Cl2之前,应先通入一段时间CO2排尽装置中的空气,其目的是
(5)测定产品中PCl3纯度的方法如下:迅速称取4.100 g产品,水解完全后配成500 mL溶液,取出25.00 mL加入过量的0.1000 mol·L-120.00 mL碘溶液,充分反应后再用0.1000 mol·L-1 Na2S2O3溶液滴定过量的碘,以淀粉溶液作指示剂,终点时消耗12.00 mL Na2S2O3溶液。已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;假设测定过程中没有其它反应。滴定终点的现象是:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
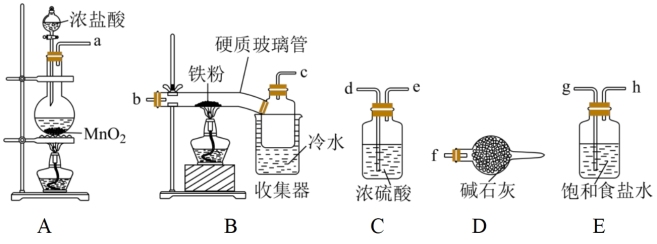
【推荐3】已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验。_______ 。
(2)B中收集器里盛放冷水的作用是_______ 。D中碱石灰的作用是_______ 、_______ 。
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸,充分反应后,进行如下实验:
固体混合物 淡黄色溶液
淡黄色溶液 淡红色溶液
淡红色溶液 深红色溶液
深红色溶液 红色褪去
红色褪去
①试剂X为_______ (填化学式)。
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是_______ 。
(4)该小组同学对上述溶液红色褪去的原因进行探究。
①取褪色后的溶液三份,分别进行以下实验,研究溶液中存在的微粒。
a.一份中滴加FeCl3溶液无明显变化,说明_______ ;
b.另一份滴加试剂X,溶液出现红色,说明_______ ;
c.还有一份滴加稀盐酸和BaCl2溶液,产生白色沉淀,说明_______ 。
②另取FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。实验②的目的是_______ ;得出结论:_______ 。
(2)B中收集器里盛放冷水的作用是
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸,充分反应后,进行如下实验:
固体混合物
 淡黄色溶液
淡黄色溶液 淡红色溶液
淡红色溶液 深红色溶液
深红色溶液 红色褪去
红色褪去①试剂X为
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是
(4)该小组同学对上述溶液红色褪去的原因进行探究。
①取褪色后的溶液三份,分别进行以下实验,研究溶液中存在的微粒。
a.一份中滴加FeCl3溶液无明显变化,说明
b.另一份滴加试剂X,溶液出现红色,说明
c.还有一份滴加稀盐酸和BaCl2溶液,产生白色沉淀,说明
②另取FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。实验②的目的是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
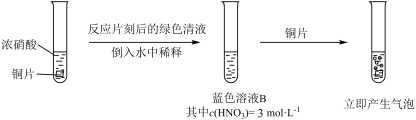
【推荐1】某小组探究Cu与 反应,发现有趣的现象,室温下3mol/L的稀硝酸(溶液A)遇铜片短时间内无明显变化,一段时间后才有少量气泡产生,而溶液B(见图)遇铜片立即产生气泡。
反应,发现有趣的现象,室温下3mol/L的稀硝酸(溶液A)遇铜片短时间内无明显变化,一段时间后才有少量气泡产生,而溶液B(见图)遇铜片立即产生气泡。
探究溶液B遇铜片立即发生反应的原因。
①假设1:___________ 对该反应有催化作用。
实验验证:将溶液A中加入少量硝酸铜,溶液呈浅蓝色,放入铜片,没有明显变化。
结论:假设1不成立。
②假设2: 对该反应有催化作用。
对该反应有催化作用。
方案Ⅰ 向盛有铜片的溶液A中通入少量 ,铜片表面立即产生气泡,反应持续进行。有同学认为应补充对比实验:向盛有铜片的溶液A中加入几滴5mol/L的硝酸,没有明显变化。补充该实验的目的是
,铜片表面立即产生气泡,反应持续进行。有同学认为应补充对比实验:向盛有铜片的溶液A中加入几滴5mol/L的硝酸,没有明显变化。补充该实验的目的是___________ 。
方案Ⅱ 向溶液B中通入氮气数分钟得溶液C.相同条件下,铜片与A、B、C三份溶液的反应速率:B>C>A,该实验能够证明假设2成立的理由是___________ 。
③查阅资料: 溶于水可以生成
溶于水可以生成 和
和___________ 。
向盛有铜片的溶液A中加入___________ ,铜片上立即产生气泡,证明 对该反应也有催化作用。
对该反应也有催化作用。
结论: 和
和 均对Cu与
均对Cu与 的反应有催化作用。
的反应有催化作用。
④Cu与稀 反应中,
反应中, 参与的可能催化过程如下:将ⅱ补充完整。
参与的可能催化过程如下:将ⅱ补充完整。
i.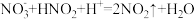
ⅱ.___________
ⅲii.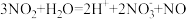
 反应,发现有趣的现象,室温下3mol/L的稀硝酸(溶液A)遇铜片短时间内无明显变化,一段时间后才有少量气泡产生,而溶液B(见图)遇铜片立即产生气泡。
反应,发现有趣的现象,室温下3mol/L的稀硝酸(溶液A)遇铜片短时间内无明显变化,一段时间后才有少量气泡产生,而溶液B(见图)遇铜片立即产生气泡。探究溶液B遇铜片立即发生反应的原因。

①假设1:
实验验证:将溶液A中加入少量硝酸铜,溶液呈浅蓝色,放入铜片,没有明显变化。
结论:假设1不成立。
②假设2:
 对该反应有催化作用。
对该反应有催化作用。方案Ⅰ 向盛有铜片的溶液A中通入少量
 ,铜片表面立即产生气泡,反应持续进行。有同学认为应补充对比实验:向盛有铜片的溶液A中加入几滴5mol/L的硝酸,没有明显变化。补充该实验的目的是
,铜片表面立即产生气泡,反应持续进行。有同学认为应补充对比实验:向盛有铜片的溶液A中加入几滴5mol/L的硝酸,没有明显变化。补充该实验的目的是方案Ⅱ 向溶液B中通入氮气数分钟得溶液C.相同条件下,铜片与A、B、C三份溶液的反应速率:B>C>A,该实验能够证明假设2成立的理由是
③查阅资料:
 溶于水可以生成
溶于水可以生成 和
和向盛有铜片的溶液A中加入
 对该反应也有催化作用。
对该反应也有催化作用。结论:
 和
和 均对Cu与
均对Cu与 的反应有催化作用。
的反应有催化作用。④Cu与稀
 反应中,
反应中, 参与的可能催化过程如下:将ⅱ补充完整。
参与的可能催化过程如下:将ⅱ补充完整。i.
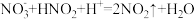
ⅱ.
ⅲii.
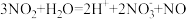
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】氨氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸的制备和性质,设计了如下图所示的装置。

(1)若分液漏斗中氨水的浓度为9.0mol·L-1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、量筒、玻璃棒、__________ 。
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X为_________ 。
(3)乙装置的作用是__________ ;写出受热时丙装置发生反应的化学方程式为______________ 。
(4)当戊中观察到___________ 现象,则说明已制得硝酸;某同学按上图组装仪器并检验气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因___________ ,如何改进装置__________ 。
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是_______________ ;为测定试管丁内硝酸溶液的浓度,从中取10mL溶液于锥形瓶中,用0.1 mol·L-1的NaOH溶液滴定,滴定前发现滴定管尖嘴处有少量气泡,请选择排出气泡的正确操作是______________ 。


(1)若分液漏斗中氨水的浓度为9.0mol·L-1,配制该浓度的氨水100mL,用到的玻璃仪器有100mL容量瓶、烧杯、量筒、玻璃棒、
(2)甲装置不需要加热即能同时产生氨气和氧气,烧瓶内固体X为
(3)乙装置的作用是
(4)当戊中观察到
(5)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在常温常压(或稍低温度)下合成,其熔点-64.5℃,沸点-5.5℃,遇水易水解。实验室模拟制备装置如图所示(部分夹持装置省略),D中三颈烧瓶置于-10℃冰盐水中。
(1)仪器甲的名称是________ 。
(2)图示装置中恒压漏斗与分液漏斗相比,其优点为___________ 。
(3) NOC1分子中各原子均满足8电子稳定结构,则NOCl的电子式为_________ 。
(4)实验开始时,先打开K1、K2,关闭K3,打开分液漏斗活塞滴入适量稀硝酸,至C中红棕色完全消失后,关闭K1、K2,此时装置C的作用为___________ 。滴入适量浓盐酸,点燃酒精灯,当_______ (填装置符号)中充满黄绿色气体时,打开K1、K3,制备NOC1。_______ ;丙为尾气处理装置,则最佳选择为_____ 。

(1)仪器甲的名称是
(2)图示装置中恒压漏斗与分液漏斗相比,其优点为
(3) NOC1分子中各原子均满足8电子稳定结构,则NOCl的电子式为
(4)实验开始时,先打开K1、K2,关闭K3,打开分液漏斗活塞滴入适量稀硝酸,至C中红棕色完全消失后,关闭K1、K2,此时装置C的作用为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】已知X是一种酸式盐,常用作化肥,其有如下转化,图中的每一个方格表示有关的一种反应物或生成物,其中常温下,A、C为无色气体。
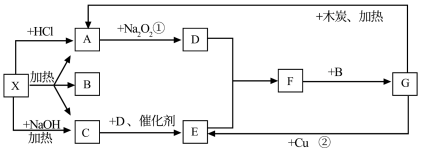
(1)写出有关物质的化学式:X___________ ;F___________ 。
(2)写出 的化学方程式:
的化学方程式:___________ 。
(3)写出实验室制备C的化学方程式:___________ 。
(4)分别取两份50mL NaOH溶液,各向其中通入一定量的A气体,随后各取反应后溶液10mL,分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入 的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl溶液体积之间的关系如图所示,试分析:
的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl溶液体积之间的关系如图所示,试分析:
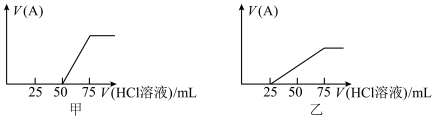
①NaOH溶液在吸收A气体后,溶液乙中存在的溶质是___________ ,其物质的量之比是___________ 。
②原NaOH溶液的物质的量浓度是___________  ,溶液甲最多还能吸收A气体的体积为
,溶液甲最多还能吸收A气体的体积为___________ mL(标准状况)。

(1)写出有关物质的化学式:X
(2)写出
 的化学方程式:
的化学方程式:(3)写出实验室制备C的化学方程式:
(4)分别取两份50mL NaOH溶液,各向其中通入一定量的A气体,随后各取反应后溶液10mL,分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入
 的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl溶液体积之间的关系如图所示,试分析:
的HCl溶液,产生的A气体体积(标准状况下)与所加入的HCl溶液体积之间的关系如图所示,试分析:
①NaOH溶液在吸收A气体后,溶液乙中存在的溶质是
②原NaOH溶液的物质的量浓度是
 ,溶液甲最多还能吸收A气体的体积为
,溶液甲最多还能吸收A气体的体积为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某化学学习小组在帮助老师整理实验室的化学试剂时,发现一盛无色盐溶液的试剂瓶,标签破损如右图,该小组根据已掌握的知识,对药品作出猜想,并设计实验验证。

(1)该实验药品为中学化学常用试剂,推测它的阳离子化合价为______________________ 。
(2)同学们做出以下三种推测。
猜想1:Na2SO4
实验设计: 进行……,.证明是Na2SO4溶液;
猜想2: K2SO4
实验设计:____________________________ ,证明是K2SO4溶液;
猜想3; (NH4)2SO4
实验设计:____________________________ ,证明是(NH4)2SO4溶液。
(3)通过实验发现“猜想3”成立,已知(NH4)2SO4受热易分解,该小组拟用下图所示装置探究其分解产物。(夹持和加热装置略)
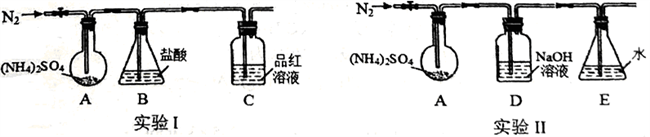
实验I:装置B 盛0.5000mol/L盐酸50.00mL,通入N2排尽空气后,将装置A 加热至260℃一段时间,停止加热,停止通入N2,品红溶液不褪色,取下装置B,用0.1000mol/LNaOH溶液滴定剩余盐酸,消耗NaOH 溶液50.00mL。经检验滴定后的溶液中无SO42-。
①请从右图选择盛放0.1000mol/LNaOH 溶液的滴定管____________ (填“甲”或“乙”)。
②装置B 内溶液吸收气体的物质的量是_____________________ mol。
实验Ⅱ:通入N2排尽空气后,将装置A 加热到400℃,至固体无残留,停止加热,停止通入N2,观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。
①装置E 的作用是____________________________ 。
②A、D之间的导气管内的少量白色固体是____________________________ 。
③有同学提出在AD之间需要增加一个防倒吸的安全瓶,老师说不需要,原因是____________________________ 。
④进一步研究发现,气体产物中无氮氧化物,则(NH4)2SO4在400℃分解的化学方程式是_______________________________ 。

(1)该实验药品为中学化学常用试剂,推测它的阳离子化合价为
(2)同学们做出以下三种推测。
猜想1:Na2SO4
实验设计: 进行……,.证明是Na2SO4溶液;
猜想2: K2SO4
实验设计:
猜想3; (NH4)2SO4
实验设计:
(3)通过实验发现“猜想3”成立,已知(NH4)2SO4受热易分解,该小组拟用下图所示装置探究其分解产物。(夹持和加热装置略)

实验I:装置B 盛0.5000mol/L盐酸50.00mL,通入N2排尽空气后,将装置A 加热至260℃一段时间,停止加热,停止通入N2,品红溶液不褪色,取下装置B,用0.1000mol/LNaOH溶液滴定剩余盐酸,消耗NaOH 溶液50.00mL。经检验滴定后的溶液中无SO42-。

①请从右图选择盛放0.1000mol/LNaOH 溶液的滴定管
②装置B 内溶液吸收气体的物质的量是
实验Ⅱ:通入N2排尽空气后,将装置A 加热到400℃,至固体无残留,停止加热,停止通入N2,观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。
①装置E 的作用是
②A、D之间的导气管内的少量白色固体是
③有同学提出在AD之间需要增加一个防倒吸的安全瓶,老师说不需要,原因是
④进一步研究发现,气体产物中无氮氧化物,则(NH4)2SO4在400℃分解的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】一定条件下经不同的化学反应,可以实现图示变化,A为酸式盐;B为无色无味气体;无色气体D可使红色石蕊试纸变蓝:X、F和Y为气体单质,且Y为有色气体,F为空气的主要成分之一;G为正盐,G和无色气体M在溶液中可反应生成B。
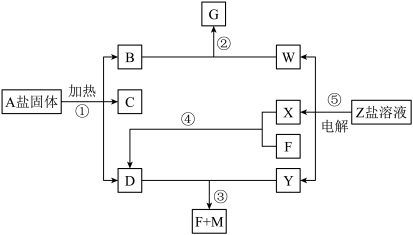
(1)写出下列物质的化学式:A___________ ;Y___________
(2)写出反应⑤的离子方程式___________ 。
(3)写出反应③的化学方程式___________ 。
(4)常温下pH=10,体积均为100mL的D、W两溶液与M反应,消耗的M的物质的量关系D___________ W(填“大于”“小于”或“等于”)。

(1)写出下列物质的化学式:A
(2)写出反应⑤的离子方程式
(3)写出反应③的化学方程式
(4)常温下pH=10,体积均为100mL的D、W两溶液与M反应,消耗的M的物质的量关系D
您最近一年使用:0次



