氧化铝在工业上有着广泛的应用。(写出计算过程)
(1)制取净水剂氯化铝。其原理为:Al2O3+3C+3Cl2 2AlCl3+3CO。25.5g 氧化铝、3.6g 碳、4.48L(标准状态)氯气混合后在高温下反应,理论上可得氯化铝
2AlCl3+3CO。25.5g 氧化铝、3.6g 碳、4.48L(标准状态)氯气混合后在高温下反应,理论上可得氯化铝_____ 克。
(2)向100g氢氧化钠溶液中加入10g 氧化铝,充分反应后,剩余固体4.9克。测得所得溶液的密度为1.051g/cm3 。则所得溶液的物质的量浓度为______________ 。
(3)超细氮化铝粉末被广泛应用于大规模集成电路生产等领域。其制取原理为:Al2O3+N2+3C 2AlN+3CO。由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。
2AlN+3CO。由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。
① 取一定量样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g·L-1(已折算成标准状况,AIN不跟O2反应)。该样品中含杂质炭__________ g。
② 向①中反应后的容器中加入过量的NaOH浓溶液共热并蒸干,AlN跟NaOH溶液反应生成NaAlO2,得到氨气3.36L(标准状况)及16.38g的固体。再将该固体配成溶液,向其中慢慢加入1mol/L盐酸,当加到20mL时开始产生沉淀。求该样品中的AlN的质量分数为________ 。(用小数表示,保留2位小数)
(4)用氧化铝为原料可制得含铝化合物X。取6.9gX放入100mL水中完全溶解,溶液呈弱酸性。取出10mL加入过量盐酸,无气泡,再加入过量氯化钡有白色沉淀0.932g 。另取10mL样品,慢慢滴加氢氧化钠溶液直至过量,过程中出现的现象为出现白色沉淀→沉淀逐渐增多→沉淀不再变化→沉淀开始减少→沉淀全部消失。若改用氨水做上述实验最终可得0.156g沉淀。经测定X中含氢量为4.64% 。求化合物X的化学式_______ 。
(1)制取净水剂氯化铝。其原理为:Al2O3+3C+3Cl2
 2AlCl3+3CO。25.5g 氧化铝、3.6g 碳、4.48L(标准状态)氯气混合后在高温下反应,理论上可得氯化铝
2AlCl3+3CO。25.5g 氧化铝、3.6g 碳、4.48L(标准状态)氯气混合后在高温下反应,理论上可得氯化铝(2)向100g氢氧化钠溶液中加入10g 氧化铝,充分反应后,剩余固体4.9克。测得所得溶液的密度为1.051g/cm3 。则所得溶液的物质的量浓度为
(3)超细氮化铝粉末被广泛应用于大规模集成电路生产等领域。其制取原理为:Al2O3+N2+3C
 2AlN+3CO。由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。
2AlN+3CO。由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。① 取一定量样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g·L-1(已折算成标准状况,AIN不跟O2反应)。该样品中含杂质炭
② 向①中反应后的容器中加入过量的NaOH浓溶液共热并蒸干,AlN跟NaOH溶液反应生成NaAlO2,得到氨气3.36L(标准状况)及16.38g的固体。再将该固体配成溶液,向其中慢慢加入1mol/L盐酸,当加到20mL时开始产生沉淀。求该样品中的AlN的质量分数为
(4)用氧化铝为原料可制得含铝化合物X。取6.9gX放入100mL水中完全溶解,溶液呈弱酸性。取出10mL加入过量盐酸,无气泡,再加入过量氯化钡有白色沉淀0.932g 。另取10mL样品,慢慢滴加氢氧化钠溶液直至过量,过程中出现的现象为出现白色沉淀→沉淀逐渐增多→沉淀不再变化→沉淀开始减少→沉淀全部消失。若改用氨水做上述实验最终可得0.156g沉淀。经测定X中含氢量为4.64% 。求化合物X的化学式
17-18高三上·上海·阶段练习 查看更多[2]
更新时间:2017-04-06 10:16:58
|
相似题推荐
填空题
|
困难
(0.15)
【推荐1】稀土元素是周期表中ⅢB族钪、钇和镧系元素之总称,金属活泼性仅次于碱金属和碱土金属元素,它们的性质极为相似,常见化合价为+3价。无论是航天、航空、军事等高科技领域,还是传统工农业,稀土的应用几乎是无所不在。其中钇(Y)元素是激光和超导的重要材料。我国蕴藏着丰富的含钇矿石(Y2FeBe2Si2O10),工业上通过如下生产流程可获得氧化钇。
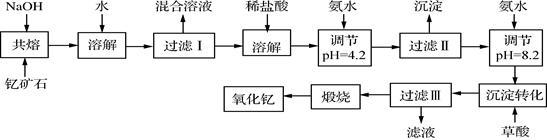
已知:
①有关金属离子形成氢氧化物沉淀时的pH见下表。
②Be(OH)2+2NaOH Na2BeO2+2H2O
Na2BeO2+2H2O
请回答下列问题:
(1)过滤Ⅲ所得滤液的溶质主要有______________ 。
(2)①欲从过滤I所得混合溶液中制得Be(OH)2沉淀,最好选用盐酸和________ 两种试剂,再通过必要的操作即可实现。
a.NaOH溶液 b.氨水 c.CO2 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式_____________________ 。
(3)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数K=
Fe(OH)3+3H+的平衡常数K=_______________________ 。
(4)写出煅烧过程的化学方程式_________________________ 。

已知:
①有关金属离子形成氢氧化物沉淀时的pH见下表。
| 离子 | 开始沉淀时 的pH | 完全沉淀时 的pH |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
 Na2BeO2+2H2O
Na2BeO2+2H2O请回答下列问题:
(1)过滤Ⅲ所得滤液的溶质主要有
(2)①欲从过滤I所得混合溶液中制得Be(OH)2沉淀,最好选用盐酸和
a.NaOH溶液 b.氨水 c.CO2 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式
(3)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O
 Fe(OH)3+3H+的平衡常数K=
Fe(OH)3+3H+的平衡常数K=(4)写出煅烧过程的化学方程式
您最近半年使用:0次
填空题
|
困难
(0.15)
【推荐2】辉铜矿是一种重要的铜矿石,主要含有硫化亚铜(Cu2S),还有Fe2O3、SiO2及一些不溶性杂质。一种以辉铜矿石为原料制备硝酸铜晶体的工艺流程如下:
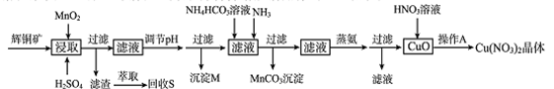
已知:部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
回答下列问题
(1)浸取后得到的浸出液中含有CuSO4、MnSO4。写出浸取时产生CuSO4、MnSO4反应的化学方程式__________ 。
(2)调节pH的目的是___________ ,pH的调节范围为___________ 。
(3)生成MnCO3沉淀的离子方程式为___________ 。
(4)操作A为___________ 。
(5)由辉铜矿制取铜的反应过程可以表示为:
2Cu2S(s)+3O2(g)═ 2Cu2O(s)+ 2SO2(g)△H=﹣768.2kJ/mol
2Cu2O(s)+ Cu2S(s)═ 6Cu(s)+ SO2(g)△H=" +116.0" kJ/mol
则由Cu2S与O2加热反应生成Cu的热化学方程式为___________ 。
(6)若用含85% Cu2S(Mr=160)的辉铜矿来制备无水Cu(NO3)2,假设浸取率为95%,调节pH时损Cu 3%,蒸氨过程中有5%未转化为CuO,其它过程中无损耗,则1.6 kg这样的辉铜矿最多能制备__________ mol无水Cu(NO3)2。(计算结果精确到小数点后1位)

已知:部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
| 离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
回答下列问题
(1)浸取后得到的浸出液中含有CuSO4、MnSO4。写出浸取时产生CuSO4、MnSO4反应的化学方程式
(2)调节pH的目的是
(3)生成MnCO3沉淀的离子方程式为
(4)操作A为
(5)由辉铜矿制取铜的反应过程可以表示为:
2Cu2S(s)+3O2(g)═ 2Cu2O(s)+ 2SO2(g)△H=﹣768.2kJ/mol
2Cu2O(s)+ Cu2S(s)═ 6Cu(s)+ SO2(g)△H=" +116.0" kJ/mol
则由Cu2S与O2加热反应生成Cu的热化学方程式为
(6)若用含85% Cu2S(Mr=160)的辉铜矿来制备无水Cu(NO3)2,假设浸取率为95%,调节pH时损Cu 3%,蒸氨过程中有5%未转化为CuO,其它过程中无损耗,则1.6 kg这样的辉铜矿最多能制备
您最近半年使用:0次
填空题
|
困难
(0.15)
解题方法
【推荐3】钼酸钠(Na2MoO4)具有广泛的用途.可做新型水处理荆、优良的金属缓蚀剂及可用于局部过热的循环水系统;Al(OH)3工业和医药上都具有重要用途.现从某废钼催化剂(主要成分MoO3、Al2O3、Fe2O3等)中回收Na2MoO4和Al(OH)3,其工艺如图:
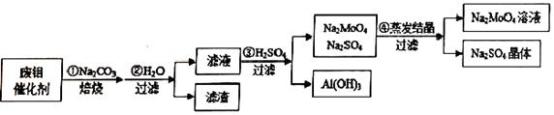
回答下列问题:
(1)已知MoO3、Al2O3与SiO2相似,均能在高温下跟Na2CO3发生类似反应,试写出MoO3与Na2CO3反应的化学方程式:__________________ 。
(2)第②步操作所后的滤液中,溶质有Na2MoO4、_________ 和过量的Na2CO3;检验第②步操作所得滤渣中含有三价铁的方法是___________________ 。
(3)第③步操作H2SO4需要适量,通常是通过_________ 来调控H2SO4的用量;与Na2SO4相比,Na2MoO4的溶解度受温度的影响变化__________ (填“较大”或“较小”)。
(4)利用铝热反应可回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得MoO3。写出MoO3发生铝热反应的化学方程式:_________________ 。
(5)取废钼催化剂5.00g,加入5.30gNa2CO3(足量),经上述实验操作后,最终得到2.34g Al(OH)3和6.39gNa2SO4晶体,则废钼催化剂中Al2O3、MoO3的物质的量的比值为_______ 。

回答下列问题:
(1)已知MoO3、Al2O3与SiO2相似,均能在高温下跟Na2CO3发生类似反应,试写出MoO3与Na2CO3反应的化学方程式:
(2)第②步操作所后的滤液中,溶质有Na2MoO4、
(3)第③步操作H2SO4需要适量,通常是通过
(4)利用铝热反应可回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得MoO3。写出MoO3发生铝热反应的化学方程式:
(5)取废钼催化剂5.00g,加入5.30gNa2CO3(足量),经上述实验操作后,最终得到2.34g Al(OH)3和6.39gNa2SO4晶体,则废钼催化剂中Al2O3、MoO3的物质的量的比值为
您最近半年使用:0次
填空题
|
困难
(0.15)
名校
解题方法
【推荐1】计算
(1)将200mL3mol/L的Al2(SO4)3溶液稀释至500mL,求稀释后硫酸根的浓度为多少______ ?
(2)将K2SO4和Al2(SO4)3和KAl(SO4)2三种混合溶液加H2SO4酸化。测得c(SO )=1.05 mol/L, c(Al3+)=0.55 mol/L,c(H+)=0.10mol/L(假设H2SO4完全电离为H+和SO
)=1.05 mol/L, c(Al3+)=0.55 mol/L,c(H+)=0.10mol/L(假设H2SO4完全电离为H+和SO ),则c(K+)为多少
),则c(K+)为多少 ______ ?
(3)Fe、Al混合物共0.2mol,用盐酸将其完全溶解,放出标准状况下5.6L气体,然后再滴入4mol/L的NaOH溶液,请计算:
①求该混合物中Fe、Al的物质的量______ ?
②若该Fe、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Fe2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积为多少______ mL?
(4)将一定质量的Mg和Al混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示计算:
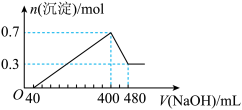
①酸的物质的量浓度为多少______ ?
②若将上述混合物中等物质的量的Mg和Al分别与稀硫酸充分反应,产生的气体通入相同条件下恒容的甲乙两密闭容器中,求甲乙两容器内的压强比为多少______ ?
(1)将200mL3mol/L的Al2(SO4)3溶液稀释至500mL,求稀释后硫酸根的浓度为多少
(2)将K2SO4和Al2(SO4)3和KAl(SO4)2三种混合溶液加H2SO4酸化。测得c(SO
 )=1.05 mol/L, c(Al3+)=0.55 mol/L,c(H+)=0.10mol/L(假设H2SO4完全电离为H+和SO
)=1.05 mol/L, c(Al3+)=0.55 mol/L,c(H+)=0.10mol/L(假设H2SO4完全电离为H+和SO ),则c(K+)为多少
),则c(K+)为多少 (3)Fe、Al混合物共0.2mol,用盐酸将其完全溶解,放出标准状况下5.6L气体,然后再滴入4mol/L的NaOH溶液,请计算:
①求该混合物中Fe、Al的物质的量
②若该Fe、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Fe2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积为多少
(4)将一定质量的Mg和Al混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示计算:

①酸的物质的量浓度为多少
②若将上述混合物中等物质的量的Mg和Al分别与稀硫酸充分反应,产生的气体通入相同条件下恒容的甲乙两密闭容器中,求甲乙两容器内的压强比为多少
您最近半年使用:0次
填空题
|
困难
(0.15)
名校
【推荐2】铝与NO3-在酸性或碱性条件下均可反应,回答下列问题:
(1)为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,完善并配平该反应:__ Al +___NO3- + ___OH- = ___ _________+ ____N2↑ + ____H2O。每消耗1mol NO3-,转移的电子数目为_____ 。
(2)某同学取一定质量的铁铝合金与100mLxmol/L稀硝酸充分反应,反应过程中没有气体放出。在反应结束后的溶液中,逐滴加入4 mol/L NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如图所示。
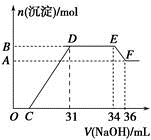
①写出EF段发生反应的离子方程式_________________________________________ 。
② C点对应的溶液中含有的阳离子除Na+外,还含有___________________________ 。
③ x=_________ 。
④铁铝合金中铝的物质的量分数为______________________ 。
(1)为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,完善并配平该反应:
(2)某同学取一定质量的铁铝合金与100mLxmol/L稀硝酸充分反应,反应过程中没有气体放出。在反应结束后的溶液中,逐滴加入4 mol/L NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如图所示。

①写出EF段发生反应的离子方程式
② C点对应的溶液中含有的阳离子除Na+外,还含有
③ x=
④铁铝合金中铝的物质的量分数为
您最近半年使用:0次
填空题
|
困难
(0.15)
【推荐3】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,最低可以还原到-3价。某同学取一定量的铁铝合金与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4 mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:

(1)请写出该合金中铁与硝酸反应的离子方程式_______________ 。
(2)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为_______________ 。
(3)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为___________ 。
(4)B与A的差值为__________ mol。
(5)B点对应的沉淀的物质的量为_______ mol,C点对应的氢氧化钠溶液的体积为______ mL。

(1)请写出该合金中铁与硝酸反应的离子方程式
(2)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为
(3)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为
(4)B与A的差值为
(5)B点对应的沉淀的物质的量为
您最近半年使用:0次
填空题
|
困难
(0.15)
解题方法
【推荐1】将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)
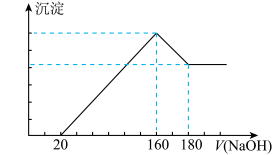
求:
(1)加入NaOH溶液0~20mL过程中反应的离子方程式为____________________ ;沉淀中Al(OH)3的质量为____________ g。
(2)合金中Mg的质量为___________ ;所用HCl的物质的量浓度为___________ mol/L。

求:
(1)加入NaOH溶液0~20mL过程中反应的离子方程式为
(2)合金中Mg的质量为
您最近半年使用:0次
填空题
|
困难
(0.15)
【推荐2】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,最低可以还原到-3价。某同学取一定量的铁铝合金与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4 mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:

(1)请写出该合金中铁与硝酸反应的离子方程式_______________ 。
(2)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为_______________ 。
(3)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为___________ 。
(4)B与A的差值为__________ mol。
(5)B点对应的沉淀的物质的量为_______ mol,C点对应的氢氧化钠溶液的体积为______ mL。

(1)请写出该合金中铁与硝酸反应的离子方程式
(2)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为
(3)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为
(4)B与A的差值为
(5)B点对应的沉淀的物质的量为
您最近半年使用:0次
填空题
|
困难
(0.15)
【推荐3】准确称取6.00克铝土矿样品(含Al2O3、Fe2O3、SiO2),将其放入盛有100毫升H2SO4溶液的烧杯中,充分反应后滤出沉淀物。在滤液X中加入10摩/升的NaOH溶液,产生的沉淀的质量w与所加NaOH溶液的体积V之间有如图所示的关系。求:
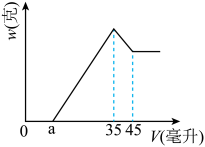
(1)分析图象可知滤液X中所含有的溶质成分为_____ (填化学式)。
(2)H2SO4溶液的物质的量浓度是__________ ?
(3)图中a值为2.3毫升时,铝土矿样品中Fe2O3的质量分数_________________ 。
(4)a值的变化范围是____________________ ?

(1)分析图象可知滤液X中所含有的溶质成分为
(2)H2SO4溶液的物质的量浓度是
(3)图中a值为2.3毫升时,铝土矿样品中Fe2O3的质量分数
(4)a值的变化范围是
您最近半年使用:0次



