已知: Fe3O4能与高浓度盐酸反应,与低浓度盐酸不反应。某研究性学习小组通过实验探究,欲确定某地所产青砖中是否含有FeO、Fe3O4和Fe2O3, 并测定青砖中铁元素的质量分数。回答下列问题:
(一)实验准备
(l)本实验探究部分需在无氧环境下进行,故配制溶液的蒸馏水常用_____ 法除去溶解氧。该实验所用试管中均需充满CO2,请选用下列装置制取干燥纯净的CO2气体,连接顺序为:
a
_____  h、i(后续装置略去)。
h、i(后续装置略去)。
(二)探究青砖中是否含有Fe3O4和Fe2O3
(2)步骤二中,若不取下试管上的塞子,又不因盐酸加入导致试管内压强增大,使用注射器实现上述目的的操作方法为__________ 。
(3)Fe3O4与高浓度盐酸反应的离子方程式为________ 。
(4)用离子方程式表示溶液变红的原因__________ 。
(5)根据上述现象,可初步得出该青砖样品中所含铁的氧化物为________ (填化学式)
(三)探究青砖中是否含有FeO
(6)另取一支充满CO2气体的试管,注入1mL上述试管1的上层清液和数滴K3[Fe(CN)6]溶液,若实验现象为_______ ,说明青砖中含有FeO。
(四)青砖样品中铁元素质量分数的测定
称取m1g 青砖细粉,用足量12mol/L盐酸充分溶解、过滤、洗涤(第一次)。将滤液(包括洗涤滤渣后的溶液)依次与足量的新制氯水、氢氧化钠溶液充分反应,过滤、洗涤(第二次),将沉淀灼烧至恒重,冷却后称得残留固体质量为m2g。
(7)若青砖中其它成分对实验无影响,则测得铁元素的质量分数为____ (填含m1、m2的表达式);该实验若未进行第一次洗涤,则测得铁元素的质量分数______ (填“偏高”、“偏低”或“无影响”)。
(一)实验准备
(l)本实验探究部分需在无氧环境下进行,故配制溶液的蒸馏水常用
a

 h、i(后续装置略去)。
h、i(后续装置略去)。
(二)探究青砖中是否含有Fe3O4和Fe2O3
| 组别 步骤及现象 | 第一组 | 第二组 | 第三组 |
| 步骤一 | 取试管l 、2 、3①分别加入2g青砖细粉②分别通入CO2气体至充满,用户塞子塞紧 | ||
| 步骤二 | 向试管1中注入10mL 3 mol/L盐酸,充分振荡 | 向试管2中注入10mL 6 mol/L盐酸,充分振荡 | 向试管3中注入10mL 12 mol/L盐酸,充分振荡 |
| 步骤三 | 取试管1、2、3中的上层清液各1mL于另三支试管中,再分别注入0.2mL相同浓度的KSCN溶液,振荡 | ||
| 步骤三的实验现象 | 溶液变红 且第一、二两组溶液颜色深浅相同 | 溶液变红 且较第一、二两组颜色更深 | |
(2)步骤二中,若不取下试管上的塞子,又不因盐酸加入导致试管内压强增大,使用注射器实现上述目的的操作方法为
(3)Fe3O4与高浓度盐酸反应的离子方程式为
(4)用离子方程式表示溶液变红的原因
(5)根据上述现象,可初步得出该青砖样品中所含铁的氧化物为
(三)探究青砖中是否含有FeO
(6)另取一支充满CO2气体的试管,注入1mL上述试管1的上层清液和数滴K3[Fe(CN)6]溶液,若实验现象为
(四)青砖样品中铁元素质量分数的测定
称取m1g 青砖细粉,用足量12mol/L盐酸充分溶解、过滤、洗涤(第一次)。将滤液(包括洗涤滤渣后的溶液)依次与足量的新制氯水、氢氧化钠溶液充分反应,过滤、洗涤(第二次),将沉淀灼烧至恒重,冷却后称得残留固体质量为m2g。
(7)若青砖中其它成分对实验无影响,则测得铁元素的质量分数为
更新时间:2017-04-15 20:59:47
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀。

(1)检验W溶液中金属阳离子所用试剂为_______ (填化学式);
(2)H在潮湿空气中变成M的现象是_______ ,发生反应的化学方程式为_______ ;
(3)A和水反应生成B和C的离子方程式为_______ ;在标准状况下生成11.2 LC气体时,转移电子的个数为_______ NA(用阿伏加德罗常数NA表示);
(4)D中加入盐酸发生反应的离子方程式为_______ 。

(1)检验W溶液中金属阳离子所用试剂为
(2)H在潮湿空气中变成M的现象是
(3)A和水反应生成B和C的离子方程式为
(4)D中加入盐酸发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】黄铜矿( )是冶炼铜及制备铁的氧化物的重要矿藏,常含有微量的金、银等。
)是冶炼铜及制备铁的氧化物的重要矿藏,常含有微量的金、银等。
(1)利用焰色反应原理即可制作五彩缤纷的节日烟花,亦可鉴定某些金属元素。黄铜矿中铜的焰色反应为_______ 。
(2)如图所示是以黄铜矿为主要原料生产铜、铁红(氧化铁)颜料的工艺流程:

①反应Ⅰ的离子方程式为_______ 。
②有大量 存在时,
存在时, 可将
可将 还原成
还原成 。
。 要缓慢滴加到溶液中的原因是
要缓慢滴加到溶液中的原因是_______ 。
③反应Ⅰ~Ⅴ中属于非氧化还原反应的是反应_______ 。已知 在反应Ⅴ中发生自身氧化还原反应,歧化为
在反应Ⅴ中发生自身氧化还原反应,歧化为 和
和 ,由此可推知溶液A中的溶质为
,由此可推知溶液A中的溶质为_______ (填化学式)。
(3)含 的废水对环境造成严重污染,常用新制的氢氧化铁沉淀与之作用形成
的废水对环境造成严重污染,常用新制的氢氧化铁沉淀与之作用形成 沉淀而除去,相同温度下溶度积:
沉淀而除去,相同温度下溶度积:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)在酸性、有氧条件下,一种叫Thibacillusferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程中发生反应的离子方程式为_______ 。
(5)将一定量的铁红溶于160 5
5 盐酸中,再加入足量铁粉,待反应结束后共收集到气体2.24L(标准状况),经检测,溶液中无
盐酸中,再加入足量铁粉,待反应结束后共收集到气体2.24L(标准状况),经检测,溶液中无 ,则参加反应的铁粉的质量为
,则参加反应的铁粉的质量为_______ 。
 )是冶炼铜及制备铁的氧化物的重要矿藏,常含有微量的金、银等。
)是冶炼铜及制备铁的氧化物的重要矿藏,常含有微量的金、银等。(1)利用焰色反应原理即可制作五彩缤纷的节日烟花,亦可鉴定某些金属元素。黄铜矿中铜的焰色反应为
(2)如图所示是以黄铜矿为主要原料生产铜、铁红(氧化铁)颜料的工艺流程:

①反应Ⅰ的离子方程式为
②有大量
 存在时,
存在时, 可将
可将 还原成
还原成 。
。 要缓慢滴加到溶液中的原因是
要缓慢滴加到溶液中的原因是③反应Ⅰ~Ⅴ中属于非氧化还原反应的是反应
 在反应Ⅴ中发生自身氧化还原反应,歧化为
在反应Ⅴ中发生自身氧化还原反应,歧化为 和
和 ,由此可推知溶液A中的溶质为
,由此可推知溶液A中的溶质为(3)含
 的废水对环境造成严重污染,常用新制的氢氧化铁沉淀与之作用形成
的废水对环境造成严重污染,常用新制的氢氧化铁沉淀与之作用形成 沉淀而除去,相同温度下溶度积:
沉淀而除去,相同温度下溶度积:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)在酸性、有氧条件下,一种叫Thibacillusferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程中发生反应的离子方程式为
(5)将一定量的铁红溶于160
 5
5 盐酸中,再加入足量铁粉,待反应结束后共收集到气体2.24L(标准状况),经检测,溶液中无
盐酸中,再加入足量铁粉,待反应结束后共收集到气体2.24L(标准状况),经检测,溶液中无 ,则参加反应的铁粉的质量为
,则参加反应的铁粉的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
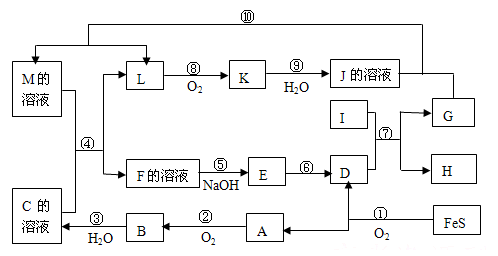
【推荐3】物质A~M在一定条件下的转化关系如图(部分产物及反应条件未列出).其中,I是既能与强酸反应生成氢气又能与强碱反应生成氢气的金属,K是一种红棕色气体,D的俗名叫铁红,A是形成酸雨的主要气体.
请填写下列空白:
(1)推导出下列物质的化学式:C:_____ E:_____
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是_______________ (填写序号).
(3)反应④的离子方程式是:______________________ .
(4)将化合物D 与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4 (高铁酸钾),同时还生成KNO2和H2O.该反应的化学方程式是:_______________________ .
请填写下列空白:
(1)推导出下列物质的化学式:C:
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是
(3)反应④的离子方程式是:
(4)将化合物D 与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4 (高铁酸钾),同时还生成KNO2和H2O.该反应的化学方程式是:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
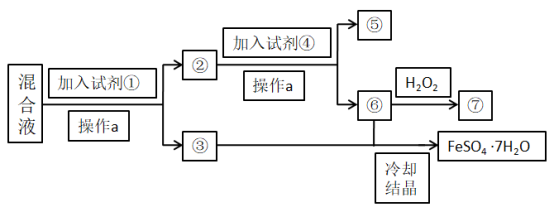
【推荐1】某小组的同学模拟工业废水的处理,设计了如图流程,混合液中含有大量FeSO4和较多的Cu2+,小组希望从中回收FeSO4•7H2O固体和Cu单质,请回答下列问题:
(1)请写出下列标号所代表的的物质(化学式)或操作方法:
①____ ;④___ ;操作a___ 。
(2)鉴别溶液⑦中的金属阳离子所需的试剂是___ ,现象是___ 。请写出流程中酸性条件下⑥→⑦步骤的离子方程式:___ 。
(3)取少量③中的溶液于试管中,滴加NaOH溶液,可观察到的现象是___ ,此过程涉及的氧化还原反应的化学方程式为___ 。
(4)铁红是一种常见的红色颜料,请设计在实验室中由FeCl3溶液制备铁红的实验方案:____ 。

(1)请写出下列标号所代表的的物质(化学式)或操作方法:
①
(2)鉴别溶液⑦中的金属阳离子所需的试剂是
(3)取少量③中的溶液于试管中,滴加NaOH溶液,可观察到的现象是
(4)铁红是一种常见的红色颜料,请设计在实验室中由FeCl3溶液制备铁红的实验方案:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】FeCl3是重要的化工原料,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解
(1)制备无水氯化铁
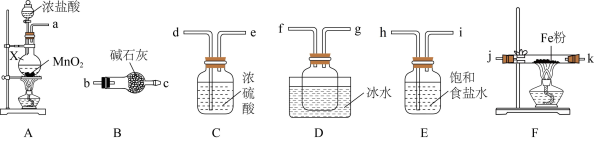
①仪器X的名称为______________ 。
②装置的连接顺序为a→______ → j,k →________ (按气流方向,用小写字母表示)。
③实验结束后,取少量F中的固体加水溶解,经检测发现溶液中含有Fe2+,其原因为____ 。
(2)探究FeCl3与SO2的反应
已知反应体系中存在下列两种化学变化:
(i) Fe3+与SO2发生络合反应生成Fe(SO2)62+(红棕色);
(ii) Fe3+与SO2发生氧化还原反应,其离子方程式为①____________
④实验结论:反应(i)、(ii)的活化能大小关系是:E(i)____ E(ii)(填“>”、 “<”或“=”,下同),平衡常数大小关系是:K(i)__________ K(ii)。
⑤另取5 mL l mol L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是
L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是____ 。
(1)制备无水氯化铁

①仪器X的名称为
②装置的连接顺序为a→
③实验结束后,取少量F中的固体加水溶解,经检测发现溶液中含有Fe2+,其原因为
(2)探究FeCl3与SO2的反应
已知反应体系中存在下列两种化学变化:
(i) Fe3+与SO2发生络合反应生成Fe(SO2)62+(红棕色);
(ii) Fe3+与SO2发生氧化还原反应,其离子方程式为①
| 步骤 | 现象 | 结论 |
| Ⅰ.取5 mL1 mol⋅L−1 FeCl3溶液于试管中,通入SO2至饱和 | 溶液很快由黄色变为红棕色 | |
| Ⅱ.用激光笔照射步骤Ⅰ中的红棕色溶液 | 溶液中无明显光路 | ②红棕色物质不是 |
| Ⅲ将步骤Ⅰ中的溶液静置 | 1小时后,溶液逐渐变为浅绿色 | |
| IV.向步骤Ⅲ中溶液加入2滴K3[Fe(CN)6]溶液 | ③ | 溶液中含有Fe2+ |
⑤另取5 mL l mol
 L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是
L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某铁矿石烧渣含 、
、 和
和 ,以该烧渣为原料制取
,以该烧渣为原料制取 的流程如下:
的流程如下:
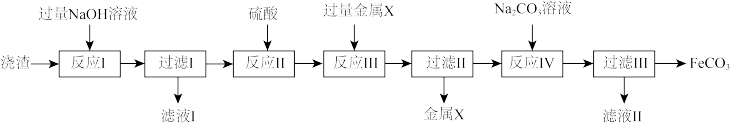
已知 是难溶于水的酸性氧化物,
是难溶于水的酸性氧化物, 是难溶于水的白色固体。
是难溶于水的白色固体。
(1)反应Ⅰ中 所发生反应的离子方程式为
所发生反应的离子方程式为____________ 。
(2)选择最适合的金属 ,写出反应Ⅲ的离子方程式:
,写出反应Ⅲ的离子方程式:____________ 。
(3)检验反应Ⅲ已经完全的方法是____________ 。
(4)反应Ⅳ中当将过滤Ⅱ的滤液缓慢滴加到 溶液中,会得到两种白色沉淀混合物,其中一种很快变成灰绿色,最终变成红褐色。
溶液中,会得到两种白色沉淀混合物,其中一种很快变成灰绿色,最终变成红褐色。
①白色沉淀中除 外,还含有
外,还含有____________ (填化学式),生成该沉淀是因为 溶液中含有
溶液中含有____________ (填离子符号)。
②写出沉淀变色时所发生反应的化学方程式:____________ 。
 、
、 和
和 ,以该烧渣为原料制取
,以该烧渣为原料制取 的流程如下:
的流程如下:
已知
 是难溶于水的酸性氧化物,
是难溶于水的酸性氧化物, 是难溶于水的白色固体。
是难溶于水的白色固体。(1)反应Ⅰ中
 所发生反应的离子方程式为
所发生反应的离子方程式为(2)选择最适合的金属
 ,写出反应Ⅲ的离子方程式:
,写出反应Ⅲ的离子方程式:(3)检验反应Ⅲ已经完全的方法是
(4)反应Ⅳ中当将过滤Ⅱ的滤液缓慢滴加到
 溶液中,会得到两种白色沉淀混合物,其中一种很快变成灰绿色,最终变成红褐色。
溶液中,会得到两种白色沉淀混合物,其中一种很快变成灰绿色,最终变成红褐色。①白色沉淀中除
 外,还含有
外,还含有 溶液中含有
溶液中含有②写出沉淀变色时所发生反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】食品膨松剂通常应用于糕点、饼干、面包、馒头等以小麦粉为主的焙烤食品的制作过程中,使其体积膨胀与结构疏松。某食品膨松剂起作用的物质为 ,某化学兴趣小组对该食品膨松剂进行了研究,实验装置如图所示。
,某化学兴趣小组对该食品膨松剂进行了研究,实验装置如图所示。
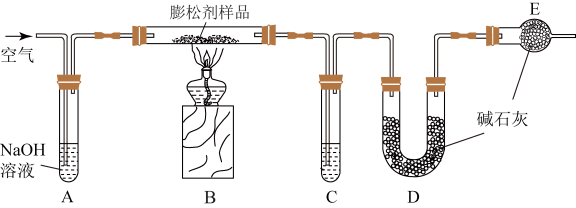
已知:碱石灰是固体氢氧化钠和氧化钙的混合物。
请回答下列问题:
(1)装置A中NaOH溶液的作用是除去空气中的___________ ,装置C内所盛试剂是___________ 。
(2)停止加热后,应继续通入空气一段时间,其目的是___________ 。测定实验前后装置___________ (填序号)的质量,其质量差(m)即为样品受热产生的二氧化碳气体的质量。
(3)装置E的作用是___________ ,若没有装置E,测定的结果将___________ (填“偏高”“偏低”或“无影响”);若没有装置A,而是在装置B的左侧用橡皮塞封闭,实验结果将___________ (填“偏高”“偏低”或“无影响”)。
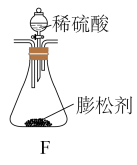
(4)充分加热后,测得装置D的质量增加了8.8g。若将装置B换为装置F进行实验(所取膨松剂样品质量相同)。不考虑导致误差的因素,则装置D的质量将增加___________ g。
(5)分解产物 是重要的化工原料,为研究其性质进行了下列实验:
是重要的化工原料,为研究其性质进行了下列实验:
分别取少量 溶液,
溶液,
①与碱反应:逐滴滴加澄清石灰水,现象为___________ 。
②与盐反应:逐滴滴加X溶液,产生白色沉淀,则X可能为___________ (填化学式)。
③与酸反应:逐滴滴加稀盐酸,开始没有气泡产生,反应产生两种盐,推测两种盐的化学式为___________ 、___________ 。
(6)取 与
与 的混合物进行下列三组实验,其中能测定
的混合物进行下列三组实验,其中能测定 的质量分数的是
的质量分数的是___________ (填序号)。
A.充分加热,质量减少bg
B.与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体
C.与足量稀硫酸充分反应,逸出气体用氯化钙溶液吸收,增重6g
 ,某化学兴趣小组对该食品膨松剂进行了研究,实验装置如图所示。
,某化学兴趣小组对该食品膨松剂进行了研究,实验装置如图所示。

已知:碱石灰是固体氢氧化钠和氧化钙的混合物。
请回答下列问题:
(1)装置A中NaOH溶液的作用是除去空气中的
(2)停止加热后,应继续通入空气一段时间,其目的是
(3)装置E的作用是
(4)充分加热后,测得装置D的质量增加了8.8g。若将装置B换为装置F进行实验(所取膨松剂样品质量相同)。不考虑导致误差的因素,则装置D的质量将增加
(5)分解产物
 是重要的化工原料,为研究其性质进行了下列实验:
是重要的化工原料,为研究其性质进行了下列实验:分别取少量
 溶液,
溶液,①与碱反应:逐滴滴加澄清石灰水,现象为
②与盐反应:逐滴滴加X溶液,产生白色沉淀,则X可能为
③与酸反应:逐滴滴加稀盐酸,开始没有气泡产生,反应产生两种盐,推测两种盐的化学式为
(6)取
 与
与 的混合物进行下列三组实验,其中能测定
的混合物进行下列三组实验,其中能测定 的质量分数的是
的质量分数的是A.充分加热,质量减少bg
B.与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体
C.与足量稀硫酸充分反应,逸出气体用氯化钙溶液吸收,增重6g
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】我国国家标准(GB2760)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。

(1)仪器A的名称是__________ ,水通入A的进口为________ 。
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为_____________________________ 。
(3)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的______ ;若滴定终点时溶液的pH=8.8,则选择的指示剂为______ ;若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)__________ (①=10 mL,②=40 mL,③<10 mL,④>40 mL)。
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为:________ g·L-1。
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施:____________ 。
(6)常温下,用一定量的NaOH溶液吸收逸出的SO2气体,若吸收后的吸收液恰好呈中性,下列关于该吸收液的说法正确的是______________________ 。

(1)仪器A的名称是
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为
(3)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为:
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施:
(6)常温下,用一定量的NaOH溶液吸收逸出的SO2气体,若吸收后的吸收液恰好呈中性,下列关于该吸收液的说法正确的是
| A.c(Na+)=c(HSO3-)+2c(SO32-) |
| B.c(Na+)>c(HSO3-)=c(SO32-)>c(H+) = c(OH-) |
| C.2c(Na+)=3c(H2SO3)+3c(HSO3-)+3c(SO32-) |
| D.c(Na+)>c(HSO3- ) + c(SO32-) +c(H2SO3) |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上,处理低品位黄铜矿[二硫化亚铁铜(CuFeS2)含量较低]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾(FeSO4•7H2O)和胆矾(CuSO4•5H2O)。相关流程如图。
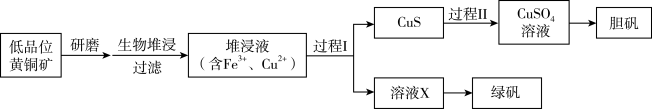
已知:①生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如表。
(1)生物堆浸前,需先将矿石进行研磨,目的是____ 。
(2)生物堆浸过程的反应在T.f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为:CuFeS2+4H++O2 Cu2++Fe2++2S+2H2O,第二阶段的反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为
Cu2++Fe2++2S+2H2O,第二阶段的反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为____ 。
(3)结合已知推断:生物堆浸过程中,应控制溶液的pH在____ 范围内。
(4)过程I中,加入Na2S2O3固体会还原堆浸液中的Fe3+,得到溶液X。为检验溶液X中Fe2+,可取少量溶液X,向其中加入____ 试剂(填试剂的化学式),观察反应现象。
(5)过程II中,用H2O2和稀硫酸处理,CuS完全反应,过滤生成的沉淀物后,可得CuSO4溶液。用离子方程式表示H2O2的作用是____ 。
(6)绿矾的纯度可通过KMnO4滴定法测定。取mg绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为cmol/L的KMnO4溶液滴定。至恰好完全反应时,消耗KMnO4溶液的体积为VmL。绿矾晶体质量分数的表达式为___ 。(已知:FeSO4•7H2O的摩尔质量为278g/mol)

已知:①生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH1.0~6.0范围内可保持活性。
②金属离子沉淀的pH如表。
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀时的pH | 1.5 | 4.2 | 6.3 |
| 完全沉淀时的pH | 2.8 | 6.7 | 8.3 |
(1)生物堆浸前,需先将矿石进行研磨,目的是
(2)生物堆浸过程的反应在T.f细菌的作用下进行,主要包括两个阶段,第一阶段的反应为:CuFeS2+4H++O2
 Cu2++Fe2++2S+2H2O,第二阶段的反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为
Cu2++Fe2++2S+2H2O,第二阶段的反应为Fe2+继续被氧化转变成Fe3+,反应的离子方程式为(3)结合已知推断:生物堆浸过程中,应控制溶液的pH在
(4)过程I中,加入Na2S2O3固体会还原堆浸液中的Fe3+,得到溶液X。为检验溶液X中Fe2+,可取少量溶液X,向其中加入
(5)过程II中,用H2O2和稀硫酸处理,CuS完全反应,过滤生成的沉淀物后,可得CuSO4溶液。用离子方程式表示H2O2的作用是
(6)绿矾的纯度可通过KMnO4滴定法测定。取mg绿矾晶体,加适量稀硫酸溶解。用物质的量浓度为cmol/L的KMnO4溶液滴定。至恰好完全反应时,消耗KMnO4溶液的体积为VmL。绿矾晶体质量分数的表达式为
您最近一年使用:0次
【推荐1】某化学实验小组用酸性 KMnO4溶液和草酸(H2C2O4)溶液反应,研究外界条件对反应速率的影响,实验操作及现象如下:
(1)补全高锰酸钾与草酸反应的离子方程式:_____
H2C2O4+ MnO + H+═ Mn2++ +
+ H+═ Mn2++ +
(2)由实验Ⅰ、Ⅱ可得出的结论是_____ 。
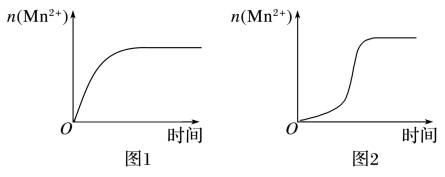
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息对于实验Ⅱ中 80s 后溶液颜色迅速变浅的原因,该小组提出了新的猜想,并继续进行实验探究。
Ⅰ.该小组同学提出的猜想是_____ 。
Ⅱ.请你帮助该小组完成实验方案,并填写表中空白。
【实验内容及记录】(H2C2O4溶液足量)
若该小组同学提出的猜想成立,则 编号2中加入的固体是_____
t___ (“>”“<”“=”) 200s。计算此时实验1中高锰酸钾的的反应速率____ (忽略10滴硫酸的体积)
编号 | 实验操作 | 实验现象 |
Ⅰ | 向一支试管中先加入5 mL 0.01 mol/L 酸性KMnO4溶液,再加入1 滴3 mol/L 硫酸和9 滴蒸馏水,最后加入5 mL 0.1 mol/L草酸溶液 | 前10 min 内溶液紫色无明显变化,后颜色加速变浅,30 min 后几乎变为无色 |
Ⅱ | 向另一支试管中先加入5 mL 0.01 mol/L酸性KMnO4溶液,再加入10 滴3 mol/L硫酸,最后加入5 mL 0.1 mol/L 草酸溶液 | 80 s内溶液紫色无明显变化,后颜色迅速变浅,约200 s后几乎变为无色 |
H2C2O4+ MnO
 + H+═ Mn2++ +
+ H+═ Mn2++ + (2)由实验Ⅰ、Ⅱ可得出的结论是

(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息对于实验Ⅱ中 80s 后溶液颜色迅速变浅的原因,该小组提出了新的猜想,并继续进行实验探究。
Ⅰ.该小组同学提出的猜想是
Ⅱ.请你帮助该小组完成实验方案,并填写表中空白。
【实验内容及记录】(H2C2O4溶液足量)
编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 | ||
0.1 mol/L H2C2O4溶液 | 0.01 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | |||
1 | 5.0 | 5.0 | 10 滴 | 无 | 200s |
2 | 5.0 | 5.0 | 10 滴 | 有 | t |
t
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】研究小组探究 与水的反应。向
与水的反应。向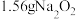 粉末中加入40mL水(密度为
粉末中加入40mL水(密度为 ),充分反应后得溶液A(溶液体积变化忽略不计),进行实验。
),充分反应后得溶液A(溶液体积变化忽略不计),进行实验。
实验1:向2mL溶液A中滴入1滴酚酞溶液,溶液变红,20s后褪色。
(1) 固体的颜色为
固体的颜色为___________ ,溶液A中溶质NaOH的质量分数为___________ (保留三位有效数字)。
(2)对实验1中溶液红色褪去的原因进行探究。
【查阅资料】
资料: 是一种在碱性条件下不稳定、具有漂白性的物质。
是一种在碱性条件下不稳定、具有漂白性的物质。
【提出猜想】
猜想1: 与
与 反应可能生成了
反应可能生成了 。
。
猜想2:生成的NaOH浓度太大。
【设计并进行实验】
①实验2:向2mL溶液A中加入黑色粉末___________ (填化学式),快速产生了能使带火星木条复燃的气体。
②实验3:向2mL质量分数为___________ %的NaOH溶液中滴入1滴酚酞溶液,溶液变红,10min后溶液褪色。向褪色的溶液中加入一定量的水,溶液变红。
【得出结论】
(3)由以上实验可得出的结论是___________ 。
【反思与评价】
(4)分析实验结果可知, 与
与 反应的化学方程式如果分两步书写,应为
反应的化学方程式如果分两步书写,应为___________ ,___________ ,但课本上没有写出中间产物 ,可能的原因是
,可能的原因是___________ 。
 与水的反应。向
与水的反应。向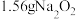 粉末中加入40mL水(密度为
粉末中加入40mL水(密度为 ),充分反应后得溶液A(溶液体积变化忽略不计),进行实验。
),充分反应后得溶液A(溶液体积变化忽略不计),进行实验。实验1:向2mL溶液A中滴入1滴酚酞溶液,溶液变红,20s后褪色。
(1)
 固体的颜色为
固体的颜色为(2)对实验1中溶液红色褪去的原因进行探究。
【查阅资料】
资料:
 是一种在碱性条件下不稳定、具有漂白性的物质。
是一种在碱性条件下不稳定、具有漂白性的物质。【提出猜想】
猜想1:
 与
与 反应可能生成了
反应可能生成了 。
。猜想2:生成的NaOH浓度太大。
【设计并进行实验】
①实验2:向2mL溶液A中加入黑色粉末
②实验3:向2mL质量分数为
【得出结论】
(3)由以上实验可得出的结论是
【反思与评价】
(4)分析实验结果可知,
 与
与 反应的化学方程式如果分两步书写,应为
反应的化学方程式如果分两步书写,应为 ,可能的原因是
,可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某实验室小组偶然发现将镁条插入饱和NaHCO3溶液中,镁条表面出现大量气泡。为了探究产生此现象的原因,该小组设计实验探究如下:
(1)用固体NaHCO3配置饱和NaHCO3溶液的操作过程 。
饱和NaHCO3溶液pH=8.4,用离子方程式表示 。
(2)请完成以下实验设计(镁条已擦去氧化膜且表面积大致相同。表中不要留空格):
(3)对于反应②中产生的气体(不考虑水蒸气),请你完成假设二和假设三:
假设一:只有CO2;假设二:只有 ;假设三:
为检验其中是否含有CO2,写出实验步骤和结论。
(1)用固体NaHCO3配置饱和NaHCO3溶液的操作过程 。
饱和NaHCO3溶液pH=8.4,用离子方程式表示 。
(2)请完成以下实验设计(镁条已擦去氧化膜且表面积大致相同。表中不要留空格):
序号 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 将镁条投入5ml蒸馏水 | 微量气泡 | |
| 2 | 将镁条投入5ml饱和NaHCO3溶液中 | Mg与NaHCO3溶液剧烈反应 | |
| 3 | 将镁条投入5ml pH= NaOH溶液中 | 现象不明显 | Mg与NaOH溶液较难反应 |
假设一:只有CO2;假设二:只有 ;假设三:
为检验其中是否含有CO2,写出实验步骤和结论。
实验步骤 | 想象和结论 |
| 大试管中加入擦去氧化膜的镁条 |
您最近一年使用:0次



