FeCl3是重要的化工原料,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解
(1)制备无水氯化铁
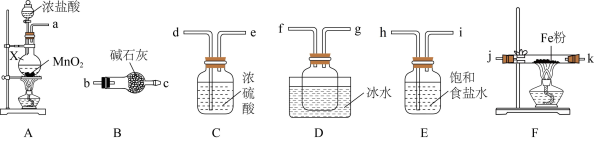
①仪器X的名称为______________ 。
②装置的连接顺序为a→______ → j,k →________ (按气流方向,用小写字母表示)。
③实验结束后,取少量F中的固体加水溶解,经检测发现溶液中含有Fe2+,其原因为____ 。
(2)探究FeCl3与SO2的反应
已知反应体系中存在下列两种化学变化:
(i) Fe3+与SO2发生络合反应生成Fe(SO2)62+(红棕色);
(ii) Fe3+与SO2发生氧化还原反应,其离子方程式为①____________
④实验结论:反应(i)、(ii)的活化能大小关系是:E(i)____ E(ii)(填“>”、 “<”或“=”,下同),平衡常数大小关系是:K(i)__________ K(ii)。
⑤另取5 mL l mol L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是
L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是____ 。
(1)制备无水氯化铁

①仪器X的名称为
②装置的连接顺序为a→
③实验结束后,取少量F中的固体加水溶解,经检测发现溶液中含有Fe2+,其原因为
(2)探究FeCl3与SO2的反应
已知反应体系中存在下列两种化学变化:
(i) Fe3+与SO2发生络合反应生成Fe(SO2)62+(红棕色);
(ii) Fe3+与SO2发生氧化还原反应,其离子方程式为①
| 步骤 | 现象 | 结论 |
| Ⅰ.取5 mL1 mol⋅L−1 FeCl3溶液于试管中,通入SO2至饱和 | 溶液很快由黄色变为红棕色 | |
| Ⅱ.用激光笔照射步骤Ⅰ中的红棕色溶液 | 溶液中无明显光路 | ②红棕色物质不是 |
| Ⅲ将步骤Ⅰ中的溶液静置 | 1小时后,溶液逐渐变为浅绿色 | |
| IV.向步骤Ⅲ中溶液加入2滴K3[Fe(CN)6]溶液 | ③ | 溶液中含有Fe2+ |
⑤另取5 mL l mol
 L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是
L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是
更新时间:2020-11-24 19:09:20
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某同学欲验证炭与浓硫酸反应产物的性质。现已将装置如图连接,请回答下列问题。

(1)烧瓶中发生反应的化学反应方程式是_______ 。
(2)实验中两次使用到品红溶液,其目的不同。A的使用目的是_______ ,通过洗气瓶C中无现象和_______ 的现象,证明反应有_______ (填化学式)生成。
(3)洗气瓶B中溶液颜色变浅,说明炭与浓硫酸反应的产物之一_______ (填化学式)具有_______ 的性质。
(4)实验完成后,取出洗气瓶A中的无色溶液于试管中,加热,可观察到_______ 。

(1)烧瓶中发生反应的化学反应方程式是
(2)实验中两次使用到品红溶液,其目的不同。A的使用目的是
(3)洗气瓶B中溶液颜色变浅,说明炭与浓硫酸反应的产物之一
(4)实验完成后,取出洗气瓶A中的无色溶液于试管中,加热,可观察到
您最近一年使用:0次
【推荐2】硫的氧化物、氮的氧化物是常见的大气污染物。
(1)酸雨是降水呈酸性(pH小于5.6)的统称,个别地方甚至低于2.1(食醋的pH=3)。引起酸雨的罪魁祸首是大气中的硫的氧化物和氮的氧化物,它们的主要来源是煤和石油的燃烧。
①汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排放量约为5×107 kg。NO2溶于水生成_____________ (写名称)和NO。
②为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫元素进行固化处理,对废气中的氮的氧化物用__________ 吸收,写出NO2与之反应的离子方程式____________________________ 。
(2)某化学兴趣小组选用下图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。

①若原料气从左向右流时,上述装置连接的顺序是:原料气→ → → → → (填字母)。_________
②装置②中发生反应的离子方程式为:___________________________________________ ;当装置②中出现_____________________________ 现象时,立即停止通气。
③你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是__________ 。
A.酸性KMnO4溶液 B.NaOH溶液 C.溴水 D.氨水
(1)酸雨是降水呈酸性(pH小于5.6)的统称,个别地方甚至低于2.1(食醋的pH=3)。引起酸雨的罪魁祸首是大气中的硫的氧化物和氮的氧化物,它们的主要来源是煤和石油的燃烧。
①汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年排放量约为5×107 kg。NO2溶于水生成
②为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫元素进行固化处理,对废气中的氮的氧化物用
(2)某化学兴趣小组选用下图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。

①若原料气从左向右流时,上述装置连接的顺序是:原料气→ → → → → (填字母)。
②装置②中发生反应的离子方程式为:
③你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是
A.酸性KMnO4溶液 B.NaOH溶液 C.溴水 D.氨水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2并完成相关性质探究。
(1)有同学认为制得的SO2中可能混有两种杂质气体(不考虑水蒸气)。为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。

①为验证并吸收SO2,装置B中加入的试剂为____ 。
②装置D中加入的试剂为____ 。
③装置G中可能出现的现象为____ 。
④装置H的作用为____ 。
⑤有同学认为应该在D装置和E装置之间再增加一个____ 装置,以避免引起实验安全问题。
(2)兴趣小组设计如图装置验证二氧化硫的化学性质。

为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去
方案Ⅱ:向第二份溶液加入BaCl2浴液,产生白色沉淀
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成
上述方案中合理的是____ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为____ 。
(1)有同学认为制得的SO2中可能混有两种杂质气体(不考虑水蒸气)。为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。

①为验证并吸收SO2,装置B中加入的试剂为
②装置D中加入的试剂为
③装置G中可能出现的现象为
④装置H的作用为
⑤有同学认为应该在D装置和E装置之间再增加一个
(2)兴趣小组设计如图装置验证二氧化硫的化学性质。

为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去
方案Ⅱ:向第二份溶液加入BaCl2浴液,产生白色沉淀
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成
上述方案中合理的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下列物质A~F是我们熟悉的单质或化合物,其中A、B均是常见的金属,且B的合金用量最大;E在常温下是黄绿色气体;在适当的条件下,它们之间可以发生如下图所示的转化。

试回答下列问题:
⑴ A的化学式是____________ ;
⑵ 反应F→D的化学方程式是______________________________________ 。
⑶ 检验F中金属阳离子的常用方法是___________________________________ 。
⑷ 物质B与盐酸反应的离子方程式是_________________________________ 。

试回答下列问题:
⑴ A的化学式是
⑵ 反应F→D的化学方程式是
⑶ 检验F中金属阳离子的常用方法是
⑷ 物质B与盐酸反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图是铁与水蒸气反应的实验装置。在硬质玻璃管中放入还原铁粉和石棉绒(石棉绒是耐高温材料,与水、铁不反应)的混合物,加热,并通入水蒸气,就可以完成高温下铁与水蒸气反应的实验。

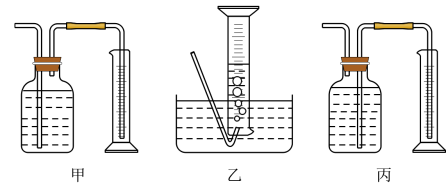
(1)已知该实验反应的反应方程式为:Fe+H2O Fe3O4+H2(请配平)
Fe3O4+H2(请配平)____ 。
(2)仪器a的名称是________ 。
(3)某同学为了研究一定时间内铁粉的转化率,设计了如下实验:准确称量一定质量的铁粉进行反应,测量反应后生成气体的体积,计算铁粉的转化率。
①该同学应该先点燃___ (填“A”或“B”)处的酒精灯(或酒精喷灯),测量气体体积不可以选用上图中___ (填“甲”“乙”或“丙”)装置。
②称取5.6 g铁粉与适量石棉绒混合,然后加热反应一段时间。若测出的气体体积在标准状况下为0.448 L,则铁粉的转化率为___ 。( )
)
(4)将硬质玻璃管中反应后的固体混合物全部取出置于烧杯中,加入足量的盐酸溶解并过滤,为探究反应后溶液中可能的阳离子,小林同学进行如下实验,请你将下表补充完整:


(1)已知该实验反应的反应方程式为:Fe+H2O
 Fe3O4+H2(请配平)
Fe3O4+H2(请配平)(2)仪器a的名称是
(3)某同学为了研究一定时间内铁粉的转化率,设计了如下实验:准确称量一定质量的铁粉进行反应,测量反应后生成气体的体积,计算铁粉的转化率。
①该同学应该先点燃
②称取5.6 g铁粉与适量石棉绒混合,然后加热反应一段时间。若测出的气体体积在标准状况下为0.448 L,则铁粉的转化率为
 )
) (4)将硬质玻璃管中反应后的固体混合物全部取出置于烧杯中,加入足量的盐酸溶解并过滤,为探究反应后溶液中可能的阳离子,小林同学进行如下实验,请你将下表补充完整:
| 步骤 | 现象 | 解释(用离子方程式表示) | 结论 |
| Ⅰ.取样,滴加KSCN溶液 | 溶液不变红色 | ①Fe3O4+8H+=Fe2++2Fe3++4H2O ② | Ⅲ.反应后的溶液中阳离子为 |
| Ⅱ.取样,滴加NaOH溶液 | 刚开始无明显现象,一段时间后先出现 | ① ②Fe2++2OH—=Fe(OH)2↓ ③4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某班同学用实验室中的硫酸亚铁固体和硫酸铁进行实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)甲同学取一定量硫酸亚铁固体,配制FeSO4溶液,取少量溶液于试管,加入2滴KSCN溶液,溶液________ ,甲同学认为硫酸亚铁固体已全部变质。
(2)乙同学认为甲同学的结论不够严谨,他取2mL甲同学配成的FeSO4溶液,加入少量的酸性高锰酸钾溶液,_______ ,乙同学认为硫酸亚铁固体部分变质,理由_____________ (用离子方程式结合文字说明回答)。
(3)甲同学继续探究Fe2+的性质,接着他向盛有H2O2溶液的试管中加入几滴甲同学配成的FeSO4溶液,发生反应的离子方程式为________ ;一段时间后,发现溶液中有气泡出现,产生气泡的原因是_______ 。
(4)丙同学取一定量硫酸铁固体,配制Fe2(SO4)3溶液,取少量溶液于试管,加入铜粉,反应中氧化性:Fe3+_____ Cu2+(填“>”或“<”)。
(5)丁同学向混有少量泥沙的浑浊水中加入Fe2(SO4)3溶液,振荡,然后将试管静置一段时间,观察试管中发生的现象是_______ 。
(1)甲同学取一定量硫酸亚铁固体,配制FeSO4溶液,取少量溶液于试管,加入2滴KSCN溶液,溶液
(2)乙同学认为甲同学的结论不够严谨,他取2mL甲同学配成的FeSO4溶液,加入少量的酸性高锰酸钾溶液,
(3)甲同学继续探究Fe2+的性质,接着他向盛有H2O2溶液的试管中加入几滴甲同学配成的FeSO4溶液,发生反应的离子方程式为
(4)丙同学取一定量硫酸铁固体,配制Fe2(SO4)3溶液,取少量溶液于试管,加入铜粉,反应中氧化性:Fe3+
(5)丁同学向混有少量泥沙的浑浊水中加入Fe2(SO4)3溶液,振荡,然后将试管静置一段时间,观察试管中发生的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某课外小组在实验室制备氨气,并进行有关氨气的性质探究。
(1)该小组同学加热生石灰与氯化铵的混合物制取干燥的氨气。

①应该选用的仪器及装置有(填字母)_______ 。
②生石灰与氯化铵反应生成氨气的化学方程式为_______ 。
(2)该小组同学设计如图所示装置探究氨气的还原性。
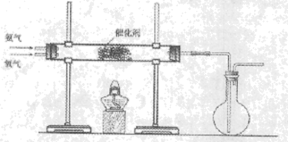
①氨催化氧化的化学方程式为_______ 。
②若实验时通入氨气的速率过快,在烧瓶中会出现白烟,该物质的化学式为_______ 。
(3)该小组同学以氨气和二氧化碳为原料制备碳酸氢铵。
①甲同学先将二氧化碳通入水中,充分溶解后,再通入氨气;乙同学先将氨气通入水中,充分溶解后,再通入二氧化碳。再选择合适的方案并说明原因_______ 。
②检验产物中有NH 的方法为
的方法为_______ 。
(1)该小组同学加热生石灰与氯化铵的混合物制取干燥的氨气。

①应该选用的仪器及装置有(填字母)
②生石灰与氯化铵反应生成氨气的化学方程式为
(2)该小组同学设计如图所示装置探究氨气的还原性。

①氨催化氧化的化学方程式为
②若实验时通入氨气的速率过快,在烧瓶中会出现白烟,该物质的化学式为
(3)该小组同学以氨气和二氧化碳为原料制备碳酸氢铵。
①甲同学先将二氧化碳通入水中,充分溶解后,再通入氨气;乙同学先将氨气通入水中,充分溶解后,再通入二氧化碳。再选择合适的方案并说明原因
②检验产物中有NH
 的方法为
的方法为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以赤铁矿(主要成分为60.0%Fe2O3,杂质有3.6%FeO,Al2O3,MnO2,CuO等)为原料制备高活性铁单质的主要生产流程如图所示:
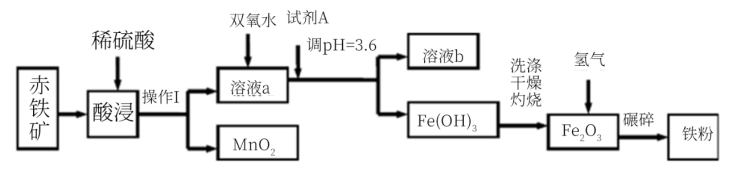
已知部分阳离子以氢氧化物形式完全沉淀时溶液的pH如表所示, 请回答下列问题:
(1)将操作Ⅰ后所得的MnO2与KClO3、KOH溶液混合共热,可得到K2MnO4,此反应的化学方程式是____________________________ 。
(2)将pH控制在3.6的目的是_______ 。 已知25℃时,Ksp[Cu(OH)2]=2×10-20 ,该温度下反应Cu2++2H2O Cu(OH)2+2H+的平衡常数K=
Cu(OH)2+2H+的平衡常数K=_______ 。
(3)加入双氧水时反应的离子方程式为_______ 。
(4)利用氨气在500℃以上分解得到的氮原子渗透到铁粉中可制备氮化铁(FexNy),若消耗氨气17.0g,消耗赤铁矿石1kg,写出该反应完整的化学方程式:_______________ 。

已知部分阳离子以氢氧化物形式完全沉淀时溶液的pH如表所示, 请回答下列问题:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Cu(OH)2 |
| pH | 3.4 | 5.2 | 9.7 | 6.7 |
(2)将pH控制在3.6的目的是
 Cu(OH)2+2H+的平衡常数K=
Cu(OH)2+2H+的平衡常数K=(3)加入双氧水时反应的离子方程式为
(4)利用氨气在500℃以上分解得到的氮原子渗透到铁粉中可制备氮化铁(FexNy),若消耗氨气17.0g,消耗赤铁矿石1kg,写出该反应完整的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4·H2O(三盐),主要制备流程如下。
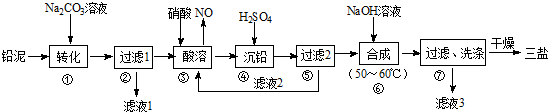
请回答下列问题:
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4 2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为
2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为__________ 。
(2)将滤液1、滤液3合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物(Mr=322),其化学式为______________________ 。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO。滤液2中溶质的主要成分为______ (填化学式)。
(4)步骤⑥合成三盐的化学方程式为______________________ 。
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是__________________ 。

请回答下列问题:
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4
 2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为
2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为(2)将滤液1、滤液3合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物(Mr=322),其化学式为
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO。滤液2中溶质的主要成分为
(4)步骤⑥合成三盐的化学方程式为
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是
您最近一年使用:0次



