下列实验方案能达到实验目的的是( )
实验目的 | 实验方案 | |
A | 检验Na2SO3晶体是否已氧化变质 | 将Na2SO3样品溶于稀硝酸后,滴加BaCl2溶液,观察是否有沉淀生成 |
B | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
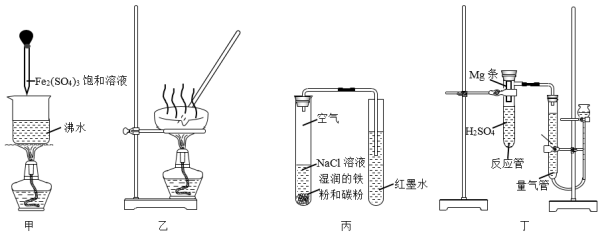
C | 制备氢氧化铁胶体 | 向沸水中滴加氯化铁稀溶液,继续煮沸至溶液呈红褐色 |
D | 证明Mg(OH)2沉淀可转化为Fe(OH)3沉淀 | 向2 mL 1 mol/L NaOH溶液中先加入3滴1 mol/L MgCl2溶液,再加入3滴1 mol/L FeCl3溶液 |
| A.A | B.B | C.C | D.D |
更新时间:2017/04/17 17:01:12
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列事实或性质与胶体没有直接关系的是
| A.同一钢笔使用不同牌号的墨水容易堵塞 | B.在河流入海处易形成三角洲 |
| C.向NaOH溶液中滴加FeCl3溶液产生沉淀 | D.水稻田使用NH4NO3的肥效较差 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.将NaOH浓溶液滴加到饱和FeCl3溶液中制备Fe(OH)3胶体 |
| B.胶体的分散质不能透过滤纸 |
| C.碱性氧化物一定是金属氧化物,金属氧化物一定是碱性氧化物 |
| D.非金属氧化物不一定是酸性氧化物,金属氧化物也不一定碱性氧化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列反应对应的方程式正确的是
A.用碳酸钠溶液处理锅炉水垢(CaSO4):CaSO4(s)+  CaCO2(s)+ CaCO2(s)+ |
B.实验室制备氢氧化铁胶体:Fe3++3NH3·H2O Fe(OH)3(胶体)+3 Fe(OH)3(胶体)+3 |
C.工业上用电解法制备金属铝:2AlC13 2Al+3C12↑ 2Al+3C12↑ |
D.湿润的淀粉碘化钾试纸遇氯气变蓝:3Cl2+I-+3H2O===6C1-+ +6H+ +6H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】分别依据下列实验事实,得出的结论正确的是
| 实验事实 | 结论 | |
| A | 苯酚和水的浊液中,加碳酸钠溶液,溶液变澄清 | 苯酚的酸性比碳酸强 |
| B | 向盛有KBr溶液的试管中滴加几滴新制氯水,再加入CCl4溶液,振荡、静置,观察CCl4层颜色 | Cl2的氧化性比Br2的强 |
| C | 铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 向2 mL 0.1 mol/L的硝酸银溶液中加入1 mL0.1mol/LNaCl溶液,出现白色沉淀,再加入几滴0.1 mol/L Na2S溶液,有黑色沉淀生成 | 氯化银的溶解度大于硫化银 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验操作与预期实验目的或所得实验结论一致的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 将氯乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验水解产物中的氯离子 |
| B | 乙醇与浓硫酸加热到170 ℃,将所得气体通入溴水中 | 确定是否有乙烯生成 |
| C | 溴乙烷与氢氧化钠醇溶液共热,将生成的气体通入溴水中 | 确定是否有乙烯生成 |
| D | 电石与水反应,制得的气体直接通入酸性KMnO4溶液 | 检验制得的气体是否为乙炔 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验操作、实验现象及结论中合理的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将乙醇与浓硫酸共热产生的气体,产生气体通入溴水 | 溴水褪色 | 产生的气体为乙烯 |
| B | 电石和饱和食盐水反应,产生的气体通过硫酸铜溶液,再通入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色 | 产生的气体为乙炔 |
| C | 向溴乙烷中加入 的乙醇溶液,加热,产生的气体通入酸性高锰酸钾溶液中 的乙醇溶液,加热,产生的气体通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色 | 产生的气体为乙烯 |
| D | 将少量卤代烃与 溶液混合共热,充分反应并冷却后,滴加 溶液混合共热,充分反应并冷却后,滴加 溶液 溶液 | 有淡黄色浑浊出现 | 该卤代烃为溴代烃 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】根据下列实验目的和实验设计,所得现象和结论正确的是
| 选项 | 实验目的 | 实验设计 | 现象和结论 |
| A | 验证浓度对反应速率的影响 | 两支试管各盛4mL 0.1 酸性高锰酸钾溶液,分别加入2mL 0.1 酸性高锰酸钾溶液,分别加入2mL 0.1 草酸溶液和2mL 0.2 草酸溶液和2mL 0.2 草酸溶液 草酸溶液 | 加0.2 草酸溶液的试管中,高锰酸钾溶液完全褪色且更快,反应物浓度越大,反应速率越快 草酸溶液的试管中,高锰酸钾溶液完全褪色且更快,反应物浓度越大,反应速率越快 |
| B | 判断 的化学键 的化学键 | 将固体 溶于水,进行导电实验 溶于水,进行导电实验 |  溶液导电, 溶液导电, 中含有离子键 中含有离子键 |
| C | 比较 和 和 结合质子的能力 结合质子的能力 | 将 溶液滴入 溶液滴入 溶液中 溶液中 | 产生白色沉淀, 比 比 结合质子的能力强 结合质子的能力强 |
| D | 探究1-溴丁烷反应机理 | 向圆底烧瓶中加入NaOH固体和无水乙醇,搅拌后再加入1-溴丁烷,微热,将产生的气体通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色,1-溴丁烷发生了消去反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】为探究某样品的成分(可能为亚硝酸钠或氯化钠),将样品溶于水配成溶液,分别取少量该溶液于试管中进行实验。下列方案设计、现象和结论都正确的是
| 选项 | 方案设计 | 现象和结论 |
| A | 先加入少量 溶液,再加 溶液,再加 溶液和足量稀硝酸,振荡 溶液和足量稀硝酸,振荡 | 若产生白色沉淀,则样品为亚硝酸钠 |
| B | 先加到少量淀粉KI溶液中,再加入稀盐酸酸化,振荡 | 若溶液变蓝色,则样品为亚硝酸钠 |
| C | 加到少量 溶液中,再加硫酸酸化,振荡 溶液中,再加硫酸酸化,振荡 | 若溶液褪色,则样品为亚硝酸钠 |
| D | 先加入少量 溶液,再加入 溶液,再加入 溶液和稀硝酸,振荡 溶液和稀硝酸,振荡 | 若产生白色沉淀,则样品为亚硝酸钠 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某澄清透明溶液可能含有Na+、Cl-、 、
、 、Mg2+、
、Mg2+、 中的几种,进行如下实验:将上述溶液分为两等份,其中一份滴加足量的BaCl2溶液,得到白色沉淀4.66g;另一份溶液中滴加足量的NaOH溶液,得到0.58g白色沉淀,加热后产生标准状况下的气体0.224L,该气体能使湿润的红色石蕊试纸变蓝色。下列说法正确的是
中的几种,进行如下实验:将上述溶液分为两等份,其中一份滴加足量的BaCl2溶液,得到白色沉淀4.66g;另一份溶液中滴加足量的NaOH溶液,得到0.58g白色沉淀,加热后产生标准状况下的气体0.224L,该气体能使湿润的红色石蕊试纸变蓝色。下列说法正确的是
 、
、 、Mg2+、
、Mg2+、 中的几种,进行如下实验:将上述溶液分为两等份,其中一份滴加足量的BaCl2溶液,得到白色沉淀4.66g;另一份溶液中滴加足量的NaOH溶液,得到0.58g白色沉淀,加热后产生标准状况下的气体0.224L,该气体能使湿润的红色石蕊试纸变蓝色。下列说法正确的是
中的几种,进行如下实验:将上述溶液分为两等份,其中一份滴加足量的BaCl2溶液,得到白色沉淀4.66g;另一份溶液中滴加足量的NaOH溶液,得到0.58g白色沉淀,加热后产生标准状况下的气体0.224L,该气体能使湿润的红色石蕊试纸变蓝色。下列说法正确的是| A.溶液中可能有Na+、Cl- |
B.溶液中一定没有Cl-、 |
C.溶液中一定有Na+、 、Mg2+、 、Mg2+、 |
| D.是否存在Na+离子只能通过焰色反应确认 |
您最近一年使用:0次

 胶体
胶体 溶液制备无水
溶液制备无水 的体积
的体积 的水称为暂时硬水,加热可除去Ca2+、Mg2+,使水变为软水。现有一锅炉厂使用这种水,试判断其水垢的主要成分为(已知Ksp(MgCO3)=6.8×10-6,Ksp[Mg(OH)2]=5.6×10-12)
的水称为暂时硬水,加热可除去Ca2+、Mg2+,使水变为软水。现有一锅炉厂使用这种水,试判断其水垢的主要成分为(已知Ksp(MgCO3)=6.8×10-6,Ksp[Mg(OH)2]=5.6×10-12)
 等杂质,可依次加入过量的Na2CO3溶液、NaOH溶液、BaCl2溶液除去
等杂质,可依次加入过量的Na2CO3溶液、NaOH溶液、BaCl2溶液除去

