以下是对金属及其化合物的讨论,根据要求回答问题:
(1)写出钠与水反应的离子方程式:____________ 。
(2)在CuSO4溶液中逐滴滴入NaOH溶液,观察到的现象是_____________ 。
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为________ 。
(1)写出钠与水反应的离子方程式:
(2)在CuSO4溶液中逐滴滴入NaOH溶液,观察到的现象是
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为
更新时间:2017-04-27 18:32:31
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】碱金属单质及其化合物有广泛应用。回答下列问题:
(1)锂是最轻的活泼金属,常用于制造高效锂电池。电解池中的电解液不能用水作溶剂,原因是_______ 。
(2)金属钾是一种活泼的金属,下列有关其性质的说法正确的是_______ (填字母)。
A.钾在空气中燃烧时,只生成
B.钾与水反应,由于反应剧烈可能会发生爆炸
C.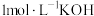 溶液比
溶液比 溶液碱性强
溶液碱性强
(3)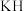 是一种野外供氢剂,其电子式为
是一种野外供氢剂,其电子式为_______ ,与水反应放出氢气,化学方程式为_______ 。生成 气时,反应中转移电子数为
气时,反应中转移电子数为_______ 。
(4) 在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为
在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为 ),脱锈过程中生成两种产物,其反应的化学方程式:
),脱锈过程中生成两种产物,其反应的化学方程式:_______ 。
(1)锂是最轻的活泼金属,常用于制造高效锂电池。电解池中的电解液不能用水作溶剂,原因是
(2)金属钾是一种活泼的金属,下列有关其性质的说法正确的是
A.钾在空气中燃烧时,只生成

B.钾与水反应,由于反应剧烈可能会发生爆炸
C.
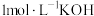 溶液比
溶液比 溶液碱性强
溶液碱性强(3)
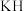 是一种野外供氢剂,其电子式为
是一种野外供氢剂,其电子式为 气时,反应中转移电子数为
气时,反应中转移电子数为(4)
 在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为
在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为 ),脱锈过程中生成两种产物,其反应的化学方程式:
),脱锈过程中生成两种产物,其反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:

(1)物质①与水反应的离子方程式为_______ ,所以通常将其保存在_______ 中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式:_______ 。
(3)从核心元素价态的视角看, 中H元素的化合价为
中H元素的化合价为_______ ,从H元素的价态分析, 常用作
常用作_______ (填“氧化剂”或“还原剂)。
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。工业上“侯氏制碱法”以 及水等为原料制备纯碱,其主要反应原理为:
及水等为原料制备纯碱,其主要反应原理为: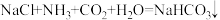
 。该工艺析出的
。该工艺析出的 固体中可能含有少量氯离子杂质,检验该固体中含有氯离子杂质的操作方法是
固体中可能含有少量氯离子杂质,检验该固体中含有氯离子杂质的操作方法是_______ 。
(5)若制得的纯碱中只含有杂质 。测定该纯碱的纯度,下列方案中可行的是
。测定该纯碱的纯度,下列方案中可行的是_______ 。(填字母)
A.向 纯碱样品中加入足量
纯碱样品中加入足量 溶液,沉淀经过滤、洗涤、干燥,称其质量为
溶液,沉淀经过滤、洗涤、干燥,称其质量为
B.向 纯碱样品中加入足量稀盐酸,用碱石灰(主要成分是
纯碱样品中加入足量稀盐酸,用碱石灰(主要成分是 和
和 )吸收产生的气体,碱石灰增重
)吸收产生的气体,碱石灰增重
C.向 纯碱样品中加入足量
纯碱样品中加入足量 溶液,产生的沉淀经过滤、洗涤、干燥,称其质量为
溶液,产生的沉淀经过滤、洗涤、干燥,称其质量为

(1)物质①与水反应的离子方程式为
(2)写出淡黄色固体②与二氧化碳反应的化学方程式:
(3)从核心元素价态的视角看,
 中H元素的化合价为
中H元素的化合价为 常用作
常用作(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。工业上“侯氏制碱法”以
 及水等为原料制备纯碱,其主要反应原理为:
及水等为原料制备纯碱,其主要反应原理为: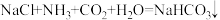
 。该工艺析出的
。该工艺析出的 固体中可能含有少量氯离子杂质,检验该固体中含有氯离子杂质的操作方法是
固体中可能含有少量氯离子杂质,检验该固体中含有氯离子杂质的操作方法是(5)若制得的纯碱中只含有杂质
 。测定该纯碱的纯度,下列方案中可行的是
。测定该纯碱的纯度,下列方案中可行的是A.向
 纯碱样品中加入足量
纯碱样品中加入足量 溶液,沉淀经过滤、洗涤、干燥,称其质量为
溶液,沉淀经过滤、洗涤、干燥,称其质量为
B.向
 纯碱样品中加入足量稀盐酸,用碱石灰(主要成分是
纯碱样品中加入足量稀盐酸,用碱石灰(主要成分是 和
和 )吸收产生的气体,碱石灰增重
)吸收产生的气体,碱石灰增重
C.向
 纯碱样品中加入足量
纯碱样品中加入足量 溶液,产生的沉淀经过滤、洗涤、干燥,称其质量为
溶液,产生的沉淀经过滤、洗涤、干燥,称其质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】把一小块金属钠投入水中,观察到以下各种现象:钠浮在水面上,熔成闪亮的小球,四处游动,逐渐减少,直至消失。
(1)写出该反应的离子方程式:_______ ,其中钠熔成闪亮小球的原因是_______ 。
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式:_______ 。
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的离子方程式:_______ ;然后将沉淀过滤、洗涤、干燥、灼烧,最后得到Fe2O3固体1.6 g,通过计算,可知最初加入金属钠的质量为_______ g(保留小数点后两位小数)。
(1)写出该反应的离子方程式:
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式:
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】在标准状况下进行甲、乙、丙三组实验,三组实验均各取30mL同浓度的盐酸,加入同一种镁铝合金粉末,产生气体,有关数据见表:
(1)甲组实验中,盐酸_____ (填“过量”、“适量”或“不足量”),理由是_____ ;
(2)丙组实验中,盐酸_____ (填“过量”、“适量”或“不足量”),理由是_____ 。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/m g | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(1)甲组实验中,盐酸
(2)丙组实验中,盐酸
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为___________ ,发生反应的离子方程式为___________ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 在同温同压下的体积之比是
在同温同压下的体积之比是___________ 。
(3)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下: 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为___________ 。
②滤液Ⅱ中溶质的用途之一是___________ 。
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 在同温同压下的体积之比是
在同温同压下的体积之比是(3)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下: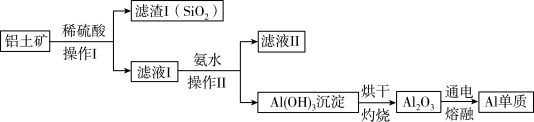
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为②滤液Ⅱ中溶质的用途之一是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】用离子方程式表示实验室怎样用化学方法除去下列物质中混有的少量杂质:
①铁粉中混有铝粉___________
②FeCl2溶液中混有FeCl3___________
③CO2气体中混有HCl气体___________
①铁粉中混有铝粉
②FeCl2溶液中混有FeCl3
③CO2气体中混有HCl气体
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为___________ ,发生反应的离子方程式为___________ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 在同温同压下的体积之比是
在同温同压下的体积之比是___________ 。
(3)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下: 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为___________ 。
②滤液Ⅱ中溶质的用途之一是___________ 。
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 在同温同压下的体积之比是
在同温同压下的体积之比是(3)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为②滤液Ⅱ中溶质的用途之一是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】波尔多液是农业上常用的杀菌剂,配制波尔多液的主要原料有生石灰和硫酸铜,在配制和使用时有诸多注意事项。
(1)配制时:先将生石灰、硫酸铜分别溶于水,该过程中发生反应的化学方程式是_______ 。然后将所得的硫酸铜溶液缓慢倒入石灰乳中,即得到波尔多液。若将石灰乳倒入硫酸铜溶液中,易产生蓝色沉淀,该沉淀的化学式是_______ 。
(2)波尔多液中硫酸铜比例过高易造成药害。有经验的果农常将磨光的铁制芽接刀浸泡在药液里,若产生药害,只需1~2分钟就有明显现象出现,该现象是_______ ,反应的化学方程式是_______ 。
(1)配制时:先将生石灰、硫酸铜分别溶于水,该过程中发生反应的化学方程式是
(2)波尔多液中硫酸铜比例过高易造成药害。有经验的果农常将磨光的铁制芽接刀浸泡在药液里,若产生药害,只需1~2分钟就有明显现象出现,该现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】我国古代在冶炼金属方面成就显著,请回答:
(1)商代司母戊鼎属于_____ (选填“青铜”、“铁合金”或“铝合金”)制品。
(2)下图为铜及其化合物之间的转化关系(反应条件略去):
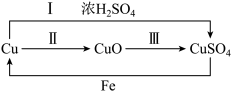
①上述转化常伴随颜色的变化,紫红色的铜与氧气反应生成______ 色的氧化铜;
②“曾青得铁则化为铜”体现了我国古代湿法炼铜的原理,其中的反应有:Fe + CuSO4 = FeSO4 + Cu,由此可知铁比铜的金属活动性________ (选填写“强”或“弱”);
③为验证铜和浓硫酸反应生成的气体,将气体通入品红溶液,观察到的现象是_______ ;
④由上图可知,制备硫酸铜可以用途径甲(反应Ⅰ)或途径乙(反应Ⅱ+Ⅲ),从环保角度考虑,应选择途径________ (选填“甲”或“乙”),理由是_____ 。
(1)商代司母戊鼎属于
(2)下图为铜及其化合物之间的转化关系(反应条件略去):

①上述转化常伴随颜色的变化,紫红色的铜与氧气反应生成
②“曾青得铁则化为铜”体现了我国古代湿法炼铜的原理,其中的反应有:Fe + CuSO4 = FeSO4 + Cu,由此可知铁比铜的金属活动性
③为验证铜和浓硫酸反应生成的气体,将气体通入品红溶液,观察到的现象是
④由上图可知,制备硫酸铜可以用途径甲(反应Ⅰ)或途径乙(反应Ⅱ+Ⅲ),从环保角度考虑,应选择途径
您最近一年使用:0次

 中,会出现少量白色固体,原因是
中,会出现少量白色固体,原因是 溶液,搅拌下滴加足量
溶液,搅拌下滴加足量

