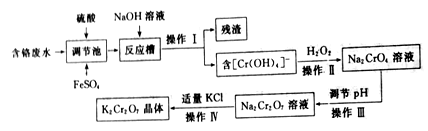
重铬酸钾(K2Cr2O7)是一种常见的强氧化剂,能氧化硫酸亚铁、盐酸等物质。某兴趣小组模拟企业处理含铬废水(主要含Cr2O72-和Cr3+),同时获得重铬酸钾晶体的流程如下:
回答下列问题:
(1)操作I是______ ,残渣的主要成分是______ 。
(2)调节池中发生的主要反应的离子方程式为__________________ 。
(3)操作Ⅲ__________ (填“能”或“不能”)用盐酸调节溶液pH,原因是___________ 。
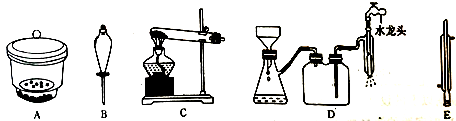
(4)从Na2Cr2O7溶液中获得K2Cr2O7晶体的操作依次是加入适量KCl固体,搅拌、溶解,在水浴上加热浓缩至________ 时停止加热。接下来获得K2Cr2O7晶体需要的一系列操作中,下列仪器可能会用到的是__________ (填标号)。
(5)为检测处理后废水是否达到排放标准,某同学进行了如下实验:取100mL处理后的废液样品于锥形瓶中,用浓醋酸调节pH=5并加入适量固体抗坏血酸,使Cr2O72-完全转化为Cr2+,再用cmol· L-1的EDTA(用H4Y表示)标准溶液进行滴定,其反应原理为:Cr3++Y4-=CrY-,若实验消耗EDTA标准溶液VmL,则处理后的废液中含铬元素浓度为______ mg·L-1(用含c、V的式子表示)。
回答下列问题:
(1)操作I是
(2)调节池中发生的主要反应的离子方程式为
(3)操作Ⅲ
(4)从Na2Cr2O7溶液中获得K2Cr2O7晶体的操作依次是加入适量KCl固体,搅拌、溶解,在水浴上加热浓缩至
(5)为检测处理后废水是否达到排放标准,某同学进行了如下实验:取100mL处理后的废液样品于锥形瓶中,用浓醋酸调节pH=5并加入适量固体抗坏血酸,使Cr2O72-完全转化为Cr2+,再用cmol· L-1的EDTA(用H4Y表示)标准溶液进行滴定,其反应原理为:Cr3++Y4-=CrY-,若实验消耗EDTA标准溶液VmL,则处理后的废液中含铬元素浓度为
更新时间:2017-05-07 19:20:10
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钪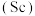 是一种重要的稀土金属,常用来制特种玻璃、轻质耐高温合金。从赤泥矿(主要成分为
是一种重要的稀土金属,常用来制特种玻璃、轻质耐高温合金。从赤泥矿(主要成分为 、
、 、
、 、
、 )中回收钪,同时生产聚合氯化铁铝
)中回收钪,同时生产聚合氯化铁铝 ,其中一种工艺流程如图所示。
,其中一种工艺流程如图所示。
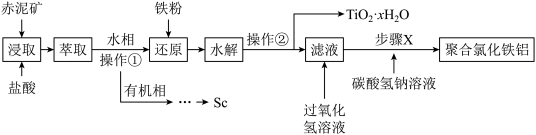
已知:浸取液中含有 。请回答以下问题:
。请回答以下问题:
(1)铝元素在元素周期表中的位置为___________ ,过氧化氢的电子式为___________ 。聚合氯化铁铝 中铁的化合价为
中铁的化合价为___________ 价。
(2)操作①的实验名称为___________ ,需要用到的玻璃仪器有___________ 。
(3)浸取时 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)步骤X中生成聚合氯化铁铝的化学方程式为___________ 。
 是一种重要的稀土金属,常用来制特种玻璃、轻质耐高温合金。从赤泥矿(主要成分为
是一种重要的稀土金属,常用来制特种玻璃、轻质耐高温合金。从赤泥矿(主要成分为 、
、 、
、 、
、 )中回收钪,同时生产聚合氯化铁铝
)中回收钪,同时生产聚合氯化铁铝 ,其中一种工艺流程如图所示。
,其中一种工艺流程如图所示。
已知:浸取液中含有
 。请回答以下问题:
。请回答以下问题:(1)铝元素在元素周期表中的位置为
 中铁的化合价为
中铁的化合价为(2)操作①的实验名称为
(3)浸取时
 发生反应的离子方程式为
发生反应的离子方程式为(4)步骤X中生成聚合氯化铁铝的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】某溶液的溶质只可能由下列离子中的几种组成:Cl—、CO 、SO
、SO 、H+、Ba2+、Na+,某同学进行了如下实验:
、H+、Ba2+、Na+,某同学进行了如下实验:
①向溶液中加入过量的BaCl2溶液,有白色沉淀生成,过滤;
②向①中滤液加入AgNO3溶液,有白色沉淀产生;
③将①的沉淀加入稀盐酸中,沉淀部分消失,有气体生成。
依据以上实验可以推断:(填化学式)
(1)原溶液中一定含有___________ ;一定没有___________ ;可能含有___________ 。
(2)②中生成的沉淀是___________ ;③中反应的离子方程式是___________ 。
 、SO
、SO 、H+、Ba2+、Na+,某同学进行了如下实验:
、H+、Ba2+、Na+,某同学进行了如下实验:①向溶液中加入过量的BaCl2溶液,有白色沉淀生成,过滤;
②向①中滤液加入AgNO3溶液,有白色沉淀产生;
③将①的沉淀加入稀盐酸中,沉淀部分消失,有气体生成。
依据以上实验可以推断:(填化学式)
(1)原溶液中一定含有
(2)②中生成的沉淀是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】草酸钴在化学中应用广泛,可以用于制取催化剂和指示剂。以铜钴矿石[主要成分为CoO(OH)、 、
、 和
和 ,还有少量
,还有少量 、NiO]为原料制取草酸钴晶体(化学式
、NiO]为原料制取草酸钴晶体(化学式 ,式量为183)的工艺流程如下:
,式量为183)的工艺流程如下:
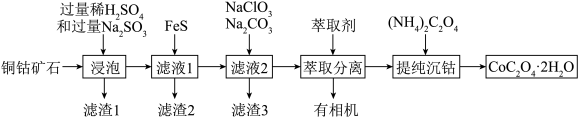
已知:部分物质的溶度积常数见下表(离子浓度c≤10-5mol/L视为该离子沉淀完全)。
回答下列问题:
(1)“浸泡”前,对铜钴矿石进行粉碎处理的目的是_______ ;“滤渣1”的成分是_______ 。
(2)“浸泡”过程中CoO(OH)发生氧化还原反应的离子方程式为_______ 。
(3)“滤液1”中加入FeS的作用是_______ 。
(4)“滤液2”中加入 的作用是调节pH,若
的作用是调节pH,若 ,则应调节pH的范围是
,则应调节pH的范围是_______ 。
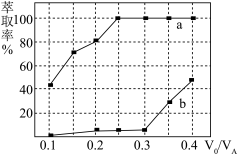
(5)加入萃取剂萃取分离 和
和 ,原理为
,原理为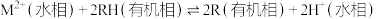 。萃取剂与溶液的体积比(
。萃取剂与溶液的体积比(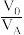 )对溶液中
)对溶液中 和
和 的萃取率影响如图所示,则
的萃取率影响如图所示,则 的萃取率对应曲线
的萃取率对应曲线_______ (填标号),在强酸性介质中“反萃取”能使有机相中_______ 再生。
(6)钴的氧化物常用作颜料或反应催化剂,可以由草酸钴晶体在空气中加热制取,取36.6 g草酸钴晶体,在空气中加热至恒重,得到CoO与 的混合物15.8 g,该混合物中CoO与
的混合物15.8 g,该混合物中CoO与 的物质的量之比为
的物质的量之比为_______ 。
 、
、 和
和 ,还有少量
,还有少量 、NiO]为原料制取草酸钴晶体(化学式
、NiO]为原料制取草酸钴晶体(化学式 ,式量为183)的工艺流程如下:
,式量为183)的工艺流程如下:
已知:部分物质的溶度积常数见下表(离子浓度c≤10-5mol/L视为该离子沉淀完全)。
| 物质 | FeS | CuS |  |  |
 |  |  | 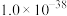 | 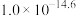 |
回答下列问题:
(1)“浸泡”前,对铜钴矿石进行粉碎处理的目的是
(2)“浸泡”过程中CoO(OH)发生氧化还原反应的离子方程式为
(3)“滤液1”中加入FeS的作用是
(4)“滤液2”中加入
 的作用是调节pH,若
的作用是调节pH,若 ,则应调节pH的范围是
,则应调节pH的范围是(5)加入萃取剂萃取分离
 和
和 ,原理为
,原理为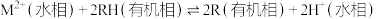 。萃取剂与溶液的体积比(
。萃取剂与溶液的体积比( )对溶液中
)对溶液中 和
和 的萃取率影响如图所示,则
的萃取率影响如图所示,则 的萃取率对应曲线
的萃取率对应曲线
(6)钴的氧化物常用作颜料或反应催化剂,可以由草酸钴晶体在空气中加热制取,取36.6 g草酸钴晶体,在空气中加热至恒重,得到CoO与
 的混合物15.8 g,该混合物中CoO与
的混合物15.8 g,该混合物中CoO与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】 是一种黑色固体,难溶于水、稀硫酸,可用于锰盐的制备,也用作氧化剂、催化剂等。某学习小组设计实验将粗
是一种黑色固体,难溶于水、稀硫酸,可用于锰盐的制备,也用作氧化剂、催化剂等。某学习小组设计实验将粗 样品(含有较多的
样品(含有较多的 和
和 )转化为纯
)转化为纯 ,其流程如图所示:
,其流程如图所示:
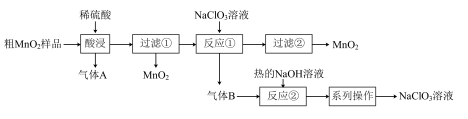
回答下列问题:
(1)“酸浸”中生成气体A的离子方程式为___________ 。
(2)反应①的离子方程式为___________ 。
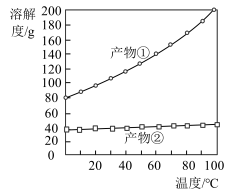
(3)若要得到较浓的 溶液,根据反应②产物的溶解度曲线(如图所示),产物②为
溶液,根据反应②产物的溶解度曲线(如图所示),产物②为___________ (写化学式),“系列操作”为先___________ ,后___________ 。
(4)若粗 样品的质量为
样品的质量为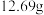 ,经“过滤①”得到
,经“过滤①”得到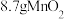 ,并收集到
,并收集到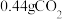 ,则在“反应①”中至少需要
,则在“反应①”中至少需要 的物质的量为
的物质的量为___________  。
。
(5)该流程中可循环利用的物质有___________ 。
 是一种黑色固体,难溶于水、稀硫酸,可用于锰盐的制备,也用作氧化剂、催化剂等。某学习小组设计实验将粗
是一种黑色固体,难溶于水、稀硫酸,可用于锰盐的制备,也用作氧化剂、催化剂等。某学习小组设计实验将粗 样品(含有较多的
样品(含有较多的 和
和 )转化为纯
)转化为纯 ,其流程如图所示:
,其流程如图所示:
回答下列问题:
(1)“酸浸”中生成气体A的离子方程式为
(2)反应①的离子方程式为
(3)若要得到较浓的
 溶液,根据反应②产物的溶解度曲线(如图所示),产物②为
溶液,根据反应②产物的溶解度曲线(如图所示),产物②为
(4)若粗
 样品的质量为
样品的质量为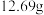 ,经“过滤①”得到
,经“过滤①”得到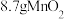 ,并收集到
,并收集到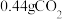 ,则在“反应①”中至少需要
,则在“反应①”中至少需要 的物质的量为
的物质的量为 。
。(5)该流程中可循环利用的物质有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。
(1)请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式___________ 。
(2)某研究性学习小组为测定 溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:
溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:
①取少量待测液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是___________ 。
②溶液组成的测定:取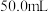 待测液,加入足量的
待测液,加入足量的 溶液,得到
溶液,得到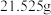 白色沉淀,则溶液中
白色沉淀,则溶液中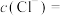
___________  。
。
(3)从腐蚀废液(主要含 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,废液处理流程如下:
溶液,废液处理流程如下:
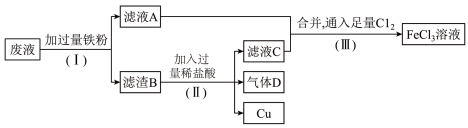
①滤渣B中主要含有___________ ,气体D是___________ 。
②写出步骤(Ⅲ)中生成 的化学方程式
的化学方程式___________ 。
③步骤(Ⅲ)中,将 换成
换成___________ 也能达到同样的目的,写出所换成的物质将 氧化为
氧化为 的离子方程式
的离子方程式___________ 。
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。(1)请写出
 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式(2)某研究性学习小组为测定
 溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:
溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:①取少量待测液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是
②溶液组成的测定:取
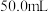 待测液,加入足量的
待测液,加入足量的 溶液,得到
溶液,得到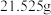 白色沉淀,则溶液中
白色沉淀,则溶液中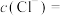
 。
。(3)从腐蚀废液(主要含
 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,废液处理流程如下:
溶液,废液处理流程如下:
①滤渣B中主要含有
②写出步骤(Ⅲ)中生成
 的化学方程式
的化学方程式③步骤(Ⅲ)中,将
 换成
换成 氧化为
氧化为 的离子方程式
的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高铁酸钾( )具有强氧化性,是一种环保、高效、多功能的水处理剂,实验室用含少量
)具有强氧化性,是一种环保、高效、多功能的水处理剂,实验室用含少量 杂质的铁屑原料,经过如下流程制备少量
杂质的铁屑原料,经过如下流程制备少量 。
。

(1) 中铁元素的化合价是
中铁元素的化合价是___________ 。
(2)往原料中添加过量 除去的物质为
除去的物质为___________ 。
(3)“预氧化”环节的离子方程式是___________ 。
(4)“制备 ”的反应中,还原剂和氧化剂的物质的量之比为
”的反应中,还原剂和氧化剂的物质的量之比为___________ 。
(5)“熔融法”是最早发现+6价高铁酸盐的方法,该法制备高铁酸盐的原理如下: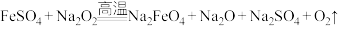 ,若反应中被氧化的
,若反应中被氧化的 与被还原的
与被还原的 之物质的量比为1∶4,请写出该反应配平后的方程式:
之物质的量比为1∶4,请写出该反应配平后的方程式:___________ 。此时,若反应产生11.2L(标准状况) ,则转移的电子为
,则转移的电子为___________ mol。
 )具有强氧化性,是一种环保、高效、多功能的水处理剂,实验室用含少量
)具有强氧化性,是一种环保、高效、多功能的水处理剂,实验室用含少量 杂质的铁屑原料,经过如下流程制备少量
杂质的铁屑原料,经过如下流程制备少量 。
。
(1)
 中铁元素的化合价是
中铁元素的化合价是(2)往原料中添加过量
 除去的物质为
除去的物质为(3)“预氧化”环节的离子方程式是
(4)“制备
 ”的反应中,还原剂和氧化剂的物质的量之比为
”的反应中,还原剂和氧化剂的物质的量之比为(5)“熔融法”是最早发现+6价高铁酸盐的方法,该法制备高铁酸盐的原理如下:
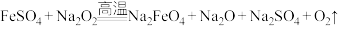 ,若反应中被氧化的
,若反应中被氧化的 与被还原的
与被还原的 之物质的量比为1∶4,请写出该反应配平后的方程式:
之物质的量比为1∶4,请写出该反应配平后的方程式: ,则转移的电子为
,则转移的电子为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】纳米TiO2在涂料、光催化化妆品等领域有着极其广泛的应用。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干,焙烧除去水分得到粉体TiO2。
用现代分析仪器测定TiO2微粒的大小,用氧化还原滴定法测定TiO2的质量分数;一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液做指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(1)TiCl4水解生成TiO2•xH2O的化学方程式为__ 。
(2)检验TiO2•xH2O中Cl-是否除净的方法是___ 。
(3)配制NH4Fe(SO4)2标准溶液时,需要加入一定量稀硫酸的原因是___ 。
(4)滴定终点的现象是___ 。
(5)滴定分析时,称取TiO2(摩尔质量为Mg•mol-1)试样wg,消耗cmol•L-1NH4Fe(SO4)2标准溶液VmL,则TiO2的质量分数的表达式为___ 。
(6)判断下列实验操作对TiO2质量分数的测定结果的影响(填“偏高”“偏低”或“无影响”)。
①配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,则测定结果___ 。
②滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果__ 。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干,焙烧除去水分得到粉体TiO2。
用现代分析仪器测定TiO2微粒的大小,用氧化还原滴定法测定TiO2的质量分数;一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液做指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(1)TiCl4水解生成TiO2•xH2O的化学方程式为
(2)检验TiO2•xH2O中Cl-是否除净的方法是
(3)配制NH4Fe(SO4)2标准溶液时,需要加入一定量稀硫酸的原因是
(4)滴定终点的现象是
(5)滴定分析时,称取TiO2(摩尔质量为Mg•mol-1)试样wg,消耗cmol•L-1NH4Fe(SO4)2标准溶液VmL,则TiO2的质量分数的表达式为
(6)判断下列实验操作对TiO2质量分数的测定结果的影响(填“偏高”“偏低”或“无影响”)。
①配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,则测定结果
②滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:
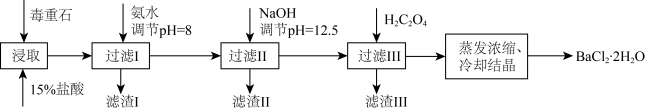
利用简洁酸碱滴定法可测定Ba2+的含量,实验分两步进行:
已知:2CrO42—+2H+=Cr2O72—+H2O Ba2++CrO42—=BaCrO4↓
步骤Ⅰ 移取xml一定浓度的Na2CrO4溶液与锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL。
步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的_______ (填“上方”或“下方”)。BaCl2溶液的浓度为________ mol·L-1,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将________ (填“偏大”或“偏小”)。

利用简洁酸碱滴定法可测定Ba2+的含量,实验分两步进行:
已知:2CrO42—+2H+=Cr2O72—+H2O Ba2++CrO42—=BaCrO4↓
步骤Ⅰ 移取xml一定浓度的Na2CrO4溶液与锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL。
步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】亚硝酸钙 可作为混凝土防冻剂和钢筋阻锈剂的主要原料。熔点为
可作为混凝土防冻剂和钢筋阻锈剂的主要原料。熔点为 ,易潮解,易溶于水。实验室中,某兴趣小组根据反应
,易潮解,易溶于水。实验室中,某兴趣小组根据反应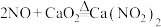 ,利用如下装置(部分装置可重复选用)制备无水亚硝酸钙并测定产品的纯度(夹持装置略)。
,利用如下装置(部分装置可重复选用)制备无水亚硝酸钙并测定产品的纯度(夹持装置略)。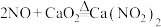 ;
;
②酸性条件下: 能被
能被 溶液氧化,
溶液氧化,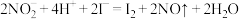 ;
;
③ 是具有氧化性的一元弱酸,
是具有氧化性的一元弱酸, 是一种难溶于水的白色化合物。
是一种难溶于水的白色化合物。
回答下列问题:
(1)上述装置按气流方向连接的顺序为_____ (填标号);装置A中发生反应的离子方程式为_____ ,装置 的作用是
的作用是_____ 。
(2) 完全还原后,进行操作:(ⅰ)停止滴加稀硝酸,停止通电;(ⅱ)……;(ⅲ)冷却后,将所得产品完全转移到试剂瓶中密封保存;(ⅳ)……操作(ⅱ)为
完全还原后,进行操作:(ⅰ)停止滴加稀硝酸,停止通电;(ⅱ)……;(ⅲ)冷却后,将所得产品完全转移到试剂瓶中密封保存;(ⅳ)……操作(ⅱ)为_____ 。
(3)兴趣小组同学认为制备的 可能会混有
可能会混有 ,下列试剂可以鉴别二者的是
,下列试剂可以鉴别二者的是_____ (填标号)。
A. 溶液 B.淀粉
溶液 B.淀粉 (酸性)溶液 C.
(酸性)溶液 C. 溶液
溶液
设计如下方案测定样品中的纯度(杂质不参与以下反应):称取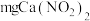 样品、溶解、定容至
样品、溶解、定容至 ;移取
;移取 溶液于锥形瓶中,加入过量酸化的
溶液于锥形瓶中,加入过量酸化的 溶液;以淀粉为指示剂,用
溶液;以淀粉为指示剂,用 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: 。平行滴定3次,平均消耗
。平行滴定3次,平均消耗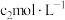 的标准液
的标准液 。
。
(4)测定过程所需仪器中,使用前必须检查是否漏液的有_____ ;样品中 的质量分数
的质量分数
_____ ;下列情况会导致 的质量分数测量值偏大的是
的质量分数测量值偏大的是_____ (填标号)。
A.称量后样品发生了潮解
B.定容时俯视刻度线
C.移取 溶液后发现滴定管尖嘴管内有气泡
溶液后发现滴定管尖嘴管内有气泡
D.滴定管用蒸馏水洗净后未用标准液润洗
 可作为混凝土防冻剂和钢筋阻锈剂的主要原料。熔点为
可作为混凝土防冻剂和钢筋阻锈剂的主要原料。熔点为 ,易潮解,易溶于水。实验室中,某兴趣小组根据反应
,易潮解,易溶于水。实验室中,某兴趣小组根据反应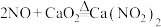 ,利用如下装置(部分装置可重复选用)制备无水亚硝酸钙并测定产品的纯度(夹持装置略)。
,利用如下装置(部分装置可重复选用)制备无水亚硝酸钙并测定产品的纯度(夹持装置略)。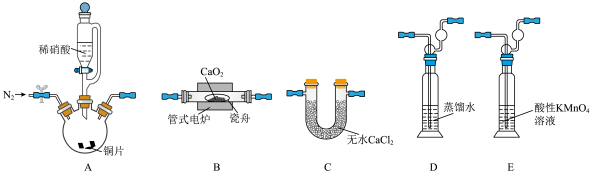
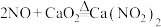 ;
;②酸性条件下:
 能被
能被 溶液氧化,
溶液氧化,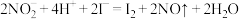 ;
;③
 是具有氧化性的一元弱酸,
是具有氧化性的一元弱酸, 是一种难溶于水的白色化合物。
是一种难溶于水的白色化合物。回答下列问题:
(1)上述装置按气流方向连接的顺序为
 的作用是
的作用是(2)
 完全还原后,进行操作:(ⅰ)停止滴加稀硝酸,停止通电;(ⅱ)……;(ⅲ)冷却后,将所得产品完全转移到试剂瓶中密封保存;(ⅳ)……操作(ⅱ)为
完全还原后,进行操作:(ⅰ)停止滴加稀硝酸,停止通电;(ⅱ)……;(ⅲ)冷却后,将所得产品完全转移到试剂瓶中密封保存;(ⅳ)……操作(ⅱ)为(3)兴趣小组同学认为制备的
 可能会混有
可能会混有 ,下列试剂可以鉴别二者的是
,下列试剂可以鉴别二者的是A.
 溶液 B.淀粉
溶液 B.淀粉 (酸性)溶液 C.
(酸性)溶液 C. 溶液
溶液设计如下方案测定样品中的纯度(杂质不参与以下反应):称取
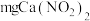 样品、溶解、定容至
样品、溶解、定容至 ;移取
;移取 溶液于锥形瓶中,加入过量酸化的
溶液于锥形瓶中,加入过量酸化的 溶液;以淀粉为指示剂,用
溶液;以淀粉为指示剂,用 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: 。平行滴定3次,平均消耗
。平行滴定3次,平均消耗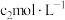 的标准液
的标准液 。
。(4)测定过程所需仪器中,使用前必须检查是否漏液的有
 的质量分数
的质量分数
 的质量分数测量值偏大的是
的质量分数测量值偏大的是A.称量后样品发生了潮解
B.定容时俯视刻度线
C.移取
 溶液后发现滴定管尖嘴管内有气泡
溶液后发现滴定管尖嘴管内有气泡D.滴定管用蒸馏水洗净后未用标准液润洗
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】某铜矿石的成分中含有Cu2O,还含有少量的Al2O3、Fe2O3和SiO2。某工厂利用此矿石炼制精铜的工艺流程示意图如下:
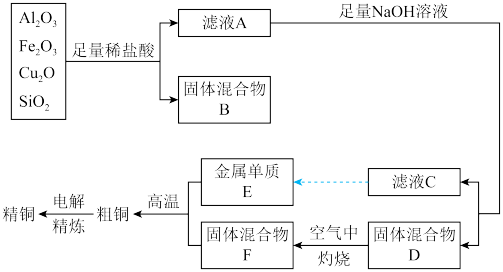
已知:CuO2+2H+=Cu+Cu2++H2O
(1)滤液A中铁元素的存在形式为______ (填离子符号),生成该离子的离子方程式为___________ ,检验滤液A中存在该离子的试剂为__________ (填试剂名称)。
(2)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为___________ 。
(3)常温下.等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH一)前者为后者的108倍,则两种溶液的pH=________________________ 。
(4)将Na2CO3溶液滴入到一定量的CuCl2溶液中,除得到蓝色沉淀,还有无色无味气体放出,写出相应的离子方程式:___________________________ 。
(5)①粗铜的电解精炼如图所示。在粗铜的电解精炼过程中,c为粗铜板,则a端应连接电源的_____ (填“正”或“负”)极,若粗铜中含有Au、Ag、Fe杂质,则电解过程中c电极上发生反应的方程式有_______ 、_______ 。
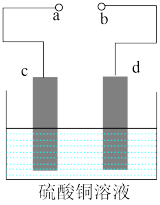
②可用酸性高锰酸钾溶液滴定法测定反应后电解液中铁元素的含量。滴定时不能用碱式滴定管盛放酸性高锰酸钾溶液的原因是______ 、滴定中发生反应的离子方程式为___________________ , 滴定时.锥形瓶中的溶液接触空气,则测得铁元素的含量会______ (填“偏高”或“偏低”)。

已知:CuO2+2H+=Cu+Cu2++H2O
(1)滤液A中铁元素的存在形式为
(2)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为
(3)常温下.等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH一)前者为后者的108倍,则两种溶液的pH=
(4)将Na2CO3溶液滴入到一定量的CuCl2溶液中,除得到蓝色沉淀,还有无色无味气体放出,写出相应的离子方程式:
(5)①粗铜的电解精炼如图所示。在粗铜的电解精炼过程中,c为粗铜板,则a端应连接电源的

②可用酸性高锰酸钾溶液滴定法测定反应后电解液中铁元素的含量。滴定时不能用碱式滴定管盛放酸性高锰酸钾溶液的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】CoCO3可用作选矿剂、催化剂及伪装涂料的颜料。以含钴废渣(主要成分为CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如图:
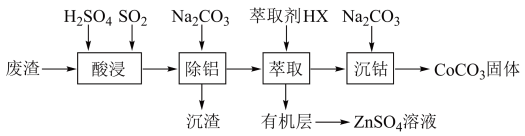
已知:①常温下,Ksp(CoCO3)=1.6×10-7
②相关金属离子[c(Mn+)=1.0mol•L-1]形成氢氧化物沉淀的pH范围如表:
(1)“酸浸”时加快溶解的方法有_______ (写出一种)。
(2)写出“酸浸”时发生氧化还原反应的化学方程式________ 。
(3)“除铝”过程中需要调节溶液pH的范围为_______ ,形成沉渣时发生反应的离子方程式为_______ 。
(4)“萃取”过程可表示为ZnSO4(水层)+2HX(有机层) ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是_______ 。
(5)“沉钴”时,Na2CO3溶液需缓慢滴加的原因是________ 。
(6)当Co2+沉淀完全时[c(Co2+)≤1×10-5mol•L-1],溶液中c(CO )至少应大于
)至少应大于_______ 。
(7)在空气中煅烧CoCO3生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴的氧化物的化学式为________ 。

已知:①常温下,Ksp(CoCO3)=1.6×10-7
②相关金属离子[c(Mn+)=1.0mol•L-1]形成氢氧化物沉淀的pH范围如表:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Co2+ | 7.6 | 9.4 |
| Al3+ | 3.0 | 5.0 |
| Zn2+ | 5.4 | 8.0 |
(1)“酸浸”时加快溶解的方法有
(2)写出“酸浸”时发生氧化还原反应的化学方程式
(3)“除铝”过程中需要调节溶液pH的范围为
(4)“萃取”过程可表示为ZnSO4(水层)+2HX(有机层)
 ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是(5)“沉钴”时,Na2CO3溶液需缓慢滴加的原因是
(6)当Co2+沉淀完全时[c(Co2+)≤1×10-5mol•L-1],溶液中c(CO
 )至少应大于
)至少应大于(7)在空气中煅烧CoCO3生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴的氧化物的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】甘氨酸亚铁(NH2CH2COO)2Fe[(NH2CH2COO)2Fe](Me = 204g/mol)可广泛用于缺铁性贫血的预防和治疗。某学习小组欲利用硫酸亚铁溶液与甘氨酸反应制备甘氨酸亚铁,实验过程如下:
步骤1 制备FeCO3:将100 mL 0.1 mol·L-1 FeSO4溶液与100 mL 0.2 mol·L-1 NH4HCO3溶液混合,反应结束后过滤并洗涤沉淀。
步骤2 制备 (NH2CH2COO)2Fe:实验装置如图,将步骤1得到的沉淀装入仪器B,利用装置A产生的CO2,将装置中空气排净后,逐滴滴入甘氨酸溶液,直至沉淀全部溶解,并稍过量。
步骤3 提纯 (NH2CH2COO)2Fe:反应结束后过滤,将滤液蒸发浓缩,加入乙醇,过滤、干燥得到产品。
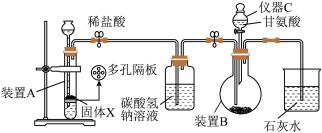
⑴固体X是______ ,仪器C的名称是______ 。
⑵碳酸氢钠溶液的作用是______ 。
⑶步骤1中,FeSO4溶液与NH4HCO3溶液混合时可观察到有白色沉淀和无色无味气体生成。该反应的化学方程式为______ 。
⑷步骤1中,检验FeCO3沉淀已洗净的操作是______ 。
⑸步骤2中当观察到现象是______ 时,可以开始滴加甘氨酸。
步骤1 制备FeCO3:将100 mL 0.1 mol·L-1 FeSO4溶液与100 mL 0.2 mol·L-1 NH4HCO3溶液混合,反应结束后过滤并洗涤沉淀。
步骤2 制备 (NH2CH2COO)2Fe:实验装置如图,将步骤1得到的沉淀装入仪器B,利用装置A产生的CO2,将装置中空气排净后,逐滴滴入甘氨酸溶液,直至沉淀全部溶解,并稍过量。
步骤3 提纯 (NH2CH2COO)2Fe:反应结束后过滤,将滤液蒸发浓缩,加入乙醇,过滤、干燥得到产品。

⑴固体X是
⑵碳酸氢钠溶液的作用是
⑶步骤1中,FeSO4溶液与NH4HCO3溶液混合时可观察到有白色沉淀和无色无味气体生成。该反应的化学方程式为
⑷步骤1中,检验FeCO3沉淀已洗净的操作是
⑸步骤2中当观察到现象是
您最近一年使用:0次



