下列说法正确的是
| A.反应物分子的每次碰撞都能发生化学反应 |
| B.活化分子之间的碰撞一定是有效碰撞 |
| C.能够发生化学反应的碰撞是有效碰撞 |
| D.增大反应物浓度时,活化分子百分数增大 |
16-17高二上·甘肃临夏·期末 查看更多[11]
江苏省天一中学2021-2022学年高二上学期期中考试化学试题甘肃省武威第十八中学2020-2021学年高二上学期期中考试化学试题甘肃省武威第八中学2020-2021学年高二上学期月考化学试题(已下线)2.1.2 活化能(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)山西省祁县第二中学校2019-2020学年高二上学期期中考试化学试题湖北省武汉市汉南区职教中心2019-2020学年高二上学期期中考试化学试题甘肃省天水市天水一中2019-2020学年高二(普通班)上学期第一次月考化学(理)试题辽宁省沈阳市东北育才学校2017-2018学年高二上学期期中考试化学试题辽宁省大连育明高级中学2018届高三人教版选修四9.7同步测试化学试题黑龙江省佳木斯市第一中学2016-2017学年高一下学期期末考试化学试题甘肃省临夏中学2016-2017学年高二上学期期末考试化学试题
更新时间:2017-06-14 21:26:22
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述,正确的是
A.pH=4的 溶液中, 溶液中,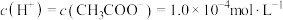 |
| B.升高温度能使化学反应速率加快,主要原因是增加了反应物分子中活化分子的百分数 |
| C.所有的化学反应都是由很多基元反应组成的 |
D.50℃时,pH=12的NaOH溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多 |
| D.催化剂不参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】保护环境,绿色发展,习主席代表我国承诺2060年前实现碳中和。科学家利用镍(Ni)及其他过渡金属配合物催化CO2和CH2=CH2氧化偶联合成丙烯酸,减少了CO2的排放,催化机理如图。下列说法错误的是
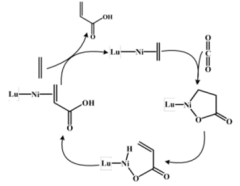

| A.丙烯酸易溶于水且能使溴水及高锰酸钾溶液褪色 |
| B.催化循环过程中包含加成反应 |
| C.该催化剂改变了反应的活化能,降低了焓变 |
D.总反应可表示为CH2=CH2+CO2 CH2=CHCOOH CH2=CHCOOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】CO与N2O在Fe+作用下发生反应的能量变化及反应历程如图所示,两步为①N2O+Fe+=N2+FeO+(慢)、②FeO++CO=CO2+Fe+(快)。下列说法正确的是


| A.总反应若在2L的密闭容器中进行,温度越高反应速率一定越快 |
| B.反应①的活化能比反应②大 |
| C.反应中每转移1mol电子,生成N2体积为11.2L |
| D.两步反应均为放热反应,总反应的化学反应速率由反应②决定 |
您最近一年使用:0次

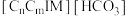 可在室温下以
可在室温下以 和
和 为原料合成DMC,具体流程如下(其中化合物①的1号C上没有H原子),下列说法
为原料合成DMC,具体流程如下(其中化合物①的1号C上没有H原子),下列说法
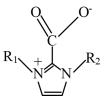
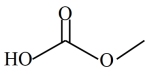
 (g)在催化剂
(g)在催化剂 (简写为HAP)表面催化生成
(简写为HAP)表面催化生成 的历程示意图如下。下列说法错误的是
的历程示意图如下。下列说法错误的是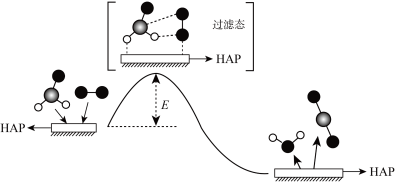
 反应物的键能总和-生成物的键能总和
反应物的键能总和-生成物的键能总和

