有A、B、C、D、E、F六种短周期的主族元素,原子序数依次增大,其中A、D元素的原子最外层均只有一个电子,且A和D可形成离子化合物;C、F同主族,B元素位于元素周期表中的第二周期,且原子最外层电子数占核外电子总数的3/4,F元素原子最外电子层比同周期E元素原子的最外电子层多5个电子。试回答:
(1)D、F两元素最高价氧化物的水化物之间发生的化学方程式是__________ 。
(2)D的氢氧化物和C的氢化物在水溶液中反应的离子方程式为__________ 。
(3)E的氢氧化物的电子式是______________ ;B的氢化物的电子式是______________ 。
(1)D、F两元素最高价氧化物的水化物之间发生的化学方程式是
(2)D的氢氧化物和C的氢化物在水溶液中反应的离子方程式为
(3)E的氢氧化物的电子式是
更新时间:2017-06-29 13:21:23
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】含硫化合物在生活和生产中有着重要应用,科学使用含硫化合物对人体健康及环境保护意义重大。
(1)葡萄酒中添加微量的SO2可抑制细菌生长,防止葡萄酒被__ (填“氧化”、“还原”)。
(2)氢的硫化物有多种:H2Sx(x=1,2,3,…),如H2S2,其结构与H2O2相似。请写出H2S3的结构式__ 。
(3)固体硫酸氢钾在加热熔化时,生成了焦硫酸钾(K2S2O7),反应中断裂的化学键类型为__ 。
(4)淮北某课题小组对连二亚硫酸钠(Na2S2O4)进行了如下探究。将0.050ml·L-1Na2S2O4溶液在空气中放置,其溶液的pH与时间(t)的关系如图所示(忽略溶液体积的变化)。
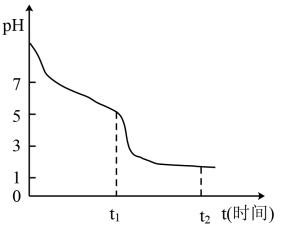
①Na2S2O4溶液显__ 性,原因是__ (用离子方程式表示)。
②t1时溶液中只有一种溶质,此时含硫元素的粒子浓度由大到小的顺序为___ 。
0-t1段发生反应的离子方程式为__ ,t1-t2段溶液的pH变小的原因是__ (用离子方程式表示)。
(1)葡萄酒中添加微量的SO2可抑制细菌生长,防止葡萄酒被
(2)氢的硫化物有多种:H2Sx(x=1,2,3,…),如H2S2,其结构与H2O2相似。请写出H2S3的结构式
(3)固体硫酸氢钾在加热熔化时,生成了焦硫酸钾(K2S2O7),反应中断裂的化学键类型为
(4)淮北某课题小组对连二亚硫酸钠(Na2S2O4)进行了如下探究。将0.050ml·L-1Na2S2O4溶液在空气中放置,其溶液的pH与时间(t)的关系如图所示(忽略溶液体积的变化)。

①Na2S2O4溶液显
②t1时溶液中只有一种溶质,此时含硫元素的粒子浓度由大到小的顺序为
0-t1段发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】在我国南方,遭遇冰雪灾害时常使用一种融雪剂,其主要成分的化学式为XY2,X、Y均为元素周期表前20号元素,X的阳离子和Y的阴离子电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂的化学式是__________________ ,该物质中化学键类型是________________ ,电子式是__________________
(2)D、E元素原子的最外层电子数是其电子层数的2倍,D与Y相邻,则元素D的阴离子结构示意图是________________ 。D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8电子稳定结构,该分子的电子式为____________________ 。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质与W的单质加热时生成物中化学键类型为__________ ,电子式为__________ 。
(1)该融雪剂的化学式是
(2)D、E元素原子的最外层电子数是其电子层数的2倍,D与Y相邻,则元素D的阴离子结构示意图是
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质与W的单质加热时生成物中化学键类型为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某课外活动小组利用下图所示装置探究甲烷与氯气的反应,回答下列问题:

(1)实验中可观察到的实验现象有:气体颜色逐渐变浅,量筒内壁出现油状液滴_______ ,_______ 等。
(2)反应后量筒内气体产物的电子式为____ ,油状液滴中非极性分子的空间构型为_____ 。
(3)实验室制备甲烷的反应方程式_______ 。
(4)从平衡移动的角度解释用排饱和食盐水的方法收集Cl2的原因_______ 。
(5)实验中生成的油状液滴中的氯仿能被空气氧化,产生剧毒气体——光气,反应的方程式为2CHCl3+O2=2COCl2+2HCl,为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是_______。
(6)若用乙烷代替甲烷进行实验,则有机产物有_______ 种。

(1)实验中可观察到的实验现象有:气体颜色逐渐变浅,量筒内壁出现油状液滴
(2)反应后量筒内气体产物的电子式为
(3)实验室制备甲烷的反应方程式
(4)从平衡移动的角度解释用排饱和食盐水的方法收集Cl2的原因
(5)实验中生成的油状液滴中的氯仿能被空气氧化,产生剧毒气体——光气,反应的方程式为2CHCl3+O2=2COCl2+2HCl,为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是_______。
| A.氢氧化钠溶液 | B.硝酸银溶液 | C.稀盐酸 | D.湿润的蓝色石蕊试纸 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为了测量NaHCO3和Na2CO3混合物中Na2CO3的质量分数。
方案一:有人设计了如下的装置。准确称取混合物样品m g盛于试管B中并连接装置,其中C、D为玻璃管,C带有刻度,回答下面有关小题。

(1)A装置的名称为_______
(2)C、D装置中的饱和X溶液应该选下列中的_______ (填序号)
a.NaOH溶液 b.蒸馏水 c.碳酸钠溶液 d.碳酸氢钠溶液
A中选用的试剂为稀H2SO4而不能选稀HCl的原因是_______ 。
(3)实验结束读数之前,要进行的操作是_______ 。
方案二:有同学经过思考提出,还可以通过如下方法测定组成,步骤为:
①称取一定量的混合物样品
②并向其中逐滴滴入0.1000 mol/L稀盐酸,记录生成的气体体积和滴入盐酸体积,如图所示:

(4)则生成CO2 在标况下的体积为_______ mL,该混合物中Na2CO3的质量分数_______ (保留两位小数)。
方案一:有人设计了如下的装置。准确称取混合物样品m g盛于试管B中并连接装置,其中C、D为玻璃管,C带有刻度,回答下面有关小题。

(1)A装置的名称为
(2)C、D装置中的饱和X溶液应该选下列中的
a.NaOH溶液 b.蒸馏水 c.碳酸钠溶液 d.碳酸氢钠溶液
A中选用的试剂为稀H2SO4而不能选稀HCl的原因是
(3)实验结束读数之前,要进行的操作是
方案二:有同学经过思考提出,还可以通过如下方法测定组成,步骤为:
①称取一定量的混合物样品
②并向其中逐滴滴入0.1000 mol/L稀盐酸,记录生成的气体体积和滴入盐酸体积,如图所示:

(4)则生成CO2 在标况下的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某兴趣小组同学制定如下三个方案对含有NaCl杂质的碳酸氢钠的含量进行测定:
方案一:用如图装置测定样品与足量酸反应生成CO2的体积。

(1)若实验测得样品中小苏打含量低于样品实际含量,可能的原因是 ___________。
方案二:测定上述样品中碳酸氢钠的质量分数还可通过如图装置进行测定。
(2)写出涉及的化学方程式__________ 。
(3)实际操作中还需要用到_______ (填仪器名称)。
方案三:通过以下流程测定样品中碳酸氢钠的含量。

(4)操作Ⅰ的名称为___________ ,根据以上实验过程,含有氯化钠的碳酸氢钠样品中碳酸氢钠的质量分数可表示为:___________ 。(样品为m1g,恒重后固体质量为m2g)
方案一:用如图装置测定样品与足量酸反应生成CO2的体积。

(1)若实验测得样品中小苏打含量低于样品实际含量,可能的原因是 ___________。
| A.CO2气体中含有水蒸气 | B.测定气体体积时未冷却至室温 |
| C.Y型管中留有反应生成的气体 | D.测定气体体积时水准管的液面高于量气管的液面 |
方案二:测定上述样品中碳酸氢钠的质量分数还可通过如图装置进行测定。

(2)写出涉及的化学方程式
(3)实际操作中还需要用到
方案三:通过以下流程测定样品中碳酸氢钠的含量。

(4)操作Ⅰ的名称为
您最近一年使用:0次
【推荐3】化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备NaHCO3,进一步处理得到产品Na2CO3和NH4Cl,实验流程如图:
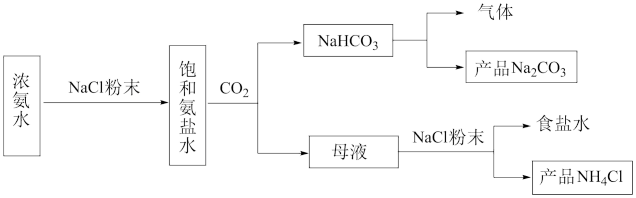
回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO3,正确的连接顺序是_______ (按气流方向,用小写字母表示)。为使A中分液漏斗内的稀盐酸顺利滴下,可将分液漏斗玻璃塞上的凹槽对准漏斗颈部的小孔或_______ 。
A.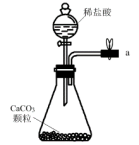 B.
B.  C.
C.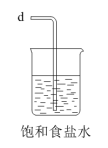 D.
D.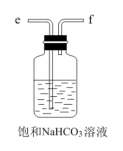 E.
E.
(2)B中使用雾化装置的优点是_______ 。
(3)生成NaHCO3的总反应的化学方程式为_______ 。
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液:
①对固体NaHCO3充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.14g,则固体NaHCO3的质量为_______ g。
②向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为_______ 、_______ 、过滤、洗涤、干燥。
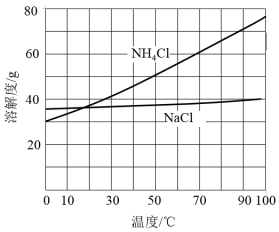
(5)将碳酸氢钠在300℃加热得到碳酸钠所选用的仪器是_______(填标号);
(6)无水NaHCO3可作为基准物质标定盐酸浓度,应选择指示剂_______ (选填“甲基橙”、“酚酞”、“石蕊”),称量前,若无水NaHCO3保存不当,吸收了一定量水分,用其标定盐酸浓度时,会使结果_______ (填标号)。
A.偏高 B.偏低 C.不变

回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO3,正确的连接顺序是
A.
 B.
B.  C.
C. D.
D. E.
E.
(2)B中使用雾化装置的优点是
(3)生成NaHCO3的总反应的化学方程式为
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液:
①对固体NaHCO3充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.14g,则固体NaHCO3的质量为
②向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为

(5)将碳酸氢钠在300℃加热得到碳酸钠所选用的仪器是_______(填标号);
A.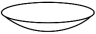 | B. | C. | D. |
A.偏高 B.偏低 C.不变
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】W、X、Y和Z都是周期表中前20号元素,其中W的原子序数均大于X、Y、Z,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是________ ;Z元素是________ 。
(2)化合物WY和WX2的化学式分别是____________ 和 ____________ 。
(3)写出Y和Z形成的两种常见化合物之一的分子式是________________ 。
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:____________________________________ 。
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是
(2)化合物WY和WX2的化学式分别是
(3)写出Y和Z形成的两种常见化合物之一的分子式是
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】几种短周期元素的原子半径及主要化合价如下表:已知 X 是短周期中最活泼的金属,且与 R 同周期。(请用化学用语答题)
(1)M 在元素周期表中的位置为___________ 。
(2)X 与 Y 按原子个数比 1∶1 构成的物质的电子式为___________ ;所含化学键类型为___________ 。
(3)X+、 Y2-、M2-离子半径从大到小的顺序为___________ 。
(4)将 YM2 通入 FeCl3 溶液中的离子方程式:___________ 。
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6,—2 | +5,—3 | —2 | +3 |
(2)X 与 Y 按原子个数比 1∶1 构成的物质的电子式为
(3)X+、 Y2-、M2-离子半径从大到小的顺序为
(4)将 YM2 通入 FeCl3 溶液中的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D、E、F、G 7种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是____ ,B位于周期表中位置 _________ ,C的原子结构示意图是________________ 。
(2)A元素与D元素形成的化合物的电子式是_________ 。
(3)G的单质与水反应的化学方程式是________ 。
(4)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是_____ (填化学式,下同),气态氢化物最稳定的是__________ 。
(5)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是_______________ 。
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是
(2)A元素与D元素形成的化合物的电子式是
(3)G的单质与水反应的化学方程式是
(4)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是
(5)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是
您最近一年使用:0次



