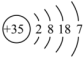
(1)下面是4种粒子的结构示意图:
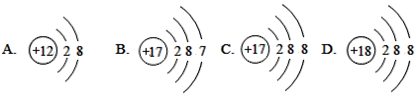
图中粒子共能表示_______ 种元素,图中表示的阳离子是____________ (用离子符号表示),图中A所表示的元素在元素周期表中的位置_____________________________ .
(2)在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
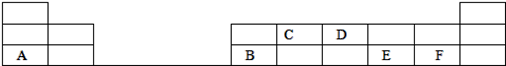
①写出D单质的电子式_____________________ ;
②写出C的最高价氧化物的结构式_____________________ ;
③E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)_____________________ ;
④A最高价氧化物的水化物所含化学键为___________________ ,其水溶液与B反应的离子方程式为___________________________ ;
(3)X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示.下列说法正确的是( )
A.金属性:N>Q
B.最高价氧化物对应水化物的酸性:M>Y
C.简单离子半径:Q>N>X
D.原子序数:Z>M>X>Y
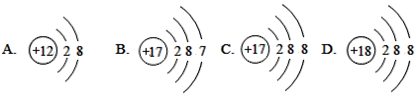
图中粒子共能表示
(2)在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:

①写出D单质的电子式
②写出C的最高价氧化物的结构式
③E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)
④A最高价氧化物的水化物所含化学键为
(3)X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示.下列说法正确的是
A.金属性:N>Q
B.最高价氧化物对应水化物的酸性:M>Y
C.简单离子半径:Q>N>X
D.原子序数:Z>M>X>Y
更新时间:2017-07-17 16:47:47
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】有A、B、C、D、E、F、G7种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是____ ,B位于周期表中第____ 周期____ 族,C的原子结构示意图是________________ 。
(2)E的单质颜色是_______ 。
(3)A元素与D元素形成的化合物的电子式是_________ 。
(4)G的单质与水反应的化学方程式是________ 。
(5)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是_____ (填化学式,下同),酸性最强的是_______ ,气态氢化物最稳定的是__________ 。
(6)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是_______________ 。
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是
(2)E的单质颜色是
(3)A元素与D元素形成的化合物的电子式是
(4)G的单质与水反应的化学方程式是
(5)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是
(6)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】元素周期表与元素周期律在学习、研究中有很重要的作用。表中是6种不同元素的相关信息,其中W、X、Y、Z位于短周期。请回答以下问题:
(1)元素W、X、Y最高价氧化物水化物的酸性由强到弱的顺序为_____ (填化学式)。与Y同主族元素硒Se位于Y的下一周期,则Se在元素周期表中的位置是_____ ,H2Se的电子式是_____ 。
(2)元素周期表中,同主族元素性质具有相似性和递变性,请写出元素Q的单质与水反应的离子方程式_____ 。Z与X分别形成的气态简单氢化物稳定性高的为_____ (填化学式)。
(3)海水中提取R的单质,将R-氧化为单质后,用空气将其吹入吸收塔中,与吸收剂SO2和水反应,则发生反应的离子的方程式是_____ ,由该反应可知SO2与Br-还原性强弱关系为_____ (用化学式表示)。
| 元素 | 元素相关信息 |
| W | 最高化合价+7价 |
| X | 原子最外层电子数是内层电子总数的一半,且为非金属元素 |
| Y | 原子M层比L层少2个电子 |
| Z | 原子获得3个电子达到8电子稳定结构 |
| Q | 焰色试验(透过蓝色钴玻璃观察)火焰呈紫色 |
| R | 原子结构示意图为: |
(2)元素周期表中,同主族元素性质具有相似性和递变性,请写出元素Q的单质与水反应的离子方程式
(3)海水中提取R的单质,将R-氧化为单质后,用空气将其吹入吸收塔中,与吸收剂SO2和水反应,则发生反应的离子的方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A、B、C、D、E、F是原子序数依次增大的前20号元素。元素A的周期数、主族序数、原子序数均相等;元素B的最高价氧化物对应水化物的化学式为HBO3;元素C与E同主族,且E元素原子的最外层电子数比次外层少2个,E、F两元素可形成化合物;D、E、F三种元素的最高价氧化物对应水化物之间可以两两反应。
(1)F在周期表中的位置为:___________ ,F2E中F离子的结构示意图为___________ 。
(2)气态化合物BA3的电子式为___________ ,空间构型为___________ ,将BA3通入滴有酚酞的水中,溶液变红,用电离方程式解释此现象___________ 。
(3)B、C、D三种元素的离子半径由大到小的顺序为:___________ (用离子符号表示)。
(4)E的一种同位素原子为33E,1mol33E的中子数为___________ 。
(1)F在周期表中的位置为:
(2)气态化合物BA3的电子式为
(3)B、C、D三种元素的离子半径由大到小的顺序为:
(4)E的一种同位素原子为33E,1mol33E的中子数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】元素周期表与元素周期律在学习、研究中有很重要的作用。表中是6种不同元素的相关信息,其中W、X、Y、Z位于短周期。请回答以下问题:
(1)元素W、X、Y最高价氧化物水化物的酸性由强到弱的顺序为_______ (填化学式)。与Y同主族元素硒Se位于Y的下一周期,则Se在元素周期表中的位置是_______ , 的电子式是
的电子式是_______ 。
(2)元素周期表中,同主族元素性质具有相似性和递变性,请写出元素Q的单质与水反应的离子方程式_______ 。Z与X分别形成的气态简单氢化物稳定性高的为_______ (填化学式)。
(3)海水中提取R的单质,将R氧化为单质后,用空气将其吹入吸收塔中,与吸收剂 和水反应,则发生反应的离子的方程式是
和水反应,则发生反应的离子的方程式是_______ 。
| 元素 | 元素相关信息 |
| W | 最高化合价+7价 |
| X | 原子最外层电子数是内层电子总数的一半,且为非金属元素 |
| Y | 原子M层比L层少2个电子 |
| Z | 原子获得3个电子达到8电子稳定结构 |
| Q | 焰色试验(透过蓝色钴玻璃观察)火焰呈紫色 |
| R | 原子结构示意图为: |
 的电子式是
的电子式是(2)元素周期表中,同主族元素性质具有相似性和递变性,请写出元素Q的单质与水反应的离子方程式
(3)海水中提取R的单质,将R氧化为单质后,用空气将其吹入吸收塔中,与吸收剂
 和水反应,则发生反应的离子的方程式是
和水反应,则发生反应的离子的方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表为元素周期表得一部分。
回答下列问题:
(1)X元素在周期表中位于_____ 周期_______ 族。
(2)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是____________ 。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(3)表中某元素的气态氢化物与该元素的最高价氧化物对应的水化物可以反应,写出该反应的化学方程式__________________ 。
(4)常温下,将稀氨水逐滴加入稀硫酸溶液中,当pH=7时,2c( )
)_______ c( )(填<、>、=)。
)(填<、>、=)。
(5)已知元素Na与元素Y可形成原子个数比为1∶1的离子化合物,写出该化合物的电子式_______ ,该化合物中的化学键类型有_____________ 。
(6)向Z单质的水溶液加入少量下列物质,能增强溶液漂白能力的是___________ 。
A.碳酸钙粉末 B.稀硫酸 C.氯化钙溶液 D.二氧化硫的水溶液
碳 | 氮 | Y | |
X | 硫 | Z |
(1)X元素在周期表中位于
(2)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(3)表中某元素的气态氢化物与该元素的最高价氧化物对应的水化物可以反应,写出该反应的化学方程式
(4)常温下,将稀氨水逐滴加入稀硫酸溶液中,当pH=7时,2c(
 )
) )(填<、>、=)。
)(填<、>、=)。(5)已知元素Na与元素Y可形成原子个数比为1∶1的离子化合物,写出该化合物的电子式
(6)向Z单质的水溶液加入少量下列物质,能增强溶液漂白能力的是
A.碳酸钙粉末 B.稀硫酸 C.氯化钙溶液 D.二氧化硫的水溶液
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素A、B、C、D、E、F均为前三周期主族元素,且原子序数依次增大。已知:B、E为同一主族元素,E原子的最外层电子数与次外层电子数之比为3∶4;C+、D3+、A+的离子半径逐渐减小,A原子半径最小。请回答下列问题:
(1)F元素在周期表中的位置为______ ,其最高价氧化物的水化物的化学式为_______ 。
(2)C+的结构示意图为_______ 。
(3)写出B、C、F按原子个数之比1∶1∶1形成的化合物的电子式:______ 。
(4)由元素A、B、C形成的化合物中含有的化学键是______ ,其与D的最高价氧化物的水化物反应的离子方程式为______ 。
(5)F的非金属性强于E的,下列能证明这一事实的是______ (填字母)。
(1)F元素在周期表中的位置为
(2)C+的结构示意图为
(3)写出B、C、F按原子个数之比1∶1∶1形成的化合物的电子式:
(4)由元素A、B、C形成的化合物中含有的化学键是
(5)F的非金属性强于E的,下列能证明这一事实的是
| A.常温下E的单质熔沸点比F单质的高 |
| B.F的简单氢化物比E的更稳定 |
| C.一定条件下,F和E的单质都能与NaOH溶液反应 |
| D.最高价氧化物对应水化物的酸性强弱:F>E |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图:______________ 。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式:__________________________ 。
(3)已知:As(s)+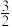 H2(g)+2O2(g)=H3AsO4(s) ΔH1;H2(g)+
H2(g)+2O2(g)=H3AsO4(s) ΔH1;H2(g)+ O2(g)=H2O(l) ΔH2;2As(s)+
O2(g)=H2O(l) ΔH2;2As(s)+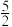 O2(g)=As2O5(s) ΔH3。则反应As2O5(s)+3H2O(l)=2H3AsO4(s)的ΔH=
O2(g)=As2O5(s) ΔH3。则反应As2O5(s)+3H2O(l)=2H3AsO4(s)的ΔH=________________________ 。
(4)298 K时,将20mL 3x mol·L-1Na2AsO3、20mL 3x mol·L-1 I2和20mL NaOH溶液混合,发生反应:AsO33- (aq)+I2(aq)+2OH-(aq)=AsO43- (aq)+2I-(aq)+H2O(l)。溶液中c(AsO43- )与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是________ (填选项字母)。
a.溶液的pH不再变化 b.v(I-)=2v(AsO33-)
c.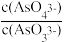 不再变化 d.c(I-)=y mol·L-1
不再变化 d.c(I-)=y mol·L-1
②tm时,v正______ v逆(填“大于”“小于”或“等于”)。
③tm时的v逆____ tn时的v逆(填“大于”“小于”或“等于”)。
(1)画出砷的原子结构示意图:
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式:
(3)已知:As(s)+
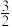 H2(g)+2O2(g)=H3AsO4(s) ΔH1;H2(g)+
H2(g)+2O2(g)=H3AsO4(s) ΔH1;H2(g)+ O2(g)=H2O(l) ΔH2;2As(s)+
O2(g)=H2O(l) ΔH2;2As(s)+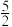 O2(g)=As2O5(s) ΔH3。则反应As2O5(s)+3H2O(l)=2H3AsO4(s)的ΔH=
O2(g)=As2O5(s) ΔH3。则反应As2O5(s)+3H2O(l)=2H3AsO4(s)的ΔH=(4)298 K时,将20mL 3x mol·L-1Na2AsO3、20mL 3x mol·L-1 I2和20mL NaOH溶液混合,发生反应:AsO33- (aq)+I2(aq)+2OH-(aq)=AsO43- (aq)+2I-(aq)+H2O(l)。溶液中c(AsO43- )与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是
a.溶液的pH不再变化 b.v(I-)=2v(AsO33-)
c.
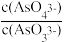 不再变化 d.c(I-)=y mol·L-1
不再变化 d.c(I-)=y mol·L-1②tm时,v正
③tm时的v逆
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】有A、B、C、D、E五种微粒:
I.A微粒不带电,其质量数为1;
II.B微粒呈电中性,得2个电子后,其电子层结构与Ne相同;
III.C微粒带有一个单位的正电荷,核电荷数为11;
IV.D微粒核内有14个中子,核外M层上有3个电子;
V.E微粒核外有18个电子,当失去一个电子时呈电中性。
(1)写出A微粒的符号_______ ,B微粒的结构示意图_______ ,C微粒的电子式_______ ,D微粒的质量数_______ ,E微粒的结构示意图_______ ;
(2)B、C、E所属三种元素可组成多种物质,请写出它们的化学式_______ 、_______ 。
I.A微粒不带电,其质量数为1;
II.B微粒呈电中性,得2个电子后,其电子层结构与Ne相同;
III.C微粒带有一个单位的正电荷,核电荷数为11;
IV.D微粒核内有14个中子,核外M层上有3个电子;
V.E微粒核外有18个电子,当失去一个电子时呈电中性。
(1)写出A微粒的符号
(2)B、C、E所属三种元素可组成多种物质,请写出它们的化学式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】A、B、C是三种元素的原子,质子数都小于18。A原子与B原子的最外层电子数都是6,A原子与C原子的核外电子层数都为3, C原子的质子数比A少4。回答下列问题:
(1)A、B的元素符号分别为___________________ 。
(2)A的离子结构示意图为_________ ;A与C组成的化合物为________ (用具体元素符号表示)。
(3)元素A的一种质量数为32的核素,与元素B的一种核素构成微粒为AB42-,1mol AB42-的质量为104g,则元素B的该核素中的中子数为_________ 。
(1)A、B的元素符号分别为
(2)A的离子结构示意图为
(3)元素A的一种质量数为32的核素,与元素B的一种核素构成微粒为AB42-,1mol AB42-的质量为104g,则元素B的该核素中的中子数为
您最近一年使用:0次