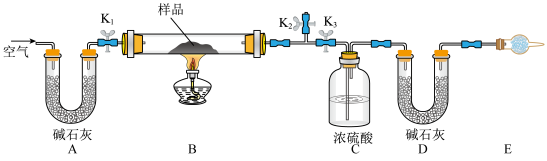
有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是____________________ 。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是______________________ 。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为________________________________________ 、_________________________________________ 。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是______________________ 。
②E处干燥管中盛放的药品是________ ,其作用是__________________ ________________ ,如果实验中没有该装置,则会导致测量结果NaHCO3的质量________ (填“偏大”、“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1 g、m2 g,则混合物中Na2CO3·10H2O的质量分数为________ (用含w、m1、m2的代数式表示)。
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是
②E处干燥管中盛放的药品是
③若样品质量为w g,反应后C、D装置增加的质量分别为m1 g、m2 g,则混合物中Na2CO3·10H2O的质量分数为
16-17高二下·河北邯郸·期末 查看更多[12]
河北省成安县第一中学2016-2017学年高二下学期期末考试化学试题2018版化学(苏教版)高考总复习课时跟踪训练:钠、镁及其重要化合物甘肃省兰州第一中学2018届高三上学期第二次月考(9月)化学试题甘肃省临夏中学2018届高三上学期期中考试化学试题安徽省滁州市民办高中2017-2018学年高一下学期第一次联考化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第1讲 钠及其氧化物【押题专练】(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第1讲 钠及化合物 (题型专练)(已下线)第07讲 钠及其重要化合物(精讲)-2022年一轮复习讲练测(已下线)专题三 金属及其化合物 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点05 钠及其化合物-备战2023年高考化学考试易错题浙江省宁波市九校联考2022-2023学年高一上学期期末考试化学试题(已下线)第三章 金属及其化合物 第12练 Na2CO3、NaHCO3碱金属
更新时间:2017-07-25 08:31:16
|
相似题推荐
【推荐1】高铝粉煤灰是火力发电厂燃煤锅炉排放出的固体废物,含有较多的 和
和 ,少量的MgO、铁的氧化物及其他不溶性杂质。从粉煤灰中提取
,少量的MgO、铁的氧化物及其他不溶性杂质。从粉煤灰中提取 的工艺流程如图:
的工艺流程如图:

已知: 不溶于水,也不溶于稀盐酸
不溶于水,也不溶于稀盐酸
(1)操作Ⅰ所用的玻璃仪器有:烧杯、______ 、______ 。
(2)滤渣1中除了其他不溶性杂质外,还有_____ (填化学式)。
(3)反应①的离子方程式为_______ ,检验生成物中阳离子的操作及现象是:_______ 。
(4)“沉铝”中反应的化学方程式为_______ 。
(5)沉铝后的滤液需要______ (选填“减压”、“常压”或“加压”)蒸发才能得到 固体;
固体;
(6)下列实验方案中,不能测定 和
和 混合物中
混合物中 质量分数的是_____。
质量分数的是_____。
 和
和 ,少量的MgO、铁的氧化物及其他不溶性杂质。从粉煤灰中提取
,少量的MgO、铁的氧化物及其他不溶性杂质。从粉煤灰中提取 的工艺流程如图:
的工艺流程如图:
已知:
 不溶于水,也不溶于稀盐酸
不溶于水,也不溶于稀盐酸(1)操作Ⅰ所用的玻璃仪器有:烧杯、
(2)滤渣1中除了其他不溶性杂质外,还有
(3)反应①的离子方程式为
(4)“沉铝”中反应的化学方程式为
(5)沉铝后的滤液需要
 固体;
固体;(6)下列实验方案中,不能测定
 和
和 混合物中
混合物中 质量分数的是_____。
质量分数的是_____。| A.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物充分加热,减重b克 |
D.取a克混合物与足量 溶液充分反应,过滤、洗涤、烘干,得b克固体 溶液充分反应,过滤、洗涤、烘干,得b克固体 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】铁、铝、钠是三种重要的金属。回答下列问题:
Ⅰ.氢氧化亚铁浊液在空气中放置会发生一系列颜色变化。
(1)写出该反应的化学方程式_________________ 。
Ⅱ.KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如图所示:

(2)试剂①应选用________ (填字母),反应的化学方程式为_______ 。
A.HCl溶液 B.H2SO4溶液
C.氨水 D.NaOH溶液
(3)请写出向滤液A中通入足量的CO2除得到沉淀B的离子反应方程式_________________ 。
Ⅲ.现有一不纯的小苏打样品(含杂质NaCl、Na2CO3·10H2O),为测定NaHCO3的质量分数,设计如图所示的实验装置(部分夹持仪器未画出)。

实验步骤如下:
①按图组装好实验装置并检查气密性。
②称取定质量的样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟。
④关闭活塞K1、K2打开K3,点燃酒精灯加热至不再产生气体。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量
(4)若无装置E,则会导致测得NaHCO3的质量分数________________ (填“偏大”、“偏小”或“无影响”)。
(5)步骤③的目的是________________ 。
(6)若实验中称取样品的质量为 50.0 g,反应后C、D装置增加的质量分别为 12.6 g、8.8 g,则混合物中NaHCO3的质量分数为________________ 。
Ⅰ.氢氧化亚铁浊液在空气中放置会发生一系列颜色变化。
(1)写出该反应的化学方程式
Ⅱ.KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如图所示:

(2)试剂①应选用
A.HCl溶液 B.H2SO4溶液
C.氨水 D.NaOH溶液
(3)请写出向滤液A中通入足量的CO2除得到沉淀B的离子反应方程式
Ⅲ.现有一不纯的小苏打样品(含杂质NaCl、Na2CO3·10H2O),为测定NaHCO3的质量分数,设计如图所示的实验装置(部分夹持仪器未画出)。

实验步骤如下:
①按图组装好实验装置并检查气密性。
②称取定质量的样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟。
④关闭活塞K1、K2打开K3,点燃酒精灯加热至不再产生气体。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量
(4)若无装置E,则会导致测得NaHCO3的质量分数
(5)步骤③的目的是
(6)若实验中称取样品的质量为 50.0 g,反应后C、D装置增加的质量分别为 12.6 g、8.8 g,则混合物中NaHCO3的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某 固体样品中含有
固体样品中含有 杂质,为测定样品中
杂质,为测定样品中 的含量,某实验小组称取ag样品进行测定。回答下列问题:
的含量,某实验小组称取ag样品进行测定。回答下列问题:

(1)装置A中反应的化学方程式为_______ ;装置B的名称为_______ 。
(2)甲同学拟通过测定 的质量来计算样品中
的质量来计算样品中 含量,仪器的连接顺序为
含量,仪器的连接顺序为_______ (每组装置仅使用一次)。
(3)乙同学拟选取A→C→B装置完成测定,则B装置中加入的试剂为_______ 。若C的质量变化为bg,则样品中 的质量分数为
的质量分数为_______ 。若无B装置会使测量结果_______ (填“偏大”、“偏小”或“无影响”)。
(4)老师指出上述方案均会导致测定结果偏小,应将A装置更换为以下装置:
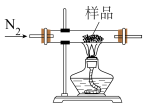
请说明原因_______ 。
 固体样品中含有
固体样品中含有 杂质,为测定样品中
杂质,为测定样品中 的含量,某实验小组称取ag样品进行测定。回答下列问题:
的含量,某实验小组称取ag样品进行测定。回答下列问题:
(1)装置A中反应的化学方程式为
(2)甲同学拟通过测定
 的质量来计算样品中
的质量来计算样品中 含量,仪器的连接顺序为
含量,仪器的连接顺序为(3)乙同学拟选取A→C→B装置完成测定,则B装置中加入的试剂为
 的质量分数为
的质量分数为(4)老师指出上述方案均会导致测定结果偏小,应将A装置更换为以下装置:

请说明原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】固体化合物X(式量小于200)由1-20号的4种元素组成,某小组开展如下探究实验气体体积都在标准状况下测定。请回答:

(1)气体B的的结构式为_______ ;白色固体C的名称是_______ ;
(2)化合物X的化学式是_______ ;
(3)气体B与红棕色固体H在加热条件下反应的化学方程式_______ ;
(4)设计实验验证溶液F中可能含有的金属阳离子_______ 。

(1)气体B的的结构式为
(2)化合物X的化学式是
(3)气体B与红棕色固体H在加热条件下反应的化学方程式
(4)设计实验验证溶液F中可能含有的金属阳离子
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:

查阅资料:Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡。(Sn: 119)
回答下列问题:
(1) 操作Ⅰ是________ 、过滤洗涤。
(2)SnCl2粉末需加浓盐酸进行溶解,目的是_______________________________ 。
(3)加入Sn粉的作用有两个:①调节溶液pH,②____________________________ 。[
(4)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是___________________ 。
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl SnCl2 + H2↑;
SnCl2 + H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:
6FeCl2 + K2Cr2O7 + 14HCl 6FeCl3 + 2KCl + 2CrCl3 +7H2O
6FeCl3 + 2KCl + 2CrCl3 +7H2O
现取0.80 g锡粉,经上述各步反应后,共用去0.1000 mol/L K2Cr2O7溶液20.00mL。则锡粉中锡的纯度为_______________ 。

查阅资料:Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡。(Sn: 119)
回答下列问题:
(1) 操作Ⅰ是
(2)SnCl2粉末需加浓盐酸进行溶解,目的是
(3)加入Sn粉的作用有两个:①调节溶液pH,②
(4)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是
(5)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl
 SnCl2 + H2↑;
SnCl2 + H2↑;②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:
6FeCl2 + K2Cr2O7 + 14HCl
 6FeCl3 + 2KCl + 2CrCl3 +7H2O
6FeCl3 + 2KCl + 2CrCl3 +7H2O现取0.80 g锡粉,经上述各步反应后,共用去0.1000 mol/L K2Cr2O7溶液20.00mL。则锡粉中锡的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
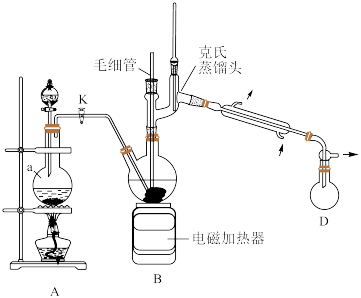
【推荐3】叠氮化钠(NaN3)是一种重要的化学分析试剂,已知NaN3无色无味,微溶于醇、易溶于水,在40℃以上会发生分解。实验室模仿工业“亚硝酸甲酯-水合肼法”制备NaN3,装置如图所示,基本操作如下:
步骤2:生成的亚硝酸甲酯(CH3ONO)蒸气通入到水合肼(N2H4·H2O)的烧碱溶液中,通过电磁加热器加热,生成叠氮化钠;
步骤3:减压蒸馏,回收甲醇;
步骤4:蒸馏后所得母液,冷却结晶、过滤、洗涤、干燥,得到叠氮化钠。
回答下列问题:
(1)仪器a的名称为___________ ;写出装置A中生成CH3ONO的化学方程式:___________ 。
(2)写出装置B中生成NaN3的化学方程式:___________ 。
(3)装置B反应结束后需采用减压蒸馏回收甲醇,不宜直接蒸馏的原因是___________ ;减压蒸馏中使用毛细管的优点是___________ 。
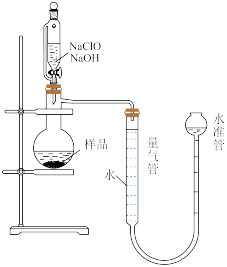
(4)量气法可有效测定产品的纯度,装置如图所示。___________ ;反应结束后水准管中液面会高于量气管,此时需要将水准管慢慢向下移动,则量气管中的液面会___________ (填“上移”“下移”或“不移动”),该产品的纯度(质量分数)为___________ (用含m、V的表达式表示)。
步骤2:生成的亚硝酸甲酯(CH3ONO)蒸气通入到水合肼(N2H4·H2O)的烧碱溶液中,通过电磁加热器加热,生成叠氮化钠;
步骤3:减压蒸馏,回收甲醇;
步骤4:蒸馏后所得母液,冷却结晶、过滤、洗涤、干燥,得到叠氮化钠。
回答下列问题:
(1)仪器a的名称为
(2)写出装置B中生成NaN3的化学方程式:
(3)装置B反应结束后需采用减压蒸馏回收甲醇,不宜直接蒸馏的原因是
(4)量气法可有效测定产品的纯度,装置如图所示。
您最近一年使用:0次



