某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是____________ 。
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式:
B_________ ;D ___________ ;E__________ 。
(3)写出①、③反应方程式①_________________ ,③_____________________ 。

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式:
B
(3)写出①、③反应方程式①
更新时间:2017-07-10 14:46:47
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E五种常见物质燃烧或灼烧时火焰都呈黄色,A、B分别与水反应都有气体放出,同时都生成C溶液,A与水反应放出的气体具有可燃性,B与水反应放出的气体能够助燃,C与适量的F气体反应生成D,D溶液与F气体反应生成E,E加热能够生成D和F气体。
根据以上叙述回答下列问题:
(1)写出下列物质的化学式:A____ ,B____ ,C____ ,D____ 。
(2)按要求完成方程式:
①加热E生成D和F的化学方程式______________________________ 。
②C溶液和CO2反应生成D的离子方程式____________________________ 。
根据以上叙述回答下列问题:
(1)写出下列物质的化学式:A
(2)按要求完成方程式:
①加热E生成D和F的化学方程式
②C溶液和CO2反应生成D的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下列图示中A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们之间相互转化关系如图。

(1)写出下列物质的化学式:A______ ,D_____________ 。
(2)以上反应中,属于氧化还原反应的有_________ (填序号)。
(3)①A→C反应的离子方程式:______________ 。
②C→D反应的离子方程式:________________ 。

(1)写出下列物质的化学式:A
(2)以上反应中,属于氧化还原反应的有
(3)①A→C反应的离子方程式:
②C→D反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)向碳酸钠的浓溶液中逐滴加入稀盐酸,直到不再产生CO2气体为止,在此过程中,溶液中的碳酸氢根离子浓度的变化是___________。
(2)有含21.2gNa2CO3和含10.95gHCl的两种溶液中:①将Na2CO3溶液逐滴加入HCl溶液中;②将HCl溶液逐滴加入Na2CO3溶液中。①②两种操作生成的CO2的质量之比为___________ 。
(3)已知固体混合物A由NaHCO3、KHCO3、MgCO3、CaCO3四种物质中的两种混合而成。请通过计算和推理完成下列各小题:
①取A与足量的盐酸反应:若固体混合物A的质量m(A)为定值,生成气体的量为定值,则A的可能组成是(填写化学式):___________ 、___________ ;___________ 、___________ ;(可以不填满)
②若先将A加热,剩余固体再与足量的盐酸反应,且先后两次产生的气体分别通过足量的澄清石灰水生成的沉淀均为10.0g,则混合固体A中碳元素的总质量是___________ g。
(1)向碳酸钠的浓溶液中逐滴加入稀盐酸,直到不再产生CO2气体为止,在此过程中,溶液中的碳酸氢根离子浓度的变化是___________。
| A.先变大后变小 | B.先变小后变大 | C.一直变小 | D.保持不变 |
(3)已知固体混合物A由NaHCO3、KHCO3、MgCO3、CaCO3四种物质中的两种混合而成。请通过计算和推理完成下列各小题:
①取A与足量的盐酸反应:若固体混合物A的质量m(A)为定值,生成气体的量为定值,则A的可能组成是(填写化学式):
②若先将A加热,剩余固体再与足量的盐酸反应,且先后两次产生的气体分别通过足量的澄清石灰水生成的沉淀均为10.0g,则混合固体A中碳元素的总质量是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】宏观辨识与微观探析是化学学科重要的学科素养。回答下列问题:
Ⅰ.已知某无色水样中只含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种。某化学研究性学习小组对该水样的成分进行检验:
中的若干种。某化学研究性学习小组对该水样的成分进行检验:
①取部分水样;
②向水样中滴加足量硝酸钡溶液,产生白色沉淀;
③向步骤②所得沉淀中滴加足量稀盐酸,沉淀部分溶解;
④向步骤③所得溶液中滴加硝酸银溶液,又产生白色沉淀。
(1)该水样中一定存在的离子是__________ (填离子符号,下同),可能存在的离子是__________ ,一定不存在的离子是__________ 。
(2)若要确定可能存在的离子是否存在,还需进行的实验操作是__________ 。
Ⅱ.现有 、
、 、
、 、
、 四种溶液,该小组同学设计如下实验步骤进行鉴别:
四种溶液,该小组同学设计如下实验步骤进行鉴别:
①取等体积的上述四种溶液A、B、C、D分别置于四支试管中,对四支试管均进行下列操作:加入过量的 溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
②向①中反应后的四支试管中,分别依次加入足量 溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
(3)溶液A、B、C、D中的溶质依次为__________ 、__________ 、__________ 、__________ (填化学式)。
(4)有同学提出用一种试剂即可将四种溶液鉴别出来,该试剂为__________ (填化学式)。
Ⅰ.已知某无色水样中只含有
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种。某化学研究性学习小组对该水样的成分进行检验:
中的若干种。某化学研究性学习小组对该水样的成分进行检验:①取部分水样;
②向水样中滴加足量硝酸钡溶液,产生白色沉淀;
③向步骤②所得沉淀中滴加足量稀盐酸,沉淀部分溶解;
④向步骤③所得溶液中滴加硝酸银溶液,又产生白色沉淀。
(1)该水样中一定存在的离子是
(2)若要确定可能存在的离子是否存在,还需进行的实验操作是
Ⅱ.现有
 、
、 、
、 、
、 四种溶液,该小组同学设计如下实验步骤进行鉴别:
四种溶液,该小组同学设计如下实验步骤进行鉴别:①取等体积的上述四种溶液A、B、C、D分别置于四支试管中,对四支试管均进行下列操作:加入过量的
 溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。②向①中反应后的四支试管中,分别依次加入足量
 溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
溶液,观察到盛装B、C溶液的试管内产生白色沉淀。(3)溶液A、B、C、D中的溶质依次为
(4)有同学提出用一种试剂即可将四种溶液鉴别出来,该试剂为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】磁性物质X只含两种元素,属于半金属材料。某兴趣小组对化合物X的组成展开如下探究(图中部分产物未标出)。

请回答:
(1)固体X含有的元素是______ (用元素符号表示),其化学式为_______ 。
(2)写出溶液A与NaOH溶液产生气体B的离子方程式_______ 。
(3)设计实验检验溶液A中阴离子的方法_______ 。

请回答:
(1)固体X含有的元素是
(2)写出溶液A与NaOH溶液产生气体B的离子方程式
(3)设计实验检验溶液A中阴离子的方法
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】高氯酸铵(NH4ClO4)是复合火箭推进剂的重要成分。
(1)NaClO4溶液和NH4Cl溶液混合后发生复分解反应,有NH4ClO4固体析出,写出该反应的化学方程式:____ 。
(2)通过如下图所示的装置及实验步骤可以测定某高氯酸铵样品的纯度。
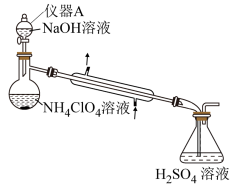
步骤1:检查装置气密性。
步骤2:准确称取样品0.2500 g于蒸馏烧瓶中,加入约150 mL水溶解。
步骤3:准确量取40.00 mL 0.1000 mol·L—1 H2SO4 溶液于锥形瓶中。
步骤4:经仪器A向蒸馏瓶中加入20 mL 3 mol·L—1NaOH 溶液。
步骤5:加热蒸馏至蒸馏烧瓶中剩余约100 mL溶液。
步骤6:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤7:向锥形瓶中加入酸碱指示剂,用0.2000mol·L—1 NaOH标准溶液滴定至终点,消耗NaOH标准溶液30.00 mL。
步骤8:将实验步骤1~7重复2次。
①仪器A的名称是____ 。
②步骤1~7中,确保生成的氨被稀硫酸完全吸收的实验步骤是____ (填步骤序号)。
③计算样品中高氯酸铵的质量分数____ (写出计算过程,已知杂质不参与反应)。
(1)NaClO4溶液和NH4Cl溶液混合后发生复分解反应,有NH4ClO4固体析出,写出该反应的化学方程式:
(2)通过如下图所示的装置及实验步骤可以测定某高氯酸铵样品的纯度。

步骤1:检查装置气密性。
步骤2:准确称取样品0.2500 g于蒸馏烧瓶中,加入约150 mL水溶解。
步骤3:准确量取40.00 mL 0.1000 mol·L—1 H2SO4 溶液于锥形瓶中。
步骤4:经仪器A向蒸馏瓶中加入20 mL 3 mol·L—1NaOH 溶液。
步骤5:加热蒸馏至蒸馏烧瓶中剩余约100 mL溶液。
步骤6:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤7:向锥形瓶中加入酸碱指示剂,用0.2000mol·L—1 NaOH标准溶液滴定至终点,消耗NaOH标准溶液30.00 mL。
步骤8:将实验步骤1~7重复2次。
①仪器A的名称是
②步骤1~7中,确保生成的氨被稀硫酸完全吸收的实验步骤是
③计算样品中高氯酸铵的质量分数
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A是一种红棕色金属氧化物,B、G是金属单质,F是一种难溶于水的白色化合物,受热后容易发生分解。

(1)写出下列物质的化学式:A:___ E:___ F:___ H:__ 。
(2)按要求写方程式:
①H与氨水反应的离子方程式:___ 。
②B与氢氧化钠溶液反应的离子方程式:___ 。
③I在空气中转化为J的化学方程式:___ 。

(1)写出下列物质的化学式:A:
(2)按要求写方程式:
①H与氨水反应的离子方程式:
②B与氢氧化钠溶液反应的离子方程式:
③I在空气中转化为J的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
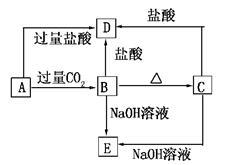
(1)写出化学式:A__________ ,B____________ ,
C____________ ,D____________ ,E____________ 。
(2)写出下列反应的离子方程式:
A→B_______________________________________
A→D_______________________________________
(3)写出下列方程式
C→E_______________________________________

(1)写出化学式:A
C
(2)写出下列反应的离子方程式:
A→B
A→D
(3)写出下列方程式
C→E
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】从铝土矿(主要成分为Al2O3,还有少量杂质)中提取铝的工艺流程及步骤如下:
试回答下列问题。
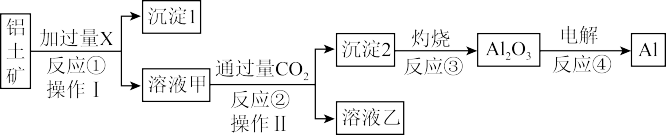
(1)试剂X为___ ;反应①的离子方程式为___ 。
(2)操作Ⅰ、操作Ⅱ均为___ (填操作名称)。反应①②③④中属于氧化还原反应的是___ (填数字序号)。
(3)反应②的离子方程式为___ 。
(4)金属铝与氧化铁的混合物在高温下会发生剧烈的反应,该反应的化学方程式为___ 。
(5)电解熔融氧化铝制取金属铝,若有0.6mol电子发生转移,理论上能得到金属铝的质量是___ g。
试回答下列问题。

(1)试剂X为
(2)操作Ⅰ、操作Ⅱ均为
(3)反应②的离子方程式为
(4)金属铝与氧化铁的混合物在高温下会发生剧烈的反应,该反应的化学方程式为
(5)电解熔融氧化铝制取金属铝,若有0.6mol电子发生转移,理论上能得到金属铝的质量是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。
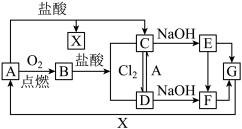
(1)写出A、C、F、G的化学式:A_______ ,C_______ ,F_______ ,G_______ 。
(2)写出B与盐酸反应的离子方程式_______
(3)检验D中阳离子的方法_______ 。
(4)制取F胶体的方法_______ 。
(5)①写出下列转化的离子方程式C→D:_______ ,
②由E转化为F的现象是_______ 。
③并写出的化学方程式E→F:_______

(1)写出A、C、F、G的化学式:A
(2)写出B与盐酸反应的离子方程式
(3)检验D中阳离子的方法
(4)制取F胶体的方法
(5)①写出下列转化的离子方程式C→D:
②由E转化为F的现象是
③并写出的化学方程式E→F:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】煤矸石是采煤过程和洗煤过程中排放的固体废物,其主要成分是Al2O3、SiO2,此外还含有FeO、Fe2O3等杂质。煤矸石经处理后,可用于制备铵明矾等。
已知:i.SiO2不与硫酸反应;Al2O3能与H2SO4反应。
ii.Fe3+、Fe2+、Al3+开始沉淀、完全沉淀的pH如表所示。
iii.NH4Al(SO4)2·12H2O的摩尔质量为453g·mol-1。

(1)酸浸过程中,Fe2O3与硫酸反应的离子方程式为___________
(2)下列说法中,正确的是___________ (填字母)。
a.预处理时,粉碎煤矸石有利于提高酸浸反应速率 b.操作I是过滤 c.滤渣1中一定含有硅元素
(3)沉铁过程中,加入氧化剂的作用是___________
(4)制备过程中,若需检验滤渣1中含有 ,实验方案为:取少量滤渣1的洗涤液,向其中加入
,实验方案为:取少量滤渣1的洗涤液,向其中加入___________ (填试剂和现象),说明其中含有 。
。
已知:i.SiO2不与硫酸反应;Al2O3能与H2SO4反应。
ii.Fe3+、Fe2+、Al3+开始沉淀、完全沉淀的pH如表所示。
| Fe2+ | Fe3+ | Al3+ | |
| 开始沉淀的pH | 6.3 | 1.5 | 3.4 |
| 完全沉淀的pH | 8.3 | 2.8 | 4.7 |
iii.NH4Al(SO4)2·12H2O的摩尔质量为453g·mol-1。

(1)酸浸过程中,Fe2O3与硫酸反应的离子方程式为
(2)下列说法中,正确的是
a.预处理时,粉碎煤矸石有利于提高酸浸反应速率 b.操作I是过滤 c.滤渣1中一定含有硅元素
(3)沉铁过程中,加入氧化剂的作用是
(4)制备过程中,若需检验滤渣1中含有
 ,实验方案为:取少量滤渣1的洗涤液,向其中加入
,实验方案为:取少量滤渣1的洗涤液,向其中加入 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某研究性学习小组在进行铁与水蒸气反应所得固体物质的成分、性质及再利用的实验探究,请回答下列问题:
探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。
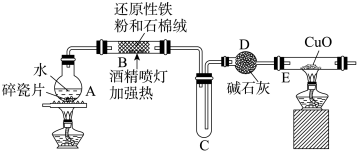
(1)硬质玻璃管B中发生反应的化学方程式为____ 。
(2)装置D的作用是____ 。
探究二:待硬质玻璃管B冷却后,取少许其中的固体继续进行如图实验,确定反应后硬质玻璃管B中黑色固体的成分。
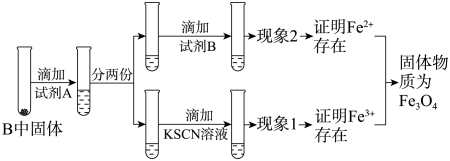
(3)试剂B是____ ,现象2为____ 。
(4)若现象1为溶液未变红色,请从硬质玻璃管B中固体物质的成分分析可能的原因:____ 。
探究三:按照如图实验流程用硬质玻璃管B中固体制备Fe3O4纳米材料。
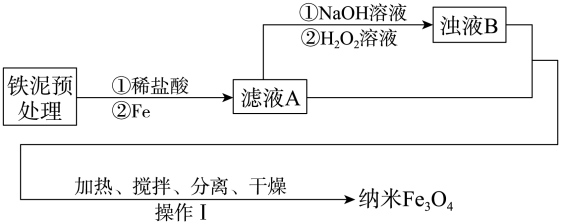
已知:①浊液B中铁元素以FeOOH形式存在;
②在操作I中,相同条件下测得Fe3O4的产率与R[R=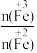 ]的关系如图所示。
]的关系如图所示。
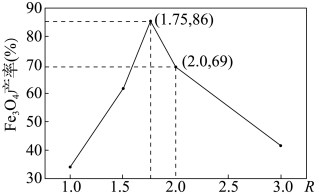
(5)在滤液A转化为浊液B反应完成后需再加热一段时间除去剩余H2O2,目的是____ 。
(6)设浊液B中FeOOH的物质的量为amol,滤液A中的n(Fe)=bmol。为使Fe3O4的产率最高,则 =
=___ 。(填数值,保留3位小数)
探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。

(1)硬质玻璃管B中发生反应的化学方程式为
(2)装置D的作用是
探究二:待硬质玻璃管B冷却后,取少许其中的固体继续进行如图实验,确定反应后硬质玻璃管B中黑色固体的成分。

(3)试剂B是
(4)若现象1为溶液未变红色,请从硬质玻璃管B中固体物质的成分分析可能的原因:
探究三:按照如图实验流程用硬质玻璃管B中固体制备Fe3O4纳米材料。

已知:①浊液B中铁元素以FeOOH形式存在;
②在操作I中,相同条件下测得Fe3O4的产率与R[R=
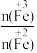 ]的关系如图所示。
]的关系如图所示。
(5)在滤液A转化为浊液B反应完成后需再加热一段时间除去剩余H2O2,目的是
(6)设浊液B中FeOOH的物质的量为amol,滤液A中的n(Fe)=bmol。为使Fe3O4的产率最高,则
 =
=
您最近一年使用:0次



