(1)请选择合适方法的填空(用字母序号填空):
A.过滤 B.裂解 C.分馏 D.裂化 E.干馏 F.还原 G.电解 H.蒸发
①从海水中提取粗盐__________________ ; ②重油转变为汽油_____________ ;
③石油炼制乙烯、丙烯等__________ ; ④煤转化为焦炭、煤焦油等____________ 。
(2)对于容积固定的反应:N2(g)+3H2(g) 2NH3(g)(正反应放热),达到平衡的标志有
2NH3(g)(正反应放热),达到平衡的标志有__________ 。
A.N2、H2、NH3 的百分含量不再变化 B.总压强不变
C.N2、H2、NH3 的分子数之比为 1∶3∶2 D.N2、H2、NH3 的浓度相等
E.N2、H2 不再起反应 F.v(N2)=v(H2)
A.过滤 B.裂解 C.分馏 D.裂化 E.干馏 F.还原 G.电解 H.蒸发
①从海水中提取粗盐
③石油炼制乙烯、丙烯等
(2)对于容积固定的反应:N2(g)+3H2(g)
 2NH3(g)(正反应放热),达到平衡的标志有
2NH3(g)(正反应放热),达到平衡的标志有A.N2、H2、NH3 的百分含量不再变化 B.总压强不变
C.N2、H2、NH3 的分子数之比为 1∶3∶2 D.N2、H2、NH3 的浓度相等
E.N2、H2 不再起反应 F.v(N2)=v(H2)
G.混合气体的密度不变 H.混合气体的平均相对分子质量不变
I.正反应放出的热量等于逆反应吸收的热量
更新时间:2017-09-10 06:52:59
|
相似题推荐
【推荐1】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。__ PB(填“>、<、=”)。
②A、B、C三点的平衡常数KA,KB,KC的大小关系是__ 。
③下列叙述能说明上述反应能达到化学平衡状态的是__ (填代号)。
a.H2的消耗速率是CH3OH消耗速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
(2)在P1压强、T1℃时,该反应的平衡常数K=__ ,再加入1.0molCO后重新到达平衡,则CO的转化率__ (填“增大,不变或减小”)。
(3)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)__ v(逆)(填“>、<或=”)。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。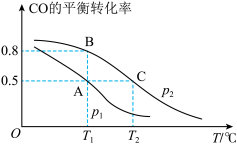
②A、B、C三点的平衡常数KA,KB,KC的大小关系是
③下列叙述能说明上述反应能达到化学平衡状态的是
a.H2的消耗速率是CH3OH消耗速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
(2)在P1压强、T1℃时,该反应的平衡常数K=
(3)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)
您最近一年使用:0次
【推荐2】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)已知:K300℃>K350℃,写出该反应的平衡常数表达式:K=_________________ 。关于该反应的下列说法中,正确的是________ 。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)下图中表示NO2的变化的曲线是____________________ 。用O2表示从0-2s内该反应的平均速率v=_______________ 。
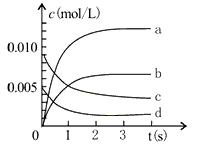
(3)能说明该反应已达到平衡状态的是__________ 。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v 逆(NO)=2v正 (O2) D.容器内密度保持不变
(4)下列措施中能使n(NO2)/n(NO)增大的有____ 。(填字母)
A.升高温度 B.加入催化剂
C.不断充入O2 D.充入He(g),使体系总压强增大
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01. | 0.008 | 0.007 | 0.007 | 0.007 |
(1)已知:K300℃>K350℃,写出该反应的平衡常数表达式:K=
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)下图中表示NO2的变化的曲线是

(3)能说明该反应已达到平衡状态的是
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v 逆(NO)=2v正 (O2) D.容器内密度保持不变
(4)下列措施中能使n(NO2)/n(NO)增大的有
A.升高温度 B.加入催化剂
C.不断充入O2 D.充入He(g),使体系总压强增大
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应:2A(g)+B(g)⇌xC (g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L-1·s-1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
(1)x =________
(2)从反应开始到40s达平衡状态,A的平均反应速率为_________
(3)平衡时容器中B的体积分数为_______
(4)该温度下此反应的平衡常数表达式为________ 数值是_____
(5)下列各项能表示该反应达到平衡状态是_________
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量 n(A)∶n(B) =2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体密度不再变化
(6)在相同温度下,若起始时c(A)=5mol·L-1,c(B)=6mol·L-1,反应进行一段时间后,测得A的浓度为3mol·L-1,则此时该反应是否达到平衡状态_____ (填“是”与“否”),此时v(正)___ v(逆)(填“大于”“小于”或“等于”)。
(1)x =
(2)从反应开始到40s达平衡状态,A的平均反应速率为
(3)平衡时容器中B的体积分数为
(4)该温度下此反应的平衡常数表达式为
(5)下列各项能表示该反应达到平衡状态是
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量 n(A)∶n(B) =2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体密度不再变化
(6)在相同温度下,若起始时c(A)=5mol·L-1,c(B)=6mol·L-1,反应进行一段时间后,测得A的浓度为3mol·L-1,则此时该反应是否达到平衡状态
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】以钛铁矿(主要成分为 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如图:
)的工艺流程如图:

已知:“溶浸”后的溶液中含金属元素的离子主要包括 、
、 、
、 、
、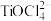 ;富铁元素主要以
;富铁元素主要以 形式存在;富钛渣中钛元素主要以
形式存在;富钛渣中钛元素主要以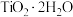 形式存在。
形式存在。
回答下列问题:
(1)“溶浸”时为加快浸取速率,可以采取的措施是___________ (答1条即可);“溶浸”过程 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)若在实验室模拟分离富钛渣和富铁液,则检验富钛渣洗涤干净的操作为___________ 。
(3)“沉铁”过程中需控制 ,其目的是
,其目的是___________ (答1条即可)。
(4)“溶钛”过程中Ti元素的浸出率与反应温度的关系如图所示,试分析40℃后Ti元素浸出率呈图像所示变化的原因:___________ 。

(5) 的晶胞结构如图1所示,设该晶胞的边长为a nm,
的晶胞结构如图1所示,设该晶胞的边长为a nm, 为阿伏伽德罗常数的值。Ti的价电子排布式为
为阿伏伽德罗常数的值。Ti的价电子排布式为___________ ,该晶体的密度
___________ (填含a的计算式)g⋅cm-3; 的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置:
的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置: 。
。________

 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如图:
)的工艺流程如图:
已知:“溶浸”后的溶液中含金属元素的离子主要包括
 、
、 、
、 、
、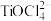 ;富铁元素主要以
;富铁元素主要以 形式存在;富钛渣中钛元素主要以
形式存在;富钛渣中钛元素主要以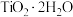 形式存在。
形式存在。回答下列问题:
(1)“溶浸”时为加快浸取速率,可以采取的措施是
 发生反应的离子方程式为
发生反应的离子方程式为(2)若在实验室模拟分离富钛渣和富铁液,则检验富钛渣洗涤干净的操作为
(3)“沉铁”过程中需控制
 ,其目的是
,其目的是(4)“溶钛”过程中Ti元素的浸出率与反应温度的关系如图所示,试分析40℃后Ti元素浸出率呈图像所示变化的原因:

(5)
 的晶胞结构如图1所示,设该晶胞的边长为a nm,
的晶胞结构如图1所示,设该晶胞的边长为a nm, 为阿伏伽德罗常数的值。Ti的价电子排布式为
为阿伏伽德罗常数的值。Ti的价电子排布式为
 的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置:
的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置: 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】铁是人类较早使用的金属之一。运用铁的有关知识,回答下列各题。
(1)据有关报道。目前已能冶炼出纯度高达99.999%的铁,下列关于纯铁的叙述中,正确的是____________ 。
A.耐腐蚀性强,不易生锈 B.不能与盐酸反应
C.与不锈钢成分相同 D.在地壳中含量仅次于铝
(2)向沸水中逐滴滴加1mol·L-1FeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒直径的范围是______________ ,写出反应的离子方程式:___________________ 。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式:________________________________ 。
检验反应后的溶液中存在Fe3+的试剂是__________________________________ 。
(4)欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液。下列试剂中,需要用到的一组是______ (填字母)。
①蒸馏水 ②铁粉 ③浓硝酸 ④浓盐酸 ④烧碱 ⑤浓氨水 ⑥氯水
A.①②④⑥ B.①③④⑥ C.②④⑤ D.①④⑥
(1)据有关报道。目前已能冶炼出纯度高达99.999%的铁,下列关于纯铁的叙述中,正确的是
A.耐腐蚀性强,不易生锈 B.不能与盐酸反应
C.与不锈钢成分相同 D.在地壳中含量仅次于铝
(2)向沸水中逐滴滴加1mol·L-1FeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒直径的范围是
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式:
检验反应后的溶液中存在Fe3+的试剂是
(4)欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液。下列试剂中,需要用到的一组是
①蒸馏水 ②铁粉 ③浓硝酸 ④浓盐酸 ④烧碱 ⑤浓氨水 ⑥氯水
A.①②④⑥ B.①③④⑥ C.②④⑤ D.①④⑥
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。___________ 。
a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2 2NaCl
2NaCl
b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为___________ 。
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为___________ 。
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)___________ 。
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和___________ 。
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO =CaCO3↓和
=CaCO3↓和___________ 。
③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和___________ 。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。

a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2
 2NaCl
2NaCl b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO
 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO
 =CaCO3↓和
=CaCO3↓和③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和
您最近一年使用:0次



