氰化钠广泛用于电镀、金的提取及有机合成中,含氰废水属于高毒类,必须对其进行处理。
(1)向NaCN溶液中通入CO2能发生反应:NaCN+H2O+CO2=HCN+NaHCO3。说明酸性:HCN___ (填“>”或“<”)H2CO3。
(2)含CN-浓度较低的废水可直接用FeSO4 ▪7H2O处理,得到一种蓝色沉淀M,M的摩尔质量为324 g • mol-1,则M的化学式为_______ 。
(3)pH在7.5〜10之间用铜作催化剂的条件下,用SO2-空气处理含氰废水会生成NH3、碳酸氢盐及硫酸盐,已知参与反应的SO2与O2的物质的量之比为1:1,则该反应的离子方程式为___________ 。
(4)工业上常用碱性氯化法处理含氰废水,其原理如下:
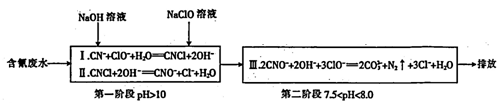
①第一阶段的中间体CNC1中碳元素的化合价为________ 。
②某工厂含氰废水中NaCN的含量为147 mg • L-1,处理10m3这样的废水,理论上需要5 mol • L-1的NaClO 溶液_______ L。
(1)向NaCN溶液中通入CO2能发生反应:NaCN+H2O+CO2=HCN+NaHCO3。说明酸性:HCN
(2)含CN-浓度较低的废水可直接用FeSO4 ▪7H2O处理,得到一种蓝色沉淀M,M的摩尔质量为324 g • mol-1,则M的化学式为
(3)pH在7.5〜10之间用铜作催化剂的条件下,用SO2-空气处理含氰废水会生成NH3、碳酸氢盐及硫酸盐,已知参与反应的SO2与O2的物质的量之比为1:1,则该反应的离子方程式为
(4)工业上常用碱性氯化法处理含氰废水,其原理如下:

①第一阶段的中间体CNC1中碳元素的化合价为
②某工厂含氰废水中NaCN的含量为147 mg • L-1,处理10m3这样的废水,理论上需要5 mol • L-1的NaClO 溶液
更新时间:2017-09-15 18:19:46
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液(有效成分NaClO);② (在水中一部分可以电离出阴、阳离子);③漂白粉;④
(在水中一部分可以电离出阴、阳离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦75%酒精;⑧过氧乙酸(
;⑥碘酒;⑦75%酒精;⑧过氧乙酸(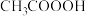 );⑨高铁酸钠(
);⑨高铁酸钠( )。回答下列问题:
)。回答下列问题:
(1)上述杀菌消毒剂属于电解质的是_______ (填序号),属于非电解质的是_______ (填序号),“84”消毒液中有效成分的电离方程式为_______ 。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能原因是NaClO与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO_______  (填“>”或“<”)。
(填“>”或“<”)。
②若混合使用“洁厕灵”(盐酸是成分之一)与“84”消毒液会产生氯气。原因是_______ (用离子方程式表示)。
③漂白粉长时间露置在空气中会变质失效的原因是_______ (用两个化学方程式表示)。
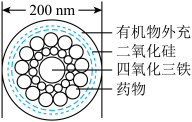
(3)如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。“纳米药物分子车”分散于水中所得的分散系属于_______ (填“溶液”“胶体”或“浊液”)。
(4)高铁酸钠 是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体:
是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体: 。当反应转移电子的数目是
。当反应转移电子的数目是 时,生成标准状况下
时,生成标准状况下 的体积约为
的体积约为_______ 。用 代替
代替 处理饮用水的优点是
处理饮用水的优点是_______ (只答一条即可)。
 (在水中一部分可以电离出阴、阳离子);③漂白粉;④
(在水中一部分可以电离出阴、阳离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦75%酒精;⑧过氧乙酸(
;⑥碘酒;⑦75%酒精;⑧过氧乙酸(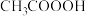 );⑨高铁酸钠(
);⑨高铁酸钠( )。回答下列问题:
)。回答下列问题:(1)上述杀菌消毒剂属于电解质的是
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能原因是NaClO与
 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO (填“>”或“<”)。
(填“>”或“<”)。②若混合使用“洁厕灵”(盐酸是成分之一)与“84”消毒液会产生氯气。原因是
③漂白粉长时间露置在空气中会变质失效的原因是
(3)如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。“纳米药物分子车”分散于水中所得的分散系属于

(4)高铁酸钠
 是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体:
是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体: 。当反应转移电子的数目是
。当反应转移电子的数目是 时,生成标准状况下
时,生成标准状况下 的体积约为
的体积约为 代替
代替 处理饮用水的优点是
处理饮用水的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I. 为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3)。碘酸钾和碘化钾在溶液中能发生下列反应: KIO3+5KI+3H2SO4 = 3I2+3K2SO4+3H2O
(1)该反应中,氧化剂是________ ,氧化产物是________ 。
(3)当有1.5 mol I2生成时,有________ mol还原剂被氧化。
(4)当有4 mol氧化剂参与反应时,转移电子数为________ 个。
II. 周杰伦在歌曲《青花瓷》中唱到“帘外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的化学成分是Cu2(OH)2CO3(碱式碳酸铜),铜在潮湿的空气中生锈的化学反应为:2Cu+O2+CO2+H2O = Cu2(OH)2CO3。
(1)该反应中的还原剂是_________ ,
(2)清除铜锈可以选择的试剂是_____________ 。
(1)该反应中,氧化剂是
(3)当有1.5 mol I2生成时,有
(4)当有4 mol氧化剂参与反应时,转移电子数为
II. 周杰伦在歌曲《青花瓷》中唱到“帘外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的化学成分是Cu2(OH)2CO3(碱式碳酸铜),铜在潮湿的空气中生锈的化学反应为:2Cu+O2+CO2+H2O = Cu2(OH)2CO3。
(1)该反应中的还原剂是
(2)清除铜锈可以选择的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】水中氰化物含量达0.lmg/L,就会使鱼类等生物死亡。因此对工业废水中氰化物含量控制很严,要求低于0.05mg/L。含氰废水可以在碱性条件下氧化处理,使CN-转变为CO2和N2。反应如下:
①CN-+ClO-=CNO-+Cl-
②2CNO-+4OH-+3C12=2CO2+N2+6Cl-+2H2O(CN-、CNO-中N的化合价为-3价)
(1)第二步反应中,___________ 元素被氧化,___________ 作氧化剂
(2)实际操作是向废水中加石灰乳并通入氯气。试填空:
①加入石灰乳的目的是___________
②通入过量氯气的目的是___________ (选填)
A.产生ClO- B.作氧化剂 C.漂白 D.杀菌
③加的是石灰乳而不是烧碱,主要是考虑到___________ 。
①CN-+ClO-=CNO-+Cl-
②2CNO-+4OH-+3C12=2CO2+N2+6Cl-+2H2O(CN-、CNO-中N的化合价为-3价)
(1)第二步反应中,
(2)实际操作是向废水中加石灰乳并通入氯气。试填空:
①加入石灰乳的目的是
②通入过量氯气的目的是
A.产生ClO- B.作氧化剂 C.漂白 D.杀菌
③加的是石灰乳而不是烧碱,主要是考虑到
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】数形结合思想是化学学科的重要思维模式。如图为硫元素的“价—类”二维图,涉及H2S、S、X、Y、Z、M、N七种物质,请结合所学知识和图像使用正确的化学用语来作答:_____ 周期第_____ 族。
(2)从硫元素的化合价角度分析,图中所示物质既有氧化性又有还原性的氧化物是______ (填化学式),写出其与酸性高锰酸钾溶液反应的离子方程式________ 。
(3)常温下,以上不能被Z的浓溶液干燥的气体是______ (填化学式),原因是(写化学方程式)_____ 。
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______ (填代号)。
a.Na2SO3+Na2SO4 b.Na2S+S c.Na2SO3+S d.SO2+Na2SO4
(5)X和H2S发生化学反应,氧化产物和还原产物的物质的量之比为____ 。
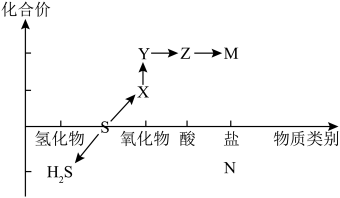
(2)从硫元素的化合价角度分析,图中所示物质既有氧化性又有还原性的氧化物是
(3)常温下,以上不能被Z的浓溶液干燥的气体是
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2SO3+Na2SO4 b.Na2S+S c.Na2SO3+S d.SO2+Na2SO4
(5)X和H2S发生化学反应,氧化产物和还原产物的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有一瓶(约100mL)硫酸和硝酸的混合溶液,取出10.00mL该混合溶液,加入足量氯化钡溶液,充分反应后过滤、洗涤、烘干,可得到4.66g沉淀。滤液跟2.00mol·L-1NaOH溶液反应,共用去35.00mL碱液时恰好中和。求:
(1)混合液中H2SO4和HNO3的物质的量浓度_______ 、________ ;
(2)另取10.00mL原混合酸溶液,加入1.60g铜粉共热,在标准状况下可收集到_______ 毫升气体。
(1)混合液中H2SO4和HNO3的物质的量浓度
(2)另取10.00mL原混合酸溶液,加入1.60g铜粉共热,在标准状况下可收集到
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素铬(Cr)在自然界主要以+3价和+6价存在。
(1)+6价的Cr能引起细胞的突变而对人体不利,可用亚硫酸钠将其还原。离子反应方程式为:3SO32-+Cr2O72-+8H+===2Cr3++3SO42-+4H2O,该反应氧化剂和还原剂的物质的量之比为___________ 。
(2)工业上利用铬铁矿( FeO. Cr2O3)冶炼铬的工艺流程如图所示:
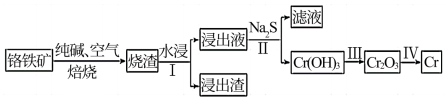
①为加快焙烧速率和提高原料的利用率,可采取的措施之一是___________ 。
②水浸Ⅰ要获得浸出液的操作是___________ 。
③浸出液的主要成分为Na2CrO4,加入Na2S反应后有Na2SO4生成,则操作Ⅱ发生反应的离子方程式为___________ 。
(3)常温下Cr(OH)3的溶度积Ksp=1×10-32,若要使Cr3+完全沉淀pH为___________ [c(Cr3+)降至10-5mol·L-1可认为完全沉淀]。
(4)以铬酸钠(Na2CrO4)为原料,用电化学法可制备重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2CrO42-+2H+=Cr2O72-+H2O)。
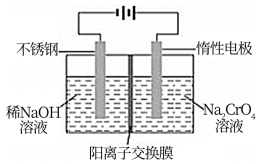
①阳极的电极反应式为___________ 。
②电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则生成重铬酸钠的物质的量为___________ mol。
(1)+6价的Cr能引起细胞的突变而对人体不利,可用亚硫酸钠将其还原。离子反应方程式为:3SO32-+Cr2O72-+8H+===2Cr3++3SO42-+4H2O,该反应氧化剂和还原剂的物质的量之比为
(2)工业上利用铬铁矿( FeO. Cr2O3)冶炼铬的工艺流程如图所示:

①为加快焙烧速率和提高原料的利用率,可采取的措施之一是
②水浸Ⅰ要获得浸出液的操作是
③浸出液的主要成分为Na2CrO4,加入Na2S反应后有Na2SO4生成,则操作Ⅱ发生反应的离子方程式为
(3)常温下Cr(OH)3的溶度积Ksp=1×10-32,若要使Cr3+完全沉淀pH为
(4)以铬酸钠(Na2CrO4)为原料,用电化学法可制备重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2CrO42-+2H+=Cr2O72-+H2O)。

①阳极的电极反应式为
②电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则生成重铬酸钠的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】粗盐中含有CaCl2、MgCl2、Na2SO4以及泥沙等杂质,请回答粗盐提纯的有关问题:
(1)NaCl既属于_______ (填酸、碱或盐),也属于______ (填强电解质或弱电解质),该分类方法称为_______ ,NaCl溶液中共含有________ 种微粒(包含分子和离子)
(2)为了除去可溶性杂质,可以按以下实验步骤进行提纯:①加过量BaCl2溶液;②加过量NaOH溶液;③加过量Na2CO3溶液;④过滤;⑤加适量盐酸.
其中,在步骤②中主要涉及的离子反应方程式是____________________________ ;步骤①和③能否交换顺序_______ (填能或不能)。
(3)将ag粗盐样品溶于水,经过以上一系列提纯操作之后,实验完毕得到bg精盐(不考虑实验过程中操作引起的损耗),下列说法正确的是___________ 。(NA表示阿伏加德罗常数)
(4)某已滤去泥沙的粗盐经检验不含Na2SO4。该粗盐溶于水配成100mL溶液,加入过量稀NaOH溶液后,过滤得到沉淀Mg(OH)25.8g,滤液中通入CO2,得到如下图(横坐标表示通 入CO2标准状况下的体积,纵坐标表示沉淀的物质的量),回答下列问题:
①b段表示的离子方程式为__________
②100mL溶液中Ca2+的物质的量与所加NaOH的物质的量之比为__________
③P点表示的CO2的体积为__________ (标准状况下)。
(1)NaCl既属于
(2)为了除去可溶性杂质,可以按以下实验步骤进行提纯:①加过量BaCl2溶液;②加过量NaOH溶液;③加过量Na2CO3溶液;④过滤;⑤加适量盐酸.
其中,在步骤②中主要涉及的离子反应方程式是
(3)将ag粗盐样品溶于水,经过以上一系列提纯操作之后,实验完毕得到bg精盐(不考虑实验过程中操作引起的损耗),下列说法正确的是
| A.粗盐中Na+数目为aNA/58.5 | B.精盐中NaCl物质的量为b/58.5mol |
| C.粗盐中NaCl的质量分数为b/a×100% | D.粗盐中关于NaCl的量无法确定 |
(4)某已滤去泥沙的粗盐经检验不含Na2SO4。该粗盐溶于水配成100mL溶液,加入过量稀NaOH溶液后,过滤得到沉淀Mg(OH)25.8g,滤液中通入CO2,得到如下图(横坐标表示通 入CO2标准状况下的体积,纵坐标表示沉淀的物质的量),回答下列问题:

①b段表示的离子方程式为
②100mL溶液中Ca2+的物质的量与所加NaOH的物质的量之比为
③P点表示的CO2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】地球的表面积为5.1亿平方公里,其中海洋的面积为3.67亿平方公里,占整个地球表面积的70.8 %。海洋是一个巨大的化学资源宝库,下面根据海水资源综合利用,请回答下列问题:
(1)淡化海水的方法有________________ (写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、________ (填化学式),之后________ (填操作名称),再加入适量________ (填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
(2)由无水MgCl2制取金属镁的常用工业方法是__________________ 。
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是__________ 。
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2,写出反应的离子方程式____________ 。再H2SO4处理所得溶液重新得到Br2,其反应的离子方程式为_______________ 。
(1)淡化海水的方法有
(2)由无水MgCl2制取金属镁的常用工业方法是
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2,写出反应的离子方程式
您最近一年使用:0次

 ,另含有Fe2+、Cu2+等杂质。先加入
,另含有Fe2+、Cu2+等杂质。先加入

