氯气、漂白液、漂白粉可用于杀菌消毒。
(1)氯气泄漏事故发生时会严重污染环境,下列处理方法不正确的是____ (填序号)。
①将人和畜迅速转移至较高的地方 ②将人和畜迅速转移至较低的地方
③在事故现场喷洒氢氧化钠溶液④用浸透氢氧化钠的毛巾捂住嘴和鼻
⑤用浸透肥皂水(呈弱碱性)的毛巾捂住嘴和鼻
(2)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为___________ 。
(3)将漂白粉溶于适量水中,呈白色浊状物,静置沉降。取少许上层清液,滴加碳酸钠溶液出现白色沉淀,发生反应的化学方程式为__________ 。
(4)瓶装漂白粉久置空气中会呈稀粥状而失去漂白作用。试用化学方程式表示漂白粉在空气中易失效的原因是①______________ ;②______________ 。
(1)氯气泄漏事故发生时会严重污染环境,下列处理方法不正确的是
①将人和畜迅速转移至较高的地方 ②将人和畜迅速转移至较低的地方
③在事故现场喷洒氢氧化钠溶液④用浸透氢氧化钠的毛巾捂住嘴和鼻
⑤用浸透肥皂水(呈弱碱性)的毛巾捂住嘴和鼻
(2)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为
(3)将漂白粉溶于适量水中,呈白色浊状物,静置沉降。取少许上层清液,滴加碳酸钠溶液出现白色沉淀,发生反应的化学方程式为
(4)瓶装漂白粉久置空气中会呈稀粥状而失去漂白作用。试用化学方程式表示漂白粉在空气中易失效的原因是①
更新时间:2017-10-15 06:05:54
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氯气是一种化学性质活泼的气体。
(1)氯气是一种具有_______ 气味的气体,密度比空气的_______ (填“大”或“小”),若采用如图装置收集氯气,则氯气应由_______ 管(填“A”或“B”)通入。
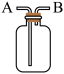
(2)氯气与NaOH溶液反应的化学方程式为_______ ,该反应可用于工业上制取漂白液,其有效成分是_______ 。
(1)氯气是一种具有

(2)氯气与NaOH溶液反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】收集氯气的方法___________ 或____________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯气是一种重要的化工原料,从氯气的发现到氯元素的确认,经历了数位科学家30多年的不懈探索,根据相关信息,回答下列问题:
(1)化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合并加热,很快产生有强烈刺激性气味的_________ 色气体,完成该反应的化学方程式:_______________ 。
(2)除去氯气中的HCl,可以使用的试剂是_______ ,最合理的氯气发生装置是_______ (填字母)。

(3)化学家贝托莱将Cl2的水溶液露置在阳光下,生成一种无色无味气体,该气体为____ ,写出该反应的化学方程式:__________ 。
(4)化学家泰耐特将Cl2通入石灰乳中得到漂白粉,该混合物具有漂白作用的物质是______ (填化学式)
(1)化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合并加热,很快产生有强烈刺激性气味的
(2)除去氯气中的HCl,可以使用的试剂是

(3)化学家贝托莱将Cl2的水溶液露置在阳光下,生成一种无色无味气体,该气体为
(4)化学家泰耐特将Cl2通入石灰乳中得到漂白粉,该混合物具有漂白作用的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】饮用水质量是关系人类的重要问题,硫酸铝、活性炭等均为常用的净水剂。回答下列问题:
(1) 中铁元素的化合价是
中铁元素的化合价是___________ 。
(2)以下物质均为常用的净水剂,其中属于盐的是___________ 。
A.氯气 B.次氯酸钙 C.活性炭 D.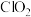 E.
E.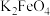
(3)自来水厂净水过程如图所示。
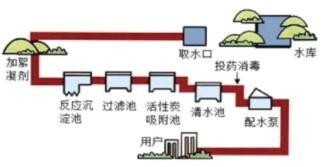
①硫酸铝可用作絮凝剂,其溶于水的电离方程式为___________ 。
②活性炭因其具有___________ 性,用于去除水中的色素和臭味。另有研究表明,活性炭可用于去除水中多余的氯气,反应生成了氯化氢和二氧化碳,写出该反应的化学方程式,并用单线桥法标明电子转移的方向和数目______ ,该反应中体现了活性炭的___________ 性。
③氯气是最早用于饮用水消毒的物质,其在水中发生反应的离子方程式为___________ 。
④二氧化氯是一种广谱杀菌剂,在起消毒作用后以 存在于溶液中。若以
存在于溶液中。若以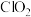 替代
替代 ,提供相同数目的电子,消耗二氧化氯和氯气的物质的量之比为
,提供相同数目的电子,消耗二氧化氯和氯气的物质的量之比为___________ 。
(1)
 中铁元素的化合价是
中铁元素的化合价是(2)以下物质均为常用的净水剂,其中属于盐的是
A.氯气 B.次氯酸钙 C.活性炭 D.
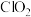 E.
E.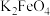
(3)自来水厂净水过程如图所示。

①硫酸铝可用作絮凝剂,其溶于水的电离方程式为
②活性炭因其具有
③氯气是最早用于饮用水消毒的物质,其在水中发生反应的离子方程式为
④二氧化氯是一种广谱杀菌剂,在起消毒作用后以
 存在于溶液中。若以
存在于溶液中。若以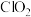 替代
替代 ,提供相同数目的电子,消耗二氧化氯和氯气的物质的量之比为
,提供相同数目的电子,消耗二氧化氯和氯气的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式_________________________ 。
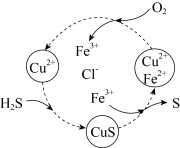
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可以回收S,其物质转化如图所示。该图示的总反应为_________________________ 。
(3)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,请完成方程式的配平。
___ Al+___ NO3-+___ =___ AlO2-+___ N2↑+___ H2O
(1)NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可以回收S,其物质转化如图所示。该图示的总反应为

(3)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,请完成方程式的配平。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与FeCl3溶液 ⑤Cl2与NaOH溶液 ⑥Fe与HNO3溶液 ⑦Fe与H2SO4溶液 ⑧Na与O2
(1)由于浓度不同而发生不同氧化还原反应的是_______ (填序号,下同)。
(2)由于温度不同而发生不同氧化还原反应的是_______ 。
(3)氧化还原反应不受浓度、温度影响的是_______ 。
(1)由于浓度不同而发生不同氧化还原反应的是
(2)由于温度不同而发生不同氧化还原反应的是
(3)氧化还原反应不受浓度、温度影响的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题
(1)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用某溶液吸收多余的氯气,原理是(用化学方程式表示)___________ ;
(2)长期露置于空气中的漂白粉,加稀盐酸后产生的气体是___________(用字母代号填)
(3)石英砂不能与碱性物质共同存放,以NaOH为例,用化学方程式表示其原因:___________ 。
(1)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用某溶液吸收多余的氯气,原理是(用化学方程式表示)
(2)长期露置于空气中的漂白粉,加稀盐酸后产生的气体是___________(用字母代号填)
| A.O2 | B.Cl2 | C.CO2 | D.HClO |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】用Cl2和石灰乳可以制备漂粉精,漂粉精可于游泳池的消毒。
(1)写出制备漂粉精的化学方程式______________ 。
(2)漂粉精真正起消毒作用的物质是HClO。漂粉精在水中释放HClO的途径如下:
途径1:Ca(ClO)2+2H2O⇌Ca(OH)2+2HClO
途径2:Ca(ClO)2+H2O+CO2=________ +_______ (把反应补充完整)
(3)游泳池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会________ (填“增强”或“减弱”)。
②池水酸性过强,会刺激眼睛和皮肤。通常加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是________ (填离子符号)。
(1)写出制备漂粉精的化学方程式
(2)漂粉精真正起消毒作用的物质是HClO。漂粉精在水中释放HClO的途径如下:
途径1:Ca(ClO)2+2H2O⇌Ca(OH)2+2HClO
途径2:Ca(ClO)2+H2O+CO2=
(3)游泳池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会
②池水酸性过强,会刺激眼睛和皮肤。通常加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有下列十种物质(微粒):①氢氧化铁胶体 ②氯水 ③四氯化碳 ④CO2 ⑤CuSO4•5H2O ⑥漂白粉 ⑦0.2 mol·L-1 Ba(OH)2溶液 ⑧0.1 mol·L-1 Na2SO4溶液 ⑨溴水 ⑩KI。
(1)属于电解质的有________ 。
(2)将⑦⑧两溶液等体积混合,所得溶液中Na+的物质的量浓度约________ 。
(3)往往用________ 来证明①为胶体。
(4)实验室欲配制480 mL的⑧,下列说法正确的是________ 。
a.应选用480 mL容量瓶
b.需称量6.8 g Na2SO4固体
c.实验前,容量瓶需洗净并干燥
d.在其他操作正确情况下,定容时,俯视刻度线会导致所配溶液浓度偏大
(5)⑥在使用时需加水浸泡片刻,才能发挥更好的漂白效果,请用离子方程式表示相应的反应原理________ 。
(1)属于电解质的有
(2)将⑦⑧两溶液等体积混合,所得溶液中Na+的物质的量浓度约
(3)往往用
(4)实验室欲配制480 mL的⑧,下列说法正确的是
a.应选用480 mL容量瓶
b.需称量6.8 g Na2SO4固体
c.实验前,容量瓶需洗净并干燥
d.在其他操作正确情况下,定容时,俯视刻度线会导致所配溶液浓度偏大
(5)⑥在使用时需加水浸泡片刻,才能发挥更好的漂白效果,请用离子方程式表示相应的反应原理
您最近一年使用:0次



