完成下列问题
(1)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用某溶液吸收多余的氯气,原理是(用化学方程式表示)___________ ;
(2)长期露置于空气中的漂白粉,加稀盐酸后产生的气体是___________(用字母代号填)
(3)石英砂不能与碱性物质共同存放,以NaOH为例,用化学方程式表示其原因:___________ 。
(1)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用某溶液吸收多余的氯气,原理是(用化学方程式表示)
(2)长期露置于空气中的漂白粉,加稀盐酸后产生的气体是___________(用字母代号填)
| A.O2 | B.Cl2 | C.CO2 | D.HClO |
更新时间:2022-04-05 09:22:22
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下表是生活生产中常见的物质:
(1)分别写出③、⑥的电离方程式__________ ;__________ 。
(2)③与⑥反应的离子方程式:__________ 。
(3)检验⑤的溶液中含有 的方法是:
的方法是:__________ ,有关的离子方程式为__________ 。
(4)常温下,将 通入②中,可以得到一种漂白液,该漂白液的有效成分为
通入②中,可以得到一种漂白液,该漂白液的有效成分为__________ (填名称),检验中②阳离子的方法是__________ (填名称)。
编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
名称 | Na |
|
| 酒精 |
|
|
(2)③与⑥反应的离子方程式:
(3)检验⑤的溶液中含有
 的方法是:
的方法是:(4)常温下,将
 通入②中,可以得到一种漂白液,该漂白液的有效成分为
通入②中,可以得到一种漂白液,该漂白液的有效成分为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】离子反应是中学化学中重要的反应类型。回答下列问题:
(1)离子方程式是重要的化学用语。下列是有关离子方程式的一个错误观点:酸碱中和反应均可表示为 ,请用一个相应的“离子方程式”否定这个观点。
,请用一个相应的“离子方程式”否定这个观点。___________
(2)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“ ”来表示,请写出2个有关反应的化学方程式:
”来表示,请写出2个有关反应的化学方程式:
①___________ ;
②___________ 。
(3)实验室用铁、氧化铜、稀硫酸为原料制取铜,某同学设计了两个实验方案:
方案一: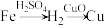
方案二:
写出上述两个方案每步转化的有关方程式。
方案一,化学方程式:___________ ;___________
方案二,离子方程式:___________ ;___________
(4)在常温下,将 通入
通入 溶液中,可以得到一种漂白液。上述反应的离子方程式为
溶液中,可以得到一种漂白液。上述反应的离子方程式为___________ ,该漂白液的有效成分是___________ (填名称)。
(5)检验某溶液中是否含有 的方法是:
的方法是:___________ ,有关离子方程式是___________ 。
(1)离子方程式是重要的化学用语。下列是有关离子方程式的一个错误观点:酸碱中和反应均可表示为
 ,请用一个相应的“离子方程式”否定这个观点。
,请用一个相应的“离子方程式”否定这个观点。(2)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“
 ”来表示,请写出2个有关反应的化学方程式:
”来表示,请写出2个有关反应的化学方程式:①
②
(3)实验室用铁、氧化铜、稀硫酸为原料制取铜,某同学设计了两个实验方案:
方案一:
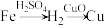
方案二:

写出上述两个方案每步转化的有关方程式。
方案一,化学方程式:
方案二,离子方程式:
(4)在常温下,将
 通入
通入 溶液中,可以得到一种漂白液。上述反应的离子方程式为
溶液中,可以得到一种漂白液。上述反应的离子方程式为(5)检验某溶液中是否含有
 的方法是:
的方法是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下(氯化过程中少量Ca(ClO)2分解为CaCl2和O2):
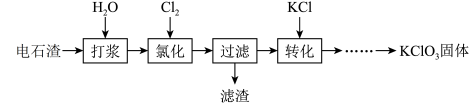
(1)氯化过程控制电石渣过量、在75 ℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2。
①生成Ca(ClO)2的化学方程式为__________________________________________________ 。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有________ (填序号)。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。请回答:
①滤渣的主要成分为__________ (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] :n[CaCl2]________ 1∶5(填“>”、“<”或“=”)。

(1)氯化过程控制电石渣过量、在75 ℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2。
①生成Ca(ClO)2的化学方程式为
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。请回答:
①滤渣的主要成分为
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] :n[CaCl2]
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】中国疾控中心指出,消毒是疫情防控的重要措施。含氯消毒剂是高效、安全的杀菌消毒剂。
(1)漂白粉主要用于游泳池水等的杀菌和消毒,久置空气中会呈稀粥状而失去漂白作用,用化学方程式表示漂白粉在空气中失效的原因___________ 。84消毒液是一种家用消毒剂,原因是 具有
具有___________ 性。
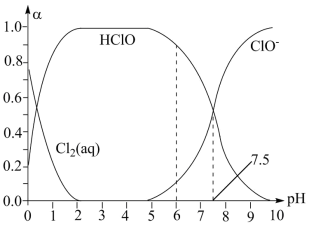
(2)新制氯水常用于杀菌消毒,在 时将氯气溶于水形成氯气-氯水体系,该体系中
时将氯气溶于水形成氯气-氯水体系,该体系中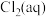 、
、 和
和 的物质的量分数(
的物质的量分数( )随
)随 变化的关系如图所示。由图分析,用氯气处理饮用水时,
变化的关系如图所示。由图分析,用氯气处理饮用水时, 与
与 两种情况下,
两种情况下,
___________ 时杀菌效果强。当 时,氯水中含氯元素的微粒有
时,氯水中含氯元素的微粒有 、
、 和
和___________ 。
(3) 是国际上公认的安全、无毒、无“三致”效应(致癌、致畸、致突变)的杀菌消毒剂。
是国际上公认的安全、无毒、无“三致”效应(致癌、致畸、致突变)的杀菌消毒剂。
①根据世界环保联盟的要求, 将逐渐取代
将逐渐取代 成为自来水的消毒剂。工业上常用
成为自来水的消毒剂。工业上常用 溶液和
溶液和 溶液混合并加入
溶液混合并加入 酸化制得
酸化制得 ,且产物中有
,且产物中有 ,则在该反应中,氧化产物和还原产物的物质的量之比为
,则在该反应中,氧化产物和还原产物的物质的量之比为___________ 。
②已知 在进行饮用水消毒时转化为
在进行饮用水消毒时转化为 ,则
,则 与
与 的消毒能力之比为
的消毒能力之比为___________ 。(写最简整数比;消毒能力用单位质量消毒剂得电子多少来衡量)
(1)漂白粉主要用于游泳池水等的杀菌和消毒,久置空气中会呈稀粥状而失去漂白作用,用化学方程式表示漂白粉在空气中失效的原因
 具有
具有(2)新制氯水常用于杀菌消毒,在
 时将氯气溶于水形成氯气-氯水体系,该体系中
时将氯气溶于水形成氯气-氯水体系,该体系中 、
、 和
和 的物质的量分数(
的物质的量分数( )随
)随 变化的关系如图所示。由图分析,用氯气处理饮用水时,
变化的关系如图所示。由图分析,用氯气处理饮用水时, 与
与 两种情况下,
两种情况下,
 时,氯水中含氯元素的微粒有
时,氯水中含氯元素的微粒有 、
、 和
和
(3)
 是国际上公认的安全、无毒、无“三致”效应(致癌、致畸、致突变)的杀菌消毒剂。
是国际上公认的安全、无毒、无“三致”效应(致癌、致畸、致突变)的杀菌消毒剂。①根据世界环保联盟的要求,
 将逐渐取代
将逐渐取代 成为自来水的消毒剂。工业上常用
成为自来水的消毒剂。工业上常用 溶液和
溶液和 溶液混合并加入
溶液混合并加入 酸化制得
酸化制得 ,且产物中有
,且产物中有 ,则在该反应中,氧化产物和还原产物的物质的量之比为
,则在该反应中,氧化产物和还原产物的物质的量之比为②已知
 在进行饮用水消毒时转化为
在进行饮用水消毒时转化为 ,则
,则 与
与 的消毒能力之比为
的消毒能力之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学与社会发展以及人们生活质量的提高有着密切的关系。回答下列问题:
(1)Na2O2常用于解决潜艇的供氧问题。CaO2与Na2O2性质相似,常用于解决鱼塘缺氧问题,其反应原理用化学方程式表示为___________ ,不用Na2O2解决该问题的原因是___________ (从与水反应生成物的性质考虑)。
(2)NaHCO3的俗名为___________ ,其水溶液呈碱性,常用于处理食品生产中面粉过度发酵产生的有机酸(有机酸的化学式用HA表示),又能使面食疏松多孔,有关反应的化学方程式为___________ 。
(3)2020年新冠肺炎病毒全球肆虐,NaClO、K2FeO4均是效果较好的消毒剂,NaClO久置于空气中失效的原因是①___________ (用化学方程式表示);
②2HClO 2HCl+O2↑。
2HCl+O2↑。
(4)咸阳市区地铁一号线3期工程正在紧张建设中,在施工中要使用各种材料。
①建设中需要大量的水泥,生产水泥的主要原料有石灰石和___________ (填字母)。
a.黏土b.纯碱c.石英
②目前国内地铁车辆主要采用的是不锈钢车体。下列有关不锈钢的叙述正确的是___________ 填字母)。
a.属于合金b.在空气中耐腐蚀c.韧性和耐磨性差
(1)Na2O2常用于解决潜艇的供氧问题。CaO2与Na2O2性质相似,常用于解决鱼塘缺氧问题,其反应原理用化学方程式表示为
(2)NaHCO3的俗名为
(3)2020年新冠肺炎病毒全球肆虐,NaClO、K2FeO4均是效果较好的消毒剂,NaClO久置于空气中失效的原因是①
②2HClO
 2HCl+O2↑。
2HCl+O2↑。(4)咸阳市区地铁一号线3期工程正在紧张建设中,在施工中要使用各种材料。
①建设中需要大量的水泥,生产水泥的主要原料有石灰石和
a.黏土b.纯碱c.石英
②目前国内地铁车辆主要采用的是不锈钢车体。下列有关不锈钢的叙述正确的是
a.属于合金b.在空气中耐腐蚀c.韧性和耐磨性差
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硫的氧化物、氮的氧化物、硅的氧化物都是重要的化工原料。将其合理利用,既能减少污染,又能充分利用资源,创造价值。
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英的成分是_______ (填化学式),该物质的类别属于_______ 氧化物(填“碱性”、 “酸性”或“两性”),实验室中不能用带玻璃塞的试剂瓶盛放NaOH溶液,原因是_______________ (用离子方程式表示)。
(2)玻璃是常用的硅酸盐材料,生产普通玻璃的主要材料有________ 、_______ 、_______ ,工艺师常用_________ (填物质名称)来雕刻玻璃,其作用过程产生________ 气体。
(3)石英坩埚可以用来灼烧下面哪种物质_______。(填字母)
(4)SiO2在自然界中广泛存在,它是制备现代通讯材料_________ (写该材料名称)的主要原料
(5)在一定量的浓硫酸中加入过量铜片,加热使之反应,反应结束后。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为_________________ 。
(6)硝酸是一种重要的工业原料。在实验室中通常保存在棕色试剂瓶中,则原因是_______________ (用化学方程式表示)。硝酸是一种易挥发性的酸,用蘸浓硝酸和蘸浓氨水的玻璃棒靠近会产生大量白烟,白烟的成分是__________ 。
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英的成分是
(2)玻璃是常用的硅酸盐材料,生产普通玻璃的主要材料有
(3)石英坩埚可以用来灼烧下面哪种物质_______。(填字母)
| A.碳酸钠 | B.氢氧化钠 | C.氢氧化钾 | D.氯化钠 |
(5)在一定量的浓硫酸中加入过量铜片,加热使之反应,反应结束后。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
(6)硝酸是一种重要的工业原料。在实验室中通常保存在棕色试剂瓶中,则原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请按要求回答下列问题:
(1)下列纯净物中:a.NaOH b.Ar c.MgCl2 d.HCl e.NH3 f.KNO3
①不含化学键的物质是_______ (填序号,下同)。
②既含有离子键又含有共价键的物质是______ 。
③只含有离子键的物质是________ 。
(2)下列变化中,不需要破坏化学键的是______ 。
A.氯化氢溶于水 B.加热氯酸钾使其分解
C.碘升华 D.氯化钠溶于水
(3)实验室盛放碱液的试剂瓶不能用玻璃塞,以氢氧化钠为例,用离子方程式表示其原因:_________ ,任写一个制造普通玻璃的主要反应的化学方程___________________ 。
(4)硅是良好的半导体材料,写出工业上生产粗硅的化学方程式:__________________________ 。
(1)下列纯净物中:a.NaOH b.Ar c.MgCl2 d.HCl e.NH3 f.KNO3
①不含化学键的物质是
②既含有离子键又含有共价键的物质是
③只含有离子键的物质是
(2)下列变化中,不需要破坏化学键的是
A.氯化氢溶于水 B.加热氯酸钾使其分解
C.碘升华 D.氯化钠溶于水
(3)实验室盛放碱液的试剂瓶不能用玻璃塞,以氢氧化钠为例,用离子方程式表示其原因:
(4)硅是良好的半导体材料,写出工业上生产粗硅的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)在下列反应中,水作氧化剂的是________ 。
A.Cl2+H2O HCl+HClO B.NaH+H2O=NaOH+H2↑
HCl+HClO B.NaH+H2O=NaOH+H2↑
C.3Fe+4H2O(g) Fe3O4 + 4H2 D. H2+CuO
Fe3O4 + 4H2 D. H2+CuO H2O+Cu
H2O+Cu
E. 2NaCl+2H2O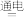 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(2)用双桥表示3Cl2+6KOH=5KCl+KClO3+3H2O电子转移的方和数目:__________________ 。
(3)在一定条件下,利用置换反应X+Y=W+Z,可实现物质之间的转化
①若X为Mg,W为C,则Z为__________________ 。
②若X为SiO2,W为CO,该反应在工业的用途是___________________ 。
(4) 某未知溶液中可能含有Fe2+,确定含该离子的实验方案为:取少量该溶液于试管中,先__________________ ,再__________________ ,则说明溶液中含有Fe2+。
A.Cl2+H2O
 HCl+HClO B.NaH+H2O=NaOH+H2↑
HCl+HClO B.NaH+H2O=NaOH+H2↑C.3Fe+4H2O(g)
 Fe3O4 + 4H2 D. H2+CuO
Fe3O4 + 4H2 D. H2+CuO H2O+Cu
H2O+CuE. 2NaCl+2H2O
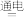 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑(2)用双桥表示3Cl2+6KOH=5KCl+KClO3+3H2O电子转移的方和数目:
(3)在一定条件下,利用置换反应X+Y=W+Z,可实现物质之间的转化
①若X为Mg,W为C,则Z为
②若X为SiO2,W为CO,该反应在工业的用途是
(4) 某未知溶液中可能含有Fe2+,确定含该离子的实验方案为:取少量该溶液于试管中,先
您最近一年使用:0次




 变质生成碳酸钙,请写出化学方程式:
变质生成碳酸钙,请写出化学方程式: 溶液能够使酸性
溶液能够使酸性 溶液褪色,请写出反应的离子方程式
溶液褪色,请写出反应的离子方程式

