下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与FeCl3溶液 ⑤Cl2与NaOH溶液 ⑥Fe与HNO3溶液 ⑦Fe与H2SO4溶液 ⑧Na与O2
(1)由于浓度不同而发生不同氧化还原反应的是_______ (填序号,下同)。
(2)由于温度不同而发生不同氧化还原反应的是_______ 。
(3)氧化还原反应不受浓度、温度影响的是_______ 。
(1)由于浓度不同而发生不同氧化还原反应的是
(2)由于温度不同而发生不同氧化还原反应的是
(3)氧化还原反应不受浓度、温度影响的是
更新时间:2023-03-08 18:29:22
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】“84消毒液”是日常生活中常用的消毒液,在抗击新冠肺炎中广泛应用。
(1)“84消毒液”的有效成分为________ ;
(2)“84消毒液”与适量硫酸混合使用可增强消毒能力,某消毒组成员欲用盐酸代替硫酸,是否可行_________ (填“是"或“否”),原因是_____________ ;
(3)Cl2是最早用于饮用水消毒的物质,ClO2是一种广谱消毒剂,等质量的Cl2和ClO2消毒效率高的是________ (填化学式);工业上ClO2常用NaClO3和Na2SO3溶液混合酸化反应制得,反应中NaClO3和Na2SO3的物质的量之比为__________ 。
(1)“84消毒液”的有效成分为
(2)“84消毒液”与适量硫酸混合使用可增强消毒能力,某消毒组成员欲用盐酸代替硫酸,是否可行
(3)Cl2是最早用于饮用水消毒的物质,ClO2是一种广谱消毒剂,等质量的Cl2和ClO2消毒效率高的是
您最近半年使用:0次
【推荐2】消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1) 、
、 、
、 (还原产物为
(还原产物为 )、
)、 都可以做消毒剂,都具有
都可以做消毒剂,都具有___________ 性。
(2)将紫色石蕊试液滴入氯水中现象是___________ 。
(3)漂白剂亚氯酸钠( )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为 (未配平)。在该反应中,被氧化的元素是
(未配平)。在该反应中,被氧化的元素是___________ ,13.7g 完全反应转移电子数是
完全反应转移电子数是___________ 。
(4)“84”消毒液(主要成分是NaClO),用氯气制取NaClO的离子方程式是___________ ,使用“84”消毒液时加入少量的稀硫酸效果更好,原理是___________ (用离子方程式表示)。
(1)
 、
、 、
、 (还原产物为
(还原产物为 )、
)、 都可以做消毒剂,都具有
都可以做消毒剂,都具有(2)将紫色石蕊试液滴入氯水中现象是
(3)漂白剂亚氯酸钠(
 )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为 (未配平)。在该反应中,被氧化的元素是
(未配平)。在该反应中,被氧化的元素是 完全反应转移电子数是
完全反应转移电子数是(4)“84”消毒液(主要成分是NaClO),用氯气制取NaClO的离子方程式是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】 与
与 的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。
的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。
回答下列问题:
(1)氯气的电子式为_______ 。
(2)氯气和氢氧化钠溶液制备漂白液的离子方程式为_______ 。
(3)某兴趣小组通过如下装置(夹持装置略)对 制备、吸收、释放和应用进行了研究。
制备、吸收、释放和应用进行了研究。
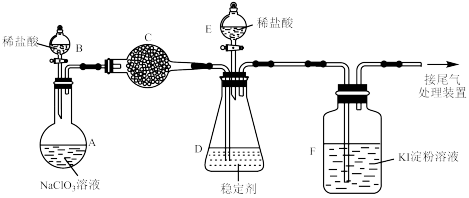
已知:装置C中的药品可以吸收氯气
①打开B的活塞,A中发生反应生成 ,请将化学方程式配平
,请将化学方程式配平_______
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ 。
。
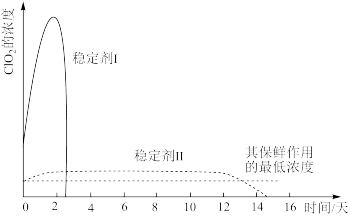
②已吸收 气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放
气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放 的浓度随时间的变化如下图所示。若将其用于水果保鲜,你认为效果较好的稳定剂是
的浓度随时间的变化如下图所示。若将其用于水果保鲜,你认为效果较好的稳定剂是_______ ,原因是_______ 。
③关闭B的活塞, 在D中被稳定剂完全吸收生成
在D中被稳定剂完全吸收生成 ,在酸性条件下
,在酸性条件下 可发生反应生成
可发生反应生成 并释放出
并释放出 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
 与
与 的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。
的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。回答下列问题:
(1)氯气的电子式为
(2)氯气和氢氧化钠溶液制备漂白液的离子方程式为
(3)某兴趣小组通过如下装置(夹持装置略)对
 制备、吸收、释放和应用进行了研究。
制备、吸收、释放和应用进行了研究。
已知:装置C中的药品可以吸收氯气
①打开B的活塞,A中发生反应生成
 ,请将化学方程式配平
,请将化学方程式配平_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ 。
。②已吸收
 气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放
气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放 的浓度随时间的变化如下图所示。若将其用于水果保鲜,你认为效果较好的稳定剂是
的浓度随时间的变化如下图所示。若将其用于水果保鲜,你认为效果较好的稳定剂是
③关闭B的活塞,
 在D中被稳定剂完全吸收生成
在D中被稳定剂完全吸收生成 ,在酸性条件下
,在酸性条件下 可发生反应生成
可发生反应生成 并释放出
并释放出 ,该反应的离子方程式为
,该反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】 为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。
为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。
(1)标准状况下,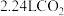 与足量的
与足量的 充分反应,转移的电子总数为
充分反应,转移的电子总数为 ,判断依据:
,判断依据:_______ 。
(2)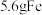 和
和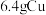 分别与
分别与 充分反应,转移的电子数均为
充分反应,转移的电子数均为 ,判断依据:
,判断依据:_______ 。
(3)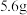 铁粉与硝酸反应失去的电子数一定为
铁粉与硝酸反应失去的电子数一定为 ,判断依据:
,判断依据:_______ 。
(4)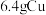 与S完全反应,转移的电子数为
与S完全反应,转移的电子数为 ,判断依据:
,判断依据:_______ 。
(5)向 溶液中通入适量
溶液中通入适量 ,当有
,当有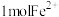 被氧化时,转移的电子总数一定等于
被氧化时,转移的电子总数一定等于 ,判断依据:
,判断依据:_______ 。
 为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。
为阿伏加德罗常数的值。请判断下列说法的正误(正确的打“√”,错误的打“×”),简述判断依据。(1)标准状况下,
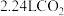 与足量的
与足量的 充分反应,转移的电子总数为
充分反应,转移的电子总数为 ,判断依据:
,判断依据:(2)
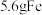 和
和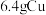 分别与
分别与 充分反应,转移的电子数均为
充分反应,转移的电子数均为 ,判断依据:
,判断依据:(3)
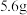 铁粉与硝酸反应失去的电子数一定为
铁粉与硝酸反应失去的电子数一定为 ,判断依据:
,判断依据:(4)
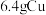 与S完全反应,转移的电子数为
与S完全反应,转移的电子数为 ,判断依据:
,判断依据:(5)向
 溶液中通入适量
溶液中通入适量 ,当有
,当有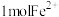 被氧化时,转移的电子总数一定等于
被氧化时,转移的电子总数一定等于 ,判断依据:
,判断依据:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列说法是否正确(正确的打“√”,不正确的打“×”),若不正确请说明理由。
(1)SiO2能与氢氧化钠溶液和氢氟酸反应,所以SiO2是两性氧化物___________ ,理由 ___________
(2)某气体通入品红溶液后,品红溶液褪色,则该气体一定是SO2___________ ,理由 ___________
(3)碳、铜与浓硝酸反应时,浓硝酸只表现强氧化性___________ ,理由 ___________
(4)王水是浓盐酸和浓硝酸体积比为3∶1的混合物,能溶解金和铂___________ ,理由______
(1)SiO2能与氢氧化钠溶液和氢氟酸反应,所以SiO2是两性氧化物
(2)某气体通入品红溶液后,品红溶液褪色,则该气体一定是SO2
(3)碳、铜与浓硝酸反应时,浓硝酸只表现强氧化性
(4)王水是浓盐酸和浓硝酸体积比为3∶1的混合物,能溶解金和铂
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮、磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式:______ 。
H2PO2-+Ag+=PO43-+Ag+。
由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下:

(2)关于除砷条件的说法合理的是_______ (填字母)。
a. 75℃使白磷熔化,并溶于水b.硝酸浓度不易过大,防止白磷反应
c.温度不宜过高,防止硝酸分解d.适当提高温度,加快化学反应速率
(3)硝酸氧化除砷时被还原为NO,氧化相同质量的砷,当转化为亚砷酸的量越多,消耗硝酸的量越____ (填“多”或“少”)。
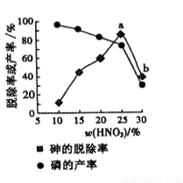
(4)某条件下,用一定量的硝酸处理一定量的工业白磷,砷的脱除率及磷的产率随硝酸质量分数的变化如图,砷的脱除率从a点到b点降低的原因是__________________ 。
(1)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式:
H2PO2-+Ag+=PO43-+Ag+。
由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下:

(2)关于除砷条件的说法合理的是
a. 75℃使白磷熔化,并溶于水b.硝酸浓度不易过大,防止白磷反应
c.温度不宜过高,防止硝酸分解d.适当提高温度,加快化学反应速率
(3)硝酸氧化除砷时被还原为NO,氧化相同质量的砷,当转化为亚砷酸的量越多,消耗硝酸的量越
(4)某条件下,用一定量的硝酸处理一定量的工业白磷,砷的脱除率及磷的产率随硝酸质量分数的变化如图,砷的脱除率从a点到b点降低的原因是

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】金属及其化合物在生活生产中具有广泛的应用价值。
(1)Fe2+在酸性介质中较稳定,则硫酸亚铁溶液的保存方法为_______ 。
(2)过二硫酸钾(K2S2O8)具有强氧化性可将 I−氧化为 I2:S2O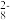 +2I-=2SO
+2I-=2SO +I2。通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示 Fe3+对上述反应催化的过程:① Fe3++2I-= I2+ Fe2+ ②
+I2。通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示 Fe3+对上述反应催化的过程:① Fe3++2I-= I2+ Fe2+ ②_______ 。
(3)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,得到炉渣(含 Fe2O3、FeO、SiO2、Al2O3) 。
该工艺的中间过程会发生反应:2Cu2O+ Cu2S 6Cu+SO2↑;反应的还原剂是
6Cu+SO2↑;反应的还原剂是_____ ;选用提供的试剂设计实验验证炉渣中含有 FeO。提供的试剂:稀盐酸、稀硫酸、KSCN 溶液、KMnO4 溶液、NaOH 溶液、碘水。所选试剂为 _____ 。证明炉渣中含有 FeO 的实验现象为 _____ 。下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是 _____ (填字母)。
(4)将 MgSO4xH2O 加热,失去 5 个 H2O,失重 36.6%,则 x=_______ (取整数)。化合物 Mg5Al3(OH)19(H2O)4 可作环保型阻燃材料,受热分解的化学方程式为:2Mg5Al3(OH)19(H2O)4 27H2O↑+10MgO+3A12O3
27H2O↑+10MgO+3A12O3
该化合物作阻燃剂的依据有: ①生成固体氧化物隔绝空气,②水蒸气稀释空气,③_______ 。
(1)Fe2+在酸性介质中较稳定,则硫酸亚铁溶液的保存方法为
(2)过二硫酸钾(K2S2O8)具有强氧化性可将 I−氧化为 I2:S2O
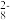 +2I-=2SO
+2I-=2SO +I2。通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示 Fe3+对上述反应催化的过程:① Fe3++2I-= I2+ Fe2+ ②
+I2。通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示 Fe3+对上述反应催化的过程:① Fe3++2I-= I2+ Fe2+ ②(3)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,得到炉渣(含 Fe2O3、FeO、SiO2、Al2O3) 。
该工艺的中间过程会发生反应:2Cu2O+ Cu2S
 6Cu+SO2↑;反应的还原剂是
6Cu+SO2↑;反应的还原剂是| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 加热时,铜可与 O2 直接化合 | 可用铜网除去 N2 中的少量 O2 | Ⅰ对;Ⅱ对;有 |
| B | 铜表面易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
| C | 无水 CuSO4 与水反应得到蓝色晶体 | 常用无水 CuSO4 作气体干燥剂 | Ⅰ对;Ⅱ对;有 |
| D | 硫酸铜溶液显酸性 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
 27H2O↑+10MgO+3A12O3
27H2O↑+10MgO+3A12O3该化合物作阻燃剂的依据有: ①生成固体氧化物隔绝空气,②水蒸气稀释空气,③
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求书写化学方程式或离子方程式。
(1)工业上用将氯气通入石灰乳中制漂白粉,相应的化学方程式为___________ 。
(2)硫酸厂附近的新收集雨水pH不断降低,相应的化学方程式为___________ 。
(3)木炭和浓硫酸混合加热产生大量的CO2和SO2,相应的化学方程式为___________ 。
(4)工业上用FeCl3溶液腐蚀铜线路板,相应的离子 方程式为___________ 。
(5)SO2能使氯水褪色,相应的离子 方程式为___________ 。
(1)工业上用将氯气通入石灰乳中制漂白粉,相应的化学方程式为
(2)硫酸厂附近的新收集雨水pH不断降低,相应的化学方程式为
(3)木炭和浓硫酸混合加热产生大量的CO2和SO2,相应的化学方程式为
(4)工业上用FeCl3溶液腐蚀铜线路板,相应的
(5)SO2能使氯水褪色,相应的
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取可以通过如下反应完成:Na+NaNO3 → Na2O+N2↑(未配平)。
请回答下列问题:
(1)为何不用钠在空气中氧化生成Na2O?____ 。
(2)在上述反应中,N2有何作用?____ 。
(3)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。某学生设计了以下实验方案来测定该样品中Na2O的质量分数,其操作流程和实验数据如图:
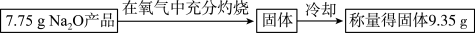
该氧化钠样品中Na2O的质量分数为____ 。
请回答下列问题:
(1)为何不用钠在空气中氧化生成Na2O?
(2)在上述反应中,N2有何作用?
(3)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。某学生设计了以下实验方案来测定该样品中Na2O的质量分数,其操作流程和实验数据如图:
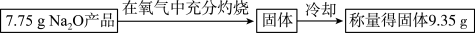
该氧化钠样品中Na2O的质量分数为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求写出相应的方程式
(1)FeSO4的电离方程式________ 。
(2)Na在空气中点燃的化学方程式________ 。
(3)Al(OH)3溶解于NaOH溶液的离子方程式________ 。
(1)FeSO4的电离方程式
(2)Na在空气中点燃的化学方程式
(3)Al(OH)3溶解于NaOH溶液的离子方程式
您最近半年使用:0次



