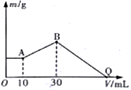
现有一定量的镁铝合金与100 mL稀硝酸充分反应,在反应过程中无气体放出。在反应结束后的溶液中,逐滴加入1.00mol/LNaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量的关系如图所示:
(1)合金中的铝与稀硝酸发生反应的化学方程式为________ 。
(2)纵坐标上A点数值是________ ,B点数值是________ 。
(3)原HNO3溶液中溶质的物质的量浓度为________ 。

(1)合金中的铝与稀硝酸发生反应的化学方程式为
(2)纵坐标上A点数值是
(3)原HNO3溶液中溶质的物质的量浓度为
更新时间:2017-10-23 17:19:31
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为10.00g的该结晶水合物,分别制成溶液。
一份加入足量NaOH溶液,生成蓝色沉淀,将此悬浊液加热,逸出的气体能使湿润的红色石蕊试纸变蓝,此气体恰好可被50.00mL1.00mol/L盐酸完全吸收。同时蓝色沉淀变为黑色沉淀;(提示:NH3被盐酸吸收的反应为:NH3 + HCl = NH4Cl)
另一份加入足量的BaCl2溶液,生成不溶于稀硝酸白色沉淀,经过滤、洗涤、干燥称其质量为11.65g。
试推断并计算10.00g该结晶水合物中三种离子及结晶水的物质的量(写出计算过程)_____________ 。
一份加入足量NaOH溶液,生成蓝色沉淀,将此悬浊液加热,逸出的气体能使湿润的红色石蕊试纸变蓝,此气体恰好可被50.00mL1.00mol/L盐酸完全吸收。同时蓝色沉淀变为黑色沉淀;(提示:NH3被盐酸吸收的反应为:NH3 + HCl = NH4Cl)
另一份加入足量的BaCl2溶液,生成不溶于稀硝酸白色沉淀,经过滤、洗涤、干燥称其质量为11.65g。
试推断并计算10.00g该结晶水合物中三种离子及结晶水的物质的量(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】1.(1)已知20℃时的溶解度:Na2CO3:S=21.2g; NaHCO3:S=9.6g。则20℃恒温条件下向121.2g饱和碳酸钠溶液中通入足量的CO2气体,理论上可以析出NaHCO3__________ g(小数点后保留1位)
(2)向500mL KOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。若通入CO2气体为2.24L(标准状况下),得到11.9g的白色固体。则所用的KOH溶液的物质的量浓度为______ mol/L。
(3)将一定质量的钠加入到89g水中,完全反应后的溶液为100g,则该溶液的质量分数为________
(4)现有甲、乙两瓶无色溶液,已知它们可能是AlCl3溶液和NaOH溶液.现做如下实验:
① 取440mL甲与120mL乙反应,产生1.56g沉淀;
② 取440mL乙与120mL甲反应,也产生1.56g沉淀;
③ 取120mL甲溶液与400mL乙溶液反应,则产生3.12g沉淀;
通过必要的计算和推理判定:
甲溶液为________ 溶液,其物质的量浓度为__________ mol·L-1;
乙溶液为_______ 溶液,其物质的量浓度是___________ mol·L-1
(2)向500mL KOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。若通入CO2气体为2.24L(标准状况下),得到11.9g的白色固体。则所用的KOH溶液的物质的量浓度为
(3)将一定质量的钠加入到89g水中,完全反应后的溶液为100g,则该溶液的质量分数为
(4)现有甲、乙两瓶无色溶液,已知它们可能是AlCl3溶液和NaOH溶液.现做如下实验:
① 取440mL甲与120mL乙反应,产生1.56g沉淀;
② 取440mL乙与120mL甲反应,也产生1.56g沉淀;
③ 取120mL甲溶液与400mL乙溶液反应,则产生3.12g沉淀;
通过必要的计算和推理判定:
甲溶液为
乙溶液为

您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】已知化合物X是由两种短周期元素和一种长周期元素组成的盐,可溶于水,与酸反应只生成两种盐和水,某学习小组进行了如下实验:
①取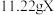 ,加入
,加入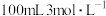 的盐酸,无气体产生,得澄清溶液,将其两等分;
的盐酸,无气体产生,得澄清溶液,将其两等分;
②向其中一份溶液中加入过量的 溶液,过滤,得到溶液A和
溶液,过滤,得到溶液A和 白色沉淀B,B是医疗上的胃肠造影剂;
白色沉淀B,B是医疗上的胃肠造影剂;
③向另一份溶液中逐滴加入 的
的 溶液,当
溶液,当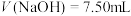 时恰好中和,继续滴加生成白色沉淀,当
时恰好中和,继续滴加生成白色沉淀,当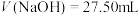 时,沉淀恰好溶解完全。
时,沉淀恰好溶解完全。
请回答:
(1)化合物X中三种元素对应的简单离子,半径最小的离子结构示意图为___________ 。
(2)化合物X的化学式为_______________ 。
(3)将化合物X完全溶于水后,溶液呈强碱性,通入足量 ,生成白色沉淀,写出通入足量
,生成白色沉淀,写出通入足量 所发生反应的离子方程式:
所发生反应的离子方程式:__________________ 。
(4)设计实验检验溶液A中的阴离子(不考虑水的电离):_______________________________ 。
①取
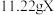 ,加入
,加入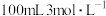 的盐酸,无气体产生,得澄清溶液,将其两等分;
的盐酸,无气体产生,得澄清溶液,将其两等分;②向其中一份溶液中加入过量的
 溶液,过滤,得到溶液A和
溶液,过滤,得到溶液A和 白色沉淀B,B是医疗上的胃肠造影剂;
白色沉淀B,B是医疗上的胃肠造影剂;③向另一份溶液中逐滴加入
 的
的 溶液,当
溶液,当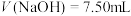 时恰好中和,继续滴加生成白色沉淀,当
时恰好中和,继续滴加生成白色沉淀,当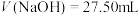 时,沉淀恰好溶解完全。
时,沉淀恰好溶解完全。请回答:
(1)化合物X中三种元素对应的简单离子,半径最小的离子结构示意图为
(2)化合物X的化学式为
(3)将化合物X完全溶于水后,溶液呈强碱性,通入足量
 ,生成白色沉淀,写出通入足量
,生成白色沉淀,写出通入足量 所发生反应的离子方程式:
所发生反应的离子方程式:(4)设计实验检验溶液A中的阴离子(不考虑水的电离):
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】硫酸高铈[Ce(SO4)2]是一种常用的强氧化剂。
(1)将Ce(SO4)2·4H2O(摩尔质量为404g/mol)在空气中加热,样品的固体残留率( )随温度的变化如图所示。
)随温度的变化如图所示。
当固体残留率为70.3%时,所得固体可能为______ (填字母)
A. Ce(SO4)2 B. Ce2(SO4)3 C. CeOSO4
(2)将一定质量的Ce(SO4)2·4H2O溶于50mL质量分数为60%、密度为1.47g/cm3的硫酸中,
再用水定容至l000mL,所得溶液中c(H+)=_______ mol/L
(3)利用Ce(SO4)2标准溶液测定FeC2O4·2H2O(摩尔质量为180g/mol)和Fe(C2O4)3·4H2O(摩尔质量为448g/mol)固体混合物中FeC2O4·2H2O含量的方法如下:
步骤l:称量1.1240g固体混合物,溶于硫酸,向溶液中加入100.00mL 0.2000mol/L的Ce(SO4)2溶液。物质转化关系如下: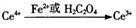
步骤2:将反应后的溶液加水稀释并定容至250.00mL,取25.00mL于锥形瓶中,滴加指示剂,用0.01000mol/LFeSO4标准溶液滴定过量的Ce4+,终点时消耗FeSO4标准溶液20.00mL。
计算固体混合物中FeC2O4·2H2O的质量分数,写出计算过程_______ 。
(1)将Ce(SO4)2·4H2O(摩尔质量为404g/mol)在空气中加热,样品的固体残留率(
 )随温度的变化如图所示。
)随温度的变化如图所示。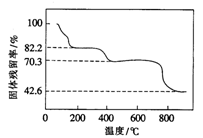
当固体残留率为70.3%时,所得固体可能为
A. Ce(SO4)2 B. Ce2(SO4)3 C. CeOSO4
(2)将一定质量的Ce(SO4)2·4H2O溶于50mL质量分数为60%、密度为1.47g/cm3的硫酸中,
再用水定容至l000mL,所得溶液中c(H+)=
(3)利用Ce(SO4)2标准溶液测定FeC2O4·2H2O(摩尔质量为180g/mol)和Fe(C2O4)3·4H2O(摩尔质量为448g/mol)固体混合物中FeC2O4·2H2O含量的方法如下:
步骤l:称量1.1240g固体混合物,溶于硫酸,向溶液中加入100.00mL 0.2000mol/L的Ce(SO4)2溶液。物质转化关系如下:
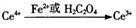
步骤2:将反应后的溶液加水稀释并定容至250.00mL,取25.00mL于锥形瓶中,滴加指示剂,用0.01000mol/LFeSO4标准溶液滴定过量的Ce4+,终点时消耗FeSO4标准溶液20.00mL。
计算固体混合物中FeC2O4·2H2O的质量分数,写出计算过程
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】工业甲醇的质量分数可以用下列方法测定:
①在稀H2SO4中甲醇被Cr2O72—氧化成CO2和H2O,
反应式为:CH3OH+Cr2O72—+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72—可用Fe2+与之完全反应:
___ Cr2O72—+___ Fe2++____ H+—_____ Cr3++____ Fe3++____ H2O
现有0.12 g工业甲醇,在H2SO4溶液中与25 mL 0.2 mol·L-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1 mol·L—1FeSO4与其反应,结果用去FeSO4溶液9.6 mL。
(1)配平第②步的离子方程式。
(2)计算工业甲醇的质量分数_______________ 。
①在稀H2SO4中甲醇被Cr2O72—氧化成CO2和H2O,
反应式为:CH3OH+Cr2O72—+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72—可用Fe2+与之完全反应:
现有0.12 g工业甲醇,在H2SO4溶液中与25 mL 0.2 mol·L-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1 mol·L—1FeSO4与其反应,结果用去FeSO4溶液9.6 mL。
(1)配平第②步的离子方程式。
(2)计算工业甲醇的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】完成下列问题。
(1)已知完全断裂物质的量均为1mol的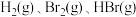 中的化学键时吸收能量分别为
中的化学键时吸收能量分别为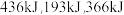 。则在该条件下,
。则在该条件下, 与
与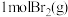 完全反应会
完全反应会_______ (填“吸收”或“放出”)_______  能量。
能量。
(2)将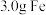 和
和 的混合粉末完全溶于
的混合粉末完全溶于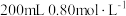 盐酸中,生成标准状况下
盐酸中,生成标准状况下 (假设气体被完全收集);反应后的溶液中滴入2滴
(假设气体被完全收集);反应后的溶液中滴入2滴 溶液后不显血红色。请通过分析计算回答:
溶液后不显血红色。请通过分析计算回答:
①则混合粉末中Fe的物质的量是_______ mol;
②若在反应后的混合液中加入锌,则理论上最多可溶解锌的质量是_______ g。
(1)已知完全断裂物质的量均为1mol的
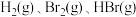 中的化学键时吸收能量分别为
中的化学键时吸收能量分别为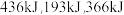 。则在该条件下,
。则在该条件下, 与
与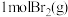 完全反应会
完全反应会 能量。
能量。(2)将
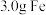 和
和 的混合粉末完全溶于
的混合粉末完全溶于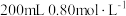 盐酸中,生成标准状况下
盐酸中,生成标准状况下 (假设气体被完全收集);反应后的溶液中滴入2滴
(假设气体被完全收集);反应后的溶液中滴入2滴 溶液后不显血红色。请通过分析计算回答:
溶液后不显血红色。请通过分析计算回答:①则混合粉末中Fe的物质的量是
②若在反应后的混合液中加入锌,则理论上最多可溶解锌的质量是
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】氮及化合物在生产生活中有着重要的作用。请回答下列问题:
(1)连二亚硝酸H2N2O2是一种二元弱酸,在水溶液中缓慢分解,其分解原理与碳酸分解原理相似,请写出连二亚硝酸分解的化学方程式_________________________ 。
(2)有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是3 mol·L-1和1 mol·L-1,取100 mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为____________ (设反应中HNO3被还原成NO)。
(3)足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.5 molO2混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入NaOH溶液至Cu2+恰好完全沉淀,则消耗溶液中NaOH的物质的量为____________ mol
(1)连二亚硝酸H2N2O2是一种二元弱酸,在水溶液中缓慢分解,其分解原理与碳酸分解原理相似,请写出连二亚硝酸分解的化学方程式
(2)有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是3 mol·L-1和1 mol·L-1,取100 mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为
(3)足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.5 molO2混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入NaOH溶液至Cu2+恰好完全沉淀,则消耗溶液中NaOH的物质的量为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石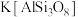 和钠长石
和钠长石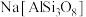 等。回答下列问题:
等。回答下列问题:
(1)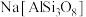 用氧化物形式表示为
用氧化物形式表示为_______ 。
(2)我国科学家发现在200℃熔盐体系中,采用金属Al还原钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能。配平下列方程式:_______ 。
______Al+______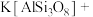 ______
______ →______Si+_____AlOCl+_____
→______Si+_____AlOCl+_____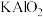 。
。
(3)将钾长石或钠长石用足量稀盐酸处理后,所得固体为_______ (填化学式)。
(4)将一定质量的铝粉和铁粉的混合物加入到一定量很稀的硝酸溶液中,充分反应,反应过程中无气体放出。向反应结束后的溶液中,逐滴加入5mol∙L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量(n)关系如图所示:
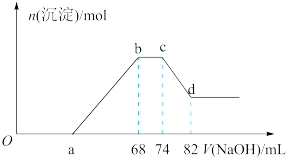
①根据关系图,写出Fe与稀硝酸反应的离子方程式:_______ 。
②样品中铝粉和铁粉的物质的量之比为_______ 。
③a点对应NaOH溶液的体积为_______ 。
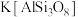 和钠长石
和钠长石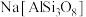 等。回答下列问题:
等。回答下列问题:(1)
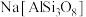 用氧化物形式表示为
用氧化物形式表示为(2)我国科学家发现在200℃熔盐体系中,采用金属Al还原钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能。配平下列方程式:
______Al+______
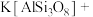 ______
______ →______Si+_____AlOCl+_____
→______Si+_____AlOCl+_____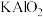 。
。(3)将钾长石或钠长石用足量稀盐酸处理后,所得固体为
(4)将一定质量的铝粉和铁粉的混合物加入到一定量很稀的硝酸溶液中,充分反应,反应过程中无气体放出。向反应结束后的溶液中,逐滴加入5mol∙L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量(n)关系如图所示:

①根据关系图,写出Fe与稀硝酸反应的离子方程式:
②样品中铝粉和铁粉的物质的量之比为
③a点对应NaOH溶液的体积为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
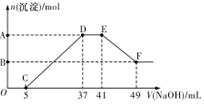
【推荐3】某同学取一定质量的铁铝合金与100 mLxmol/L稀硝酸充分反应,反应过程中没有气体放出。在反应结束后的溶液中,逐滴加入2 mol/L NaOH溶液,所加 NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如图所示:

(1)写出EF段发生反应的离子方程式____________
(2)C点对应的溶液中含有的阳离子除Na+外,还含有_______ 。
(3)x =________ 。
(4)铁铝合金中铝的物质的量分数为_________ 。

(1)写出EF段发生反应的离子方程式
(2)C点对应的溶液中含有的阳离子除Na+外,还含有
(3)x =
(4)铁铝合金中铝的物质的量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】在m毫升b摩/升AlCl3溶液中加入等体积a摩/升NaOH溶液。
(1)当0<a≤3b时,生成Al(OH)3沉淀的物质的量是_______________ 。
(2)当 a=3b时, 生成沉淀_______ 克
(3)当a,b满足___________ 条件时,无沉淀生成。
(4)当3b≤a<4b时,有沉淀生成,生成Al(OH)3沉淀的质量是__________
(1)当0<a≤3b时,生成Al(OH)3沉淀的物质的量是
(2)当 a=3b时, 生成沉淀
(3)当a,b满足
(4)当3b≤a<4b时,有沉淀生成,生成Al(OH)3沉淀的质量是
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58 g白色沉淀析出,向所得的浊液中,逐滴加入0.5 mol·L-1的盐酸,加入盐酸的体积和生成沉淀的质量关系如图所示。

(1)混合物中NaOH的质量是______ g。
(2)P点所表示盐酸加入的体积为______ mL。

(1)混合物中NaOH的质量是
(2)P点所表示盐酸加入的体积为
您最近一年使用:0次