侯德榜制碱法的反应原理为NH3+CO2+H2O+NaCl = NaHCO3↓+NH4Cl,下列装置制取碳酸钠粗品能达到实验目的的是
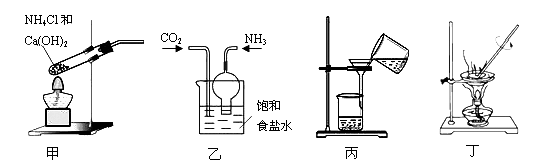

| A.用装置甲制取氨气 | B.用装置乙制取碳酸氢钠 |
| C.用装置丙分离碳酸氢钠 | D.用装置丁加热碳酸氢钠制备碳酸钠 |
更新时间:2017-11-06 19:02:46
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
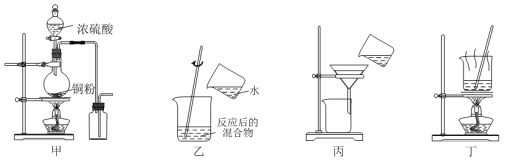
【推荐1】完成下列实验,下图所示仪器和方法均正确的是


| A.装置甲:蒸发结晶,制备NaCl晶体 |
B.装置乙:称量,配制 溶液,称量9.6gNaOH 溶液,称量9.6gNaOH |
C.装置丙:分液,用苯萃取溴水中的 ,打开分液漏斗活塞,在烧杯中收集到溴的苯溶液 ,打开分液漏斗活塞,在烧杯中收集到溴的苯溶液 |
D.装置丁:洗气,除去 中的HCl气体 中的HCl气体 |
您最近一年使用:0次
【推荐2】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,工业上生产NaClO2的一种工艺流程如下,其中纯ClO2易分解爆炸,下列说法错误的是
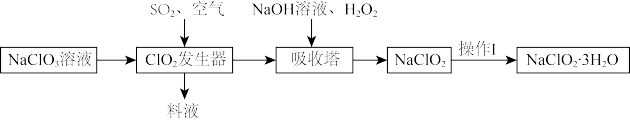

A.空气的作用是氧化 |
B.吸收塔中反应为 |
| C.操作Ⅰ是蒸发浓缩、冷却结晶、过滤、烘干 |
| D.料液中溶质主要是Na2SO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列混合物的分离方法不可行的是
| A.互溶的液体混合物可以用分液的方法进行分离 |
| B.互不相溶的液体混合物可以用分液的方法进行分离 |
| C.沸点不同的混合物可以用蒸馏的方法进行分离 |
| D.可溶于水的固体与难溶于水的固体的混合物可用溶解、过滤的方法进行分离 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关实验的描述或操作错误的是( )
| A.提取海带中碘元素,为保证I - 完全氧化为I 2 , 加入的氧化剂(H 2 O 2 或新制氯水)均应过量 |
| B.纸上层析法通常以滤纸作为惰性支持物。滤纸纤维上的羟基具有亲水性,它所吸附的水作为固定相 |
| C.制备硫酸亚铁铵晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液表面出现晶膜为止,不能将溶液全部蒸干 |
| D.减压过滤不宜用于过滤胶状沉淀或颗粒太小的沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酰氯(SO2Cl2)可用作杀虫剂,通常条件下为无色液体,熔点为-54.1℃,沸点为60.1℃。在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为SO2(g)+Cl2(g)=SO2Cl2(l)△H=-97.3kJ•mol-1,所用装置如图所示。下列叙述错误的是


| A.球形冷凝管B应从a口进水b口出水 |
| B.可通过观察D和E中气泡产生速率控制通入A中的SO2和Cl2的体积比 |
| C.仪器C、D中盛放的试剂依次为无水氯化钙、浓硫酸 |
| D.长期放置的硫酰氯液体会发黄的原因是溶解了氯气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】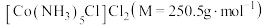 是一种易溶于热水,难溶于乙醇的紫红色晶体。
是一种易溶于热水,难溶于乙醇的紫红色晶体。
(1)制备步骤:将适量氯化铵溶于浓氨水中,边搅拌边分批次加入 研细的
研细的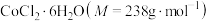 ,得到
,得到 沉淀。边搅拌边慢慢滴入足量
沉淀。边搅拌边慢慢滴入足量 溶液,得到
溶液,得到 溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到
溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到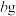 产品。
产品。
(2)钴的测定:取 样品于锥形瓶中,加入
样品于锥形瓶中,加入 溶液并加热使钴(Ⅲ)完全沉淀,后加入
溶液并加热使钴(Ⅲ)完全沉淀,后加入 和
和 将其还原为钴(Ⅱ),再加入
将其还原为钴(Ⅱ),再加入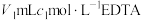 ,用
,用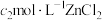 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗
,消耗 溶液平均体积为
溶液平均体积为 与金属阳离子
与金属阳离子 反应)。
反应)。
对于上述实验,下列说法错误的是
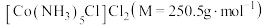 是一种易溶于热水,难溶于乙醇的紫红色晶体。
是一种易溶于热水,难溶于乙醇的紫红色晶体。(1)制备步骤:将适量氯化铵溶于浓氨水中,边搅拌边分批次加入
 研细的
研细的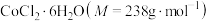 ,得到
,得到 沉淀。边搅拌边慢慢滴入足量
沉淀。边搅拌边慢慢滴入足量 溶液,得到
溶液,得到 溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到
溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到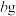 产品。
产品。(2)钴的测定:取
 样品于锥形瓶中,加入
样品于锥形瓶中,加入 溶液并加热使钴(Ⅲ)完全沉淀,后加入
溶液并加热使钴(Ⅲ)完全沉淀,后加入 和
和 将其还原为钴(Ⅱ),再加入
将其还原为钴(Ⅱ),再加入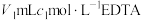 ,用
,用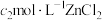 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗
,消耗 溶液平均体积为
溶液平均体积为 与金属阳离子
与金属阳离子 反应)。
反应)。对于上述实验,下列说法错误的是
| A.本实验应在通风橱中进行 |
B.分批次加入研细的 ,目的是防止反应过快 ,目的是防止反应过快 |
C.温度过高不利于 的生成 的生成 |
D.还原性: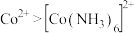 |
您最近一年使用:0次