把少量的MnO2粉末加入50mL过氧化氢的溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
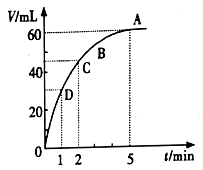
回答下列问题:
(1)实验时放出气体的总体积为________ 。
(2)放出一半气体所需要的时间为________ 。
(3) 反应放出 气体所需要的时间为
气体所需要的时间为________ 。
(4) A、B、C、D各点反应速率的快慢顺序为________ 。
(5)反应速率变化的原因________ 。
(6)可以代替MnO2粉末的物质有(答出1种即可)________ 。

回答下列问题:
(1)实验时放出气体的总体积为
(2)放出一半气体所需要的时间为
(3) 反应放出
 气体所需要的时间为
气体所需要的时间为(4) A、B、C、D各点反应速率的快慢顺序为
(5)反应速率变化的原因
(6)可以代替MnO2粉末的物质有(答出1种即可)
更新时间:2017-11-12 19:46:29
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
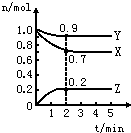
(1)该反应的化学方程式为___________________________ 。
(2)反应开始至2min,以气体Z表示的平均反应速率为______________ 。
(3)平衡时X的转化率为_____________ 。
(4)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:①此时体系内压强与开始时压强之比为________________ ;②达平衡时,容器内混合气体的平均相对分子质量比起始投料时____________________ (填“增大”“减小”或“相等”)。

(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)平衡时X的转化率为
(4)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:①此时体系内压强与开始时压强之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业制硝酸的主要反应为:4NH3(g)+5O2(g)⇌4NO(g)+6H2O(l)△H
(1)已知氢气的燃烧热为△H=﹣285.8kJ/mol.
N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ/mol;
N2(g)+O2(g)═2NO(g)△H=+180.6kJ/mol.
则上述工业制硝酸的主要反应的△H=_____ 。
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如表:
①反应在第2min到第4min时,O2的平均反应速率为_____ 。
②反应在第6min时改变了条件,改变的条件可能是_____ (填序号).
A.使用催化剂 B.升高温度 C.减小压强 D.增加O2的浓度
③下列说法中能说明4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)达到平衡状态的是_____ (填序号).
A.单位时间内生成n mol NO的同时,生成n mol NH3
B.条件一定,混合气体的平均相对分子质量不再变化
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O)=4:5:4:6
E.若在恒温恒压下容积可变的容器中反应,混合气体的密度不再变化
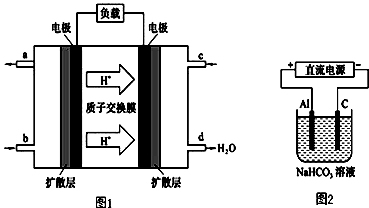
(3)某研究所组装的CH2=CH2﹣O2燃料电池的工作原理如图1所示.
①该电池工作时,b口通入的物质为_____ 。
②该电池负极的电极反应式为:_____ 。
③以此电池作电源,在实验室中模拟铝制品表面“钝化”处理(装置如图2所示)的过程中,发现阳极周围变浑浊并有气泡产生,其原因可能是:_____ (用相关的离子方程式表示)。
(1)已知氢气的燃烧热为△H=﹣285.8kJ/mol.
N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ/mol;
N2(g)+O2(g)═2NO(g)△H=+180.6kJ/mol.
则上述工业制硝酸的主要反应的△H=
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如表:
| 浓度 | c(NH3)(mol/L) | c(O2)(mol/L) | c(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.7 | 1.475 | 0.1 |
①反应在第2min到第4min时,O2的平均反应速率为
②反应在第6min时改变了条件,改变的条件可能是
A.使用催化剂 B.升高温度 C.减小压强 D.增加O2的浓度
③下列说法中能说明4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)达到平衡状态的是
A.单位时间内生成n mol NO的同时,生成n mol NH3
B.条件一定,混合气体的平均相对分子质量不再变化
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O)=4:5:4:6
E.若在恒温恒压下容积可变的容器中反应,混合气体的密度不再变化
(3)某研究所组装的CH2=CH2﹣O2燃料电池的工作原理如图1所示.
①该电池工作时,b口通入的物质为
②该电池负极的电极反应式为:
③以此电池作电源,在实验室中模拟铝制品表面“钝化”处理(装置如图2所示)的过程中,发现阳极周围变浑浊并有气泡产生,其原因可能是:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】甲醇被称为2l世纪的新型燃料,工业上可以用CH4和H2O为原料来制备甲醇。
(1)将1.0molCH4和2.0molH2O(g)通入容积为10L的反应室,在一定条件下发生反应I:CH4(g)+H2O(g) CO(g)+3H2(g),CH4的平衡转化率与温度、压强的关系如图甲:
CO(g)+3H2(g),CH4的平衡转化率与温度、压强的关系如图甲:

①已知100℃,压强为P1时,达到平衡所需的时间为5min,则用H2表示的平均反应速率为______ 。
②在其它条件不变的情况下升高温度,化学平衡常数将___________ (填“增大”“减小”或“不变”)。
③图中的P1___________ P2(填“<”、“>”或“=”),在100℃,压强为P1时平衡常数为___________ 。
④保持反应体系100℃,压强为P1,5min后再向容器中充入H2O、H2各0.5mol,化学平衡将向___________ 移动(填“向左”“向右或“不”)。
(2)在一定条件下,将amolCO与3amolH2的混合气体在催化剂作用下能自发发生反应II:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
①该反应的△H___________ 0(填“<”、“>”或“=”)。
②若容器容积不变,下列措施可以提高CO转化率的是___________ 。
A.升高温度 B.将CH3OH(g)从体系中分离出来
C.充入He,使体系总压强增大 D.再充入一定量的H2
(1)将1.0molCH4和2.0molH2O(g)通入容积为10L的反应室,在一定条件下发生反应I:CH4(g)+H2O(g)
 CO(g)+3H2(g),CH4的平衡转化率与温度、压强的关系如图甲:
CO(g)+3H2(g),CH4的平衡转化率与温度、压强的关系如图甲:
①已知100℃,压强为P1时,达到平衡所需的时间为5min,则用H2表示的平均反应速率为
②在其它条件不变的情况下升高温度,化学平衡常数将
③图中的P1
④保持反应体系100℃,压强为P1,5min后再向容器中充入H2O、H2各0.5mol,化学平衡将向
(2)在一定条件下,将amolCO与3amolH2的混合气体在催化剂作用下能自发发生反应II:CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)①该反应的△H
②若容器容积不变,下列措施可以提高CO转化率的是
A.升高温度 B.将CH3OH(g)从体系中分离出来
C.充入He,使体系总压强增大 D.再充入一定量的H2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO发生如下反应2NO+2CO 2CO2+N2,将NO、CO转化为无毒气体。回答下列问题:
2CO2+N2,将NO、CO转化为无毒气体。回答下列问题:
(1)为了测定在该催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
前4s内的平均反应速率v(CO2)=____ 。0~1s和1~2s时间段内反应速率变化的主要原因是____ 。
(2)一定温度下,在固定容积的密闭容器中,通入1molCO和1molNO,在催化剂作用下发生反应。下列能作为反应达到平衡状态的依据的是____ (填序号)。
a.单位时间内消耗1molCO,同时生成1molNO
b.单位时间内断裂氮氧键的数目与断裂氮氮键的数目相等
c.NO的浓度与CO浓度相等
d.容器内总压强不再改变
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证不同条件对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表格中。
①实验I、II的目的是____ ,实验II选择的实验条件是温度____ 、c(NO)=____ ,c(NO)=____ 。
②对比实验I、III,得出的结论是____ 。
 2CO2+N2,将NO、CO转化为无毒气体。回答下列问题:
2CO2+N2,将NO、CO转化为无毒气体。回答下列问题:(1)为了测定在该催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2,.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(2)一定温度下,在固定容积的密闭容器中,通入1molCO和1molNO,在催化剂作用下发生反应。下列能作为反应达到平衡状态的依据的是
a.单位时间内消耗1molCO,同时生成1molNO
b.单位时间内断裂氮氧键的数目与断裂氮氮键的数目相等
c.NO的浓度与CO浓度相等
d.容器内总压强不再改变
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证不同条件对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表格中。
| 实验编号 | T/℃ | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 催化剂的比表面积/m2•g-1 |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 124 | |||
| III | 350 | 1.20×10-3 | 5.80×10-3 | 82 |
②对比实验I、III,得出的结论是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】为探究化学反应速率的影响因素,学生设计了锌与过量的c mol/L 100mL盐酸起反应的实验,得到了下面的结果:
(1)上述实验中①②③④是探究_____________ 对化学反应速率的影响;__________ (填序号)是探究固体表面积对化学反应速率的影响。
(2)下列说法正确的是___________ 。
a.t1=75s b. 100﹥t2﹥t3
c.单位时间内耗锌的质量⑤﹥⑥﹥②
d.以上都不正确
(3)②中气泡生成的速率与时间的关系大致如图。推测从0到t速率不减反增的原因可能是________________________ 。

(4)某同学为了探究化学腐蚀与电化学腐蚀的速率,设计实验与②进行对照。操作如下: 25℃时,另取一个烧杯,放入与实验②完全相同的锌片,先加入2mL某浓度的_________ 溶液,再加入与②相同的盐酸。可以观察到__________________ 。
| 序号 | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶解于酸的时间/s |
| ① | 2.0 | 薄片 | 15 | 200 |
| ② | 2.0 | 薄片 | 25 | 100 |
| ③ | 2.0 | 薄片 | 30 | t1 |
| ④ | 2.0 | 薄片 | 35 | 50 |
| ⑤ | 2.0 | 颗粒 | 25 | t2 |
| ⑥ | 2.0 | 粉末 | 25 | t3 |
(1)上述实验中①②③④是探究
(2)下列说法正确的是
a.t1=75s b. 100﹥t2﹥t3
c.单位时间内耗锌的质量⑤﹥⑥﹥②
d.以上都不正确
(3)②中气泡生成的速率与时间的关系大致如图。推测从0到t速率不减反增的原因可能是

(4)某同学为了探究化学腐蚀与电化学腐蚀的速率,设计实验与②进行对照。操作如下: 25℃时,另取一个烧杯,放入与实验②完全相同的锌片,先加入2mL某浓度的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】可逆反应2SO2(g)+O2(g)  2SO3(g)是工业上制取H2SO4的重要反应。
2SO3(g)是工业上制取H2SO4的重要反应。
(1)在恒压条件下,该反应分组实验的有关条件如下表:
已知Ⅰ、Ⅱ两组实验过程中,SO3气体的体积分数φ(SO3)随时间t的变化曲线如图所示。
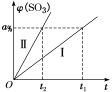
①Ⅱ组与Ⅰ相比不同的条件是___________ ;
②将Ⅰ组实验中温度变为800 ℃,则φ(SO3)达到a%所需时间___________ t1(填“小于”“大于”或“等于”)。
(2)向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小排列的是___________。
甲:在500 ℃时,10 mol SO2和10 mol O2反应
乙:在500 ℃时,用V2O5作催化剂,10 mol SO2和10 mol O2反应
丙:在450 ℃时,8 mol SO2和5 mol O2反应
丁:在500 ℃时,8 mol SO2和5 mol O2反应
 2SO3(g)是工业上制取H2SO4的重要反应。
2SO3(g)是工业上制取H2SO4的重要反应。(1)在恒压条件下,该反应分组实验的有关条件如下表:
| 反应条件 | 温度 | 容器容积 | 起始n(SO2) | 起始n(O2) | 其他条件 |
| Ⅰ组 | 500 ℃ | 1 L | 1 mol | 2 mol | 无 |
| Ⅱ组 | 500 ℃ | 1 L | 1 mol | 2 mol |

①Ⅱ组与Ⅰ相比不同的条件是
②将Ⅰ组实验中温度变为800 ℃,则φ(SO3)达到a%所需时间
(2)向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小排列的是___________。
甲:在500 ℃时,10 mol SO2和10 mol O2反应
乙:在500 ℃时,用V2O5作催化剂,10 mol SO2和10 mol O2反应
丙:在450 ℃时,8 mol SO2和5 mol O2反应
丁:在500 ℃时,8 mol SO2和5 mol O2反应
| A.甲、乙、丙、丁 | B.乙、甲、丙、丁 |
| C.乙、甲、丁、丙 | D.丁、丙、乙、甲 |
您最近一年使用:0次



