某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
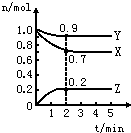
(1)该反应的化学方程式为___________________________ 。
(2)反应开始至2min,以气体Z表示的平均反应速率为______________ 。
(3)平衡时X的转化率为_____________ 。
(4)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:①此时体系内压强与开始时压强之比为________________ ;②达平衡时,容器内混合气体的平均相对分子质量比起始投料时____________________ (填“增大”“减小”或“相等”)。

(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)平衡时X的转化率为
(4)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:①此时体系内压强与开始时压强之比为
更新时间:2017-09-07 06:29:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
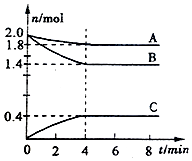
【推荐1】根据如图所示图象填空:
(1)生成物是__ (填A、B、C)。
(2)在2min内用A、C表示的化学反应速率分别为__ ,__ 。
(3)该反应的化学方程式是__ 。

(1)生成物是
(2)在2min内用A、C表示的化学反应速率分别为
(3)该反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有三个反应:
反应① Fe(s)+H2O(g) FeO(s)+H2(g) △H1 平衡常数为K1
FeO(s)+H2(g) △H1 平衡常数为K1
反应② CO(g)+H2O(g) H2(g)+CO2(g) △H2 平衡常数为K2
H2(g)+CO2(g) △H2 平衡常数为K2
反应③ Fe(s)+CO2 (g) FeO(s)+CO(g) △H3 平衡常数为K3
FeO(s)+CO(g) △H3 平衡常数为K3
在不同温度下,部分K1、K2的值如下:
(1)K1的表达式为________ ;根据反应①、②、③推导出K1、K2、K3的关系式K3=______ 。
(2)要使反应①在一定条件下建立的平衡右移,可采取的措施有_________ 。(填字母)
A.缩小容器体积 B.降低温度 C.升高温度
D.使用合适的催化剂 E.设法减少H2的量 F.设法减少FeO的量
(3)800℃时,向容积为2L的恒容密闭容器中充入一定量的CO和H2O维持恒温,发生反应②,反应过程中测定的部分数据见下表:
①反应在2 min内的平均速率为v(H2O)=________________ ;
②800℃时,K2的值为_______________ ;
③保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率_______________ (填“增大”或“减小”或“不变”)。
(4)由以上信息推断反应③正反应方向为________ (填“放热”或“吸热”)反应。
反应① Fe(s)+H2O(g)
 FeO(s)+H2(g) △H1 平衡常数为K1
FeO(s)+H2(g) △H1 平衡常数为K1反应② CO(g)+H2O(g)
 H2(g)+CO2(g) △H2 平衡常数为K2
H2(g)+CO2(g) △H2 平衡常数为K2反应③ Fe(s)+CO2 (g)
 FeO(s)+CO(g) △H3 平衡常数为K3
FeO(s)+CO(g) △H3 平衡常数为K3在不同温度下,部分K1、K2的值如下:
| T/℃ | 700 | 800 |
| K1 | 2.38 | 2.56 |
| K2 | 0.80 |
(1)K1的表达式为
(2)要使反应①在一定条件下建立的平衡右移,可采取的措施有
A.缩小容器体积 B.降低温度 C.升高温度
D.使用合适的催化剂 E.设法减少H2的量 F.设法减少FeO的量
(3)800℃时,向容积为2L的恒容密闭容器中充入一定量的CO和H2O维持恒温,发生反应②,反应过程中测定的部分数据见下表:
| 反应时间/min | 0 | 2 | 4 | 6 |
| n(CO)/mol | 1.20 | 0.90 | 0.80 | |
| n(H2O)/ mol | 0.60 | 0.20 |
①反应在2 min内的平均速率为v(H2O)=
②800℃时,K2的值为
③保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率
(4)由以上信息推断反应③正反应方向为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】我国在汽车尾气和燃煤尾气的净化方面取得了一定成效。汽车尾气净化的主要原理为 。在密闭容器中发生该反应时,
。在密闭容器中发生该反应时, 随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
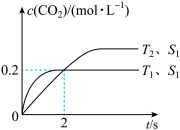
(1) 温度下,
温度下, 内的平均反应速率
内的平均反应速率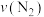
___________ 。
(2)当固体催化剂的质量一定时,将催化剂磨成粉末,则反应速率___________ (填“增大”“减小”或“不变”,下同), 转化率
转化率___________ 。
(3)若在绝热、恒容的密闭体系中充入一定量的 和
和 气体进行该反应,下列示意图正确且能说明反应在进行到
气体进行该反应,下列示意图正确且能说明反应在进行到 时刻达到平衡状态的是
时刻达到平衡状态的是___________ (填序号)。
a.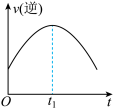 b.
b.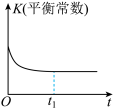 c.
c.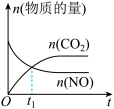 d.
d.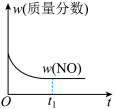
 。在密闭容器中发生该反应时,
。在密闭容器中发生该反应时, 随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
(1)
 温度下,
温度下, 内的平均反应速率
内的平均反应速率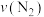
(2)当固体催化剂的质量一定时,将催化剂磨成粉末,则反应速率
 转化率
转化率(3)若在绝热、恒容的密闭体系中充入一定量的
 和
和 气体进行该反应,下列示意图正确且能说明反应在进行到
气体进行该反应,下列示意图正确且能说明反应在进行到 时刻达到平衡状态的是
时刻达到平衡状态的是a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】汽车等交通工具为出行、物流带来了舒适和方便。然而,燃油车排放的尾气中含有大量的氮氧化物。NOx的处理是环境科学研究的热点课题,利用活性炭对NO进行吸附。
(1)向容积为2 L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g) N2(g)+CO2(g) ΔH= -34.0 kJ·mol-1,NO和N2的物质的量变化如表所示:
N2(g)+CO2(g) ΔH= -34.0 kJ·mol-1,NO和N2的物质的量变化如表所示:
① 0-5 min内,以N2表示该反应速率v(N2)=______ ,第15 min后,将温度调整为T2,数据变化如上表所示,则T1______ T2(填“>、< 或 =”)。
② 若为绝热恒容容器,下列表示该反应已达到平衡状态的是______ (填字母)。
A.混合气体的密度不再变化 B.温度不再变化
C.NO和 的消耗速率之比为1:2 D.混合气体中c(NO) = c(N2)
的消耗速率之比为1:2 D.混合气体中c(NO) = c(N2)
(2)恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时NO的转化率随温度的变化如图所示:
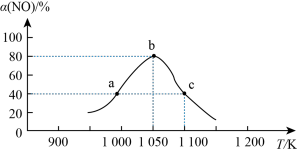
图中a、b、c三点,达到平衡的点是______ 。
(3)现代技术处理尾气的反应原理是 NO(g) + NO2(g) + 2NH3(g) 3H2O(g) + 2N2(g) ΔH < 0。450 ℃时,在2 L恒容密闭容器中充入1 mol NO、1 mol NO2和2 mol NH3,12 min时反应达到平衡,此时
3H2O(g) + 2N2(g) ΔH < 0。450 ℃时,在2 L恒容密闭容器中充入1 mol NO、1 mol NO2和2 mol NH3,12 min时反应达到平衡,此时 的转化率为50%,体系压强为P0 MPa。450℃时该反应的平衡常数Kp =
的转化率为50%,体系压强为P0 MPa。450℃时该反应的平衡常数Kp =______ (用含P0的代数式表示,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
(1)向容积为2 L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)
 N2(g)+CO2(g) ΔH= -34.0 kJ·mol-1,NO和N2的物质的量变化如表所示:
N2(g)+CO2(g) ΔH= -34.0 kJ·mol-1,NO和N2的物质的量变化如表所示:物质的量/mol | T1/℃ | T2/℃ | |||||
0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
② 若为绝热恒容容器,下列表示该反应已达到平衡状态的是
A.混合气体的密度不再变化 B.温度不再变化
C.NO和
 的消耗速率之比为1:2 D.混合气体中c(NO) = c(N2)
的消耗速率之比为1:2 D.混合气体中c(NO) = c(N2)(2)恒压密闭容器中加入足量活性炭和一定量NO气体,反应相同时间时NO的转化率随温度的变化如图所示:

图中a、b、c三点,达到平衡的点是
(3)现代技术处理尾气的反应原理是 NO(g) + NO2(g) + 2NH3(g)
 3H2O(g) + 2N2(g) ΔH < 0。450 ℃时,在2 L恒容密闭容器中充入1 mol NO、1 mol NO2和2 mol NH3,12 min时反应达到平衡,此时
3H2O(g) + 2N2(g) ΔH < 0。450 ℃时,在2 L恒容密闭容器中充入1 mol NO、1 mol NO2和2 mol NH3,12 min时反应达到平衡,此时 的转化率为50%,体系压强为P0 MPa。450℃时该反应的平衡常数Kp =
的转化率为50%,体系压强为P0 MPa。450℃时该反应的平衡常数Kp =
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
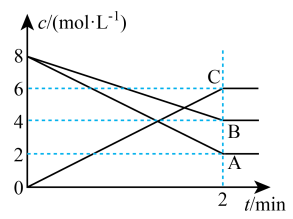
【推荐2】某温度时,在一个容积为4 L 的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:
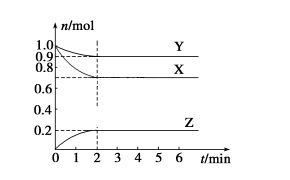
(1)该反应的化学方程式为:_________________ 。
(2)反应开始至2min,气体X的平均反应速率v(X)=____________ 。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的________ 倍;
②若此时将容器的体积缩小为1L,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为________ 反应(填“放热”或“吸热”)。
(4)上述反应在t1~t6内反应速率与时间图象如图,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是______________ 。
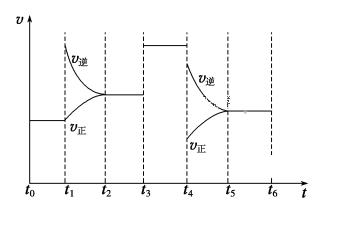
A.在t1时增大了压强 B.在t3时加入了催化剂
C.在t4时降低了温度 D.t2~t3时X的转化率最高

(1)该反应的化学方程式为:
(2)反应开始至2min,气体X的平均反应速率v(X)=
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的
②若此时将容器的体积缩小为1L,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
(4)上述反应在t1~t6内反应速率与时间图象如图,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是

A.在t1时增大了压强 B.在t3时加入了催化剂
C.在t4时降低了温度 D.t2~t3时X的转化率最高
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】近日IPCC发布了由来自 个国家的
个国家的 位科学家编写的《全球升温
位科学家编写的《全球升温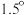 特别报告》,温室效应引发的环境问题日益严重,物种灭绝,洪灾、旱灾、粮食欠收等自然灾害发生频率不断增加,
特别报告》,温室效应引发的环境问题日益严重,物种灭绝,洪灾、旱灾、粮食欠收等自然灾害发生频率不断增加, 的减排和综合利用是解决温室及能源问题的有效途径。
的减排和综合利用是解决温室及能源问题的有效途径。
(1) 可转化成有机物实现碳循环,在体积为1L的密闭容器中,充入
可转化成有机物实现碳循环,在体积为1L的密闭容器中,充入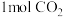 和
和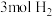 ,一定条件下反应:
,一定条件下反应: ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
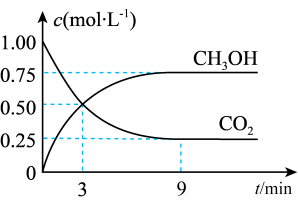
下列说法正确的是_______ (填字母)。
A.混合气体的密度不随时间的变化而变化,则说明上述反应达到平衡状态
B.平衡时 的转化率为
的转化率为
C.平衡时混合气体中 的体积分数是
的体积分数是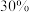
D.该条件下,第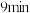 时
时 大于第
大于第 时
时 。
。
(2)工业中, 和
和 在催化剂
在催化剂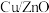 作用下可发生两个平行反应,分别生成
作用下可发生两个平行反应,分别生成 和
和 。
。
反应A:
反应B:
控制 和
和 初始投料比为
初始投料比为 时,温度对
时,温度对 平衡转化率及甲醇和CO产率的影响如图所示。
平衡转化率及甲醇和CO产率的影响如图所示。
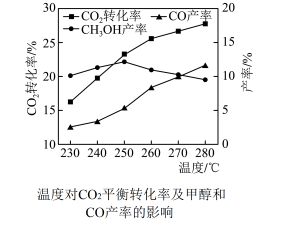
①由图可知温度升高CO的产率上升,其主要原因可能是_______ ;
②由图可知获取 最适宜的温度是
最适宜的温度是_______ ,下列措施有利于提高 转化为
转化为 的平衡转化率的有
的平衡转化率的有_______ (填字母);
A.使用催化剂
B.增大体系压强
C.增大 和
和 的初始投料比
的初始投料比
D.投料比不变和容器体积不变,增加反应物的浓度
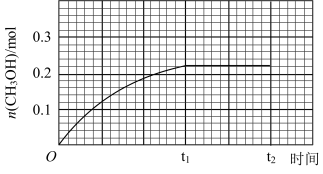
(3) 下
下 物质的量随时间的变化曲线如图所示。画出
物质的量随时间的变化曲线如图所示。画出 下
下 时刻
时刻 物质的量随时间的变化曲线示意图
物质的量随时间的变化曲线示意图_______ 。
 个国家的
个国家的 位科学家编写的《全球升温
位科学家编写的《全球升温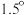 特别报告》,温室效应引发的环境问题日益严重,物种灭绝,洪灾、旱灾、粮食欠收等自然灾害发生频率不断增加,
特别报告》,温室效应引发的环境问题日益严重,物种灭绝,洪灾、旱灾、粮食欠收等自然灾害发生频率不断增加, 的减排和综合利用是解决温室及能源问题的有效途径。
的减排和综合利用是解决温室及能源问题的有效途径。(1)
 可转化成有机物实现碳循环,在体积为1L的密闭容器中,充入
可转化成有机物实现碳循环,在体积为1L的密闭容器中,充入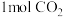 和
和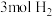 ,一定条件下反应:
,一定条件下反应: ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
下列说法正确的是
A.混合气体的密度不随时间的变化而变化,则说明上述反应达到平衡状态
B.平衡时
 的转化率为
的转化率为
C.平衡时混合气体中
 的体积分数是
的体积分数是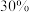
D.该条件下,第
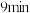 时
时 大于第
大于第 时
时 。
。(2)工业中,
 和
和 在催化剂
在催化剂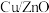 作用下可发生两个平行反应,分别生成
作用下可发生两个平行反应,分别生成 和
和 。
。反应A:

反应B:

控制
 和
和 初始投料比为
初始投料比为 时,温度对
时,温度对 平衡转化率及甲醇和CO产率的影响如图所示。
平衡转化率及甲醇和CO产率的影响如图所示。
①由图可知温度升高CO的产率上升,其主要原因可能是
②由图可知获取
 最适宜的温度是
最适宜的温度是 转化为
转化为 的平衡转化率的有
的平衡转化率的有A.使用催化剂
B.增大体系压强
C.增大
 和
和 的初始投料比
的初始投料比D.投料比不变和容器体积不变,增加反应物的浓度
(3)
 下
下 物质的量随时间的变化曲线如图所示。画出
物质的量随时间的变化曲线如图所示。画出 下
下 时刻
时刻 物质的量随时间的变化曲线示意图
物质的量随时间的变化曲线示意图
您最近一年使用:0次
【推荐2】(1)CH4氧化器中发生的主反应:
i.CH4(g)+Fe3O4(s)⇌CO(g)+2H2(g)+3FeO(s)
ii.CH4(g)+4Fe3O4(s)⇌CO2(g)+2H2O(g)+12FeO(s)
850 时,压强和部分气体体积分数、固相各组分质量分数的关系如图。
时,压强和部分气体体积分数、固相各组分质量分数的关系如图。
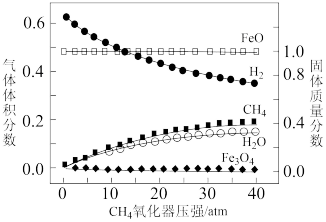
①随着压强的增大,反应i的平衡常数K值____ (填“增大”、“减小”或“不变”)。
②结合图像,分析H2O的体积分数变化的原因_________ (用化学方程式表示)。
(2)将一定量的FeO和CO2置于CO2还原器(体积不变的密闭容器)中,发生的主反应:
CO2(g)+3FeO(s)⇌Fe3O4(s)+CO(g) ΔH2,保持其他条件不变,测得不同温度下最终反应体系中CO、CO2体积分数如下表。
①ΔH2_____ 0(填“>”或“<”)。
②若在150 时进行上述转化,理论转化率α(FeO)=
时进行上述转化,理论转化率α(FeO)=______ 。
③在上述反应体系中,一定可以说明该反应达到平衡状态的是_____ (填标号)。
A.体系的压强不变
B.CO2的物质的量不变
C.CO的生成速率和消耗速率相等且不等于零
D.气体的平均摩尔质量不变
④根据化学反应原理,分析CO2还原器温度设置在170 的原因
的原因_________ 。
i.CH4(g)+Fe3O4(s)⇌CO(g)+2H2(g)+3FeO(s)
ii.CH4(g)+4Fe3O4(s)⇌CO2(g)+2H2O(g)+12FeO(s)
850
 时,压强和部分气体体积分数、固相各组分质量分数的关系如图。
时,压强和部分气体体积分数、固相各组分质量分数的关系如图。
①随着压强的增大,反应i的平衡常数K值
②结合图像,分析H2O的体积分数变化的原因
(2)将一定量的FeO和CO2置于CO2还原器(体积不变的密闭容器)中,发生的主反应:
CO2(g)+3FeO(s)⇌Fe3O4(s)+CO(g) ΔH2,保持其他条件不变,测得不同温度下最终反应体系中CO、CO2体积分数如下表。
温度t/ | 100 | 170 | 200 | 300 | 400 | 500 |
| CO2体积分数 | 0.67 | 0.67 | 0.75 | 0.82 | 0.9 | 0.92 |
| CO体积分数 | 0.33 | 0.33 | 0.25 | 0.18 | 0.1 | 0.08 |
①ΔH2
②若在150
 时进行上述转化,理论转化率α(FeO)=
时进行上述转化,理论转化率α(FeO)=③在上述反应体系中,一定可以说明该反应达到平衡状态的是
A.体系的压强不变
B.CO2的物质的量不变
C.CO的生成速率和消耗速率相等且不等于零
D.气体的平均摩尔质量不变
④根据化学反应原理,分析CO2还原器温度设置在170
 的原因
的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将气体A、B置于2L的刚性密闭绝热容器中,发生如下反应: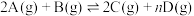 ,反应进行到20s末,测得A的物质的量为
,反应进行到20s末,测得A的物质的量为 ,C的物质的量为
,C的物质的量为 ,20s内D的反应速率为
,20s内D的反应速率为 ,则:
,则:
(1)用C表示20s内反应的平均反应速率为______  。
。
(2)生成物D的化学计量数n为______ 。
(3)20s末反应物A的转化率为______ 。
(4)反应进程中,正反应速率随时间的变化曲线如图所示:
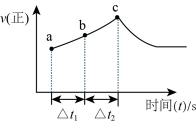
①该反应为______ 反应(填“吸热”或“放热”),理由是______ 。
②反应在c点处
______  (填“>”或“=”或“<”)。
(填“>”或“=”或“<”)。
③若 ,反应物B的转化率:ab段
,反应物B的转化率:ab段______ bc段(填“>”或“=”或“<”)。
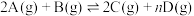 ,反应进行到20s末,测得A的物质的量为
,反应进行到20s末,测得A的物质的量为 ,C的物质的量为
,C的物质的量为 ,20s内D的反应速率为
,20s内D的反应速率为 ,则:
,则:(1)用C表示20s内反应的平均反应速率为
 。
。(2)生成物D的化学计量数n为
(3)20s末反应物A的转化率为
(4)反应进程中,正反应速率随时间的变化曲线如图所示:
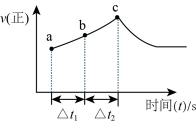
①该反应为
②反应在c点处

 (填“>”或“=”或“<”)。
(填“>”或“=”或“<”)。③若
 ,反应物B的转化率:ab段
,反应物B的转化率:ab段
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某温度下,在2L的密闭容器中,X、Y、Z三种物质随时间变化的曲线如图所示.请回答下列问题
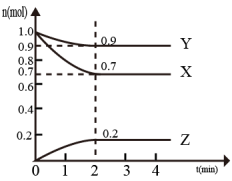
(1)由图中数据分析,该反应的化学方程式为___________________________
(2)反应开始至2min,Z的平均反应速率为________
(3)3min时,Z的生成速率与Z的消耗速率相比较,前者________ (填“大于”“小于”或“等于”)后者.
(4)上述反应进行过程中,如果降低温度,则其反应速率________ (填“增大”“减小”或“不变”).
(5)下列各项中不可以说明上述反应达到平衡的是________ (填字母).
a.生成1molZ和同时生成1.5molX b. X、Y、Z的反应速率之比为3:2:1
c.同一物质的正反应速率等于逆反应速率 d.X的浓度保持不变

(1)由图中数据分析,该反应的化学方程式为
(2)反应开始至2min,Z的平均反应速率为
(3)3min时,Z的生成速率与Z的消耗速率相比较,前者
(4)上述反应进行过程中,如果降低温度,则其反应速率
(5)下列各项中不可以说明上述反应达到平衡的是
a.生成1molZ和同时生成1.5molX b. X、Y、Z的反应速率之比为3:2:1
c.同一物质的正反应速率等于逆反应速率 d.X的浓度保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】工业上先将煤转化为CO,再利用CO和水蒸气反应制H2时,存在以下平衡:CO(g)+H2O(g)⇌CO2(g)+H2(g)。
(1)平衡常数的表达式K=_________________________
(2)向1L恒容密闭容器中充入CO和H2O(g),某温度时测得部分数据如下表。
则从反应开始到2min时,用H2表示的反应速率为__________ ;该温度下反应的平衡常数K=________ (小数点后保留2位有效数字)。
(3)已知该反应在不同的温度下的平衡常数数值分别为
①根据表中的数据判断,该反应为________ (填“吸热”或“放热”)反应。
②800℃,向2L恒容密闭容器中充入1molCO(g)、1molH2O(g)、2molCO2(g)、2molH2(g),此时v正_______ v逆 (填“>”“<”或“=”)。
(1)平衡常数的表达式K=
(2)向1L恒容密闭容器中充入CO和H2O(g),某温度时测得部分数据如下表。
| t/min | 0 | 1 | 2 | 3 | 4 |
| n(H2O)/mol | 1.20 | 1.04 | 0.90 | 0.70 | 0.70 |
| n(CO)/mol | 0.80 | 0.64 | 0.50 | 0.30 | 0.30 |
则从反应开始到2min时,用H2表示的反应速率为
(3)已知该反应在不同的温度下的平衡常数数值分别为
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.19 | 1.00 | 0.60 | 0.38 |
①根据表中的数据判断,该反应为
②800℃,向2L恒容密闭容器中充入1molCO(g)、1molH2O(g)、2molCO2(g)、2molH2(g),此时v正
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知2SO2(g)+O2(g) 2SO3(g) △H=-196.6kJ/mol)
2SO3(g) △H=-196.6kJ/mol)
(1)根据上表下列说法正确的是__________ 。
A.2c1>c3 B.a+b=196.6 C.2p2<p3 D. α1+α2<1
(2)甲容器中的进行反应的平衡常数表达式_________________ 。
(3)甲容器平衡时SO2的转化率____________ (用含有a的代数式表示)
(4)关于2SO2(g)+O2(g) 2SO3(g)下列说法正确的是
2SO3(g)下列说法正确的是__________ 。
A.保持容器等温等压状态,待反应平衡后,再加1mol SO3重新平衡,SO3体积分数小于原平衡
B.平衡时,测得SO2的转化率为12. 5%,O2的转化率为25%,开始充入容器中的SO2、O2物质的量之比为4∶1
C.反应混合物中,SO3的质量分数不再改变时反应处于平衡
D.保持容器等温等容状态,待反应平衡后,再加1mol SO3重新平衡,SO3体积分数小于原平衡
 2SO3(g) △H=-196.6kJ/mol)
2SO3(g) △H=-196.6kJ/mol)| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol SO2、1mol O2 | 2mol SO3 | 4mol SO3 |
| SO3的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
(1)根据上表下列说法正确的是
A.2c1>c3 B.a+b=196.6 C.2p2<p3 D. α1+α2<1
(2)甲容器中的进行反应的平衡常数表达式
(3)甲容器平衡时SO2的转化率
(4)关于2SO2(g)+O2(g)
 2SO3(g)下列说法正确的是
2SO3(g)下列说法正确的是A.保持容器等温等压状态,待反应平衡后,再加1mol SO3重新平衡,SO3体积分数小于原平衡
B.平衡时,测得SO2的转化率为12. 5%,O2的转化率为25%,开始充入容器中的SO2、O2物质的量之比为4∶1
C.反应混合物中,SO3的质量分数不再改变时反应处于平衡
D.保持容器等温等容状态,待反应平衡后,再加1mol SO3重新平衡,SO3体积分数小于原平衡
您最近一年使用:0次