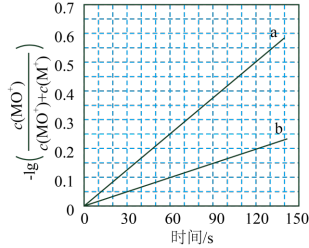
将气体A、B置于2L的刚性密闭绝热容器中,发生如下反应: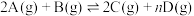 ,反应进行到20s末,测得A的物质的量为
,反应进行到20s末,测得A的物质的量为 ,C的物质的量为
,C的物质的量为 ,20s内D的反应速率为
,20s内D的反应速率为 ,则:
,则:
(1)用C表示20s内反应的平均反应速率为______  。
。
(2)生成物D的化学计量数n为______ 。
(3)20s末反应物A的转化率为______ 。
(4)反应进程中,正反应速率随时间的变化曲线如图所示:
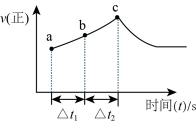
①该反应为______ 反应(填“吸热”或“放热”),理由是______ 。
②反应在c点处
______  (填“>”或“=”或“<”)。
(填“>”或“=”或“<”)。
③若 ,反应物B的转化率:ab段
,反应物B的转化率:ab段______ bc段(填“>”或“=”或“<”)。
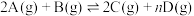 ,反应进行到20s末,测得A的物质的量为
,反应进行到20s末,测得A的物质的量为 ,C的物质的量为
,C的物质的量为 ,20s内D的反应速率为
,20s内D的反应速率为 ,则:
,则:(1)用C表示20s内反应的平均反应速率为
 。
。(2)生成物D的化学计量数n为
(3)20s末反应物A的转化率为
(4)反应进程中,正反应速率随时间的变化曲线如图所示:
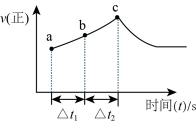
①该反应为
②反应在c点处

 (填“>”或“=”或“<”)。
(填“>”或“=”或“<”)。③若
 ,反应物B的转化率:ab段
,反应物B的转化率:ab段
更新时间:2023-10-25 14:07:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】合成氨是人工固氮的主要手段,对人类生存、社会进步和经济发展都有着重大意义。
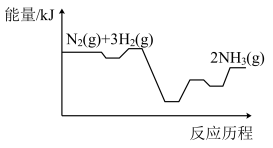
(1)下列物质间能量的变化与合成氨的能量变化(如图所示)相符的是___________(填标号)。
(2)一定温度下,在2L的某恒容密闭容器中,通入0.1mol 和0.3mol
和0.3mol ,发生反应
,发生反应
 ,5min后,该反应达到平衡,此时测得体系的总压强为起始时总压强的
,5min后,该反应达到平衡,此时测得体系的总压强为起始时总压强的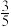 ,则:
,则:
①反应达到平衡时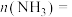
___________ mol。
②0~5min内,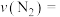
___________  。
。
③为了加快该反应的速率,除加入合适的催化剂,升高温度外,还可采取的措施为___________ (写一种即可)。
(3)利用反应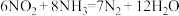 为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
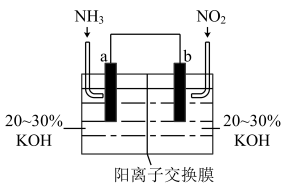
①电池工作时,电解质溶液中的 穿过阳离子交换膜向
穿过阳离子交换膜向___________ (填“a”或“b”)电极移动。
②b电极上的电极反应式为___________ 。
③电池工作一段时间后,左侧工作室溶液的pH___________ (填“变大”、“变小”或“不变”)。
(1)下列物质间能量的变化与合成氨的能量变化(如图所示)相符的是___________(填标号)。

| A.盐酸与碳酸氢钠的反应 | B.氢氧化钡与氯化铵的反应 |
| C.铝片与稀硫酸的反应 | D.氢气与氯气的反应 |
 和0.3mol
和0.3mol ,发生反应
,发生反应
 ,5min后,该反应达到平衡,此时测得体系的总压强为起始时总压强的
,5min后,该反应达到平衡,此时测得体系的总压强为起始时总压强的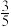 ,则:
,则:①反应达到平衡时
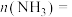
②0~5min内,
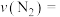
 。
。③为了加快该反应的速率,除加入合适的催化剂,升高温度外,还可采取的措施为
(3)利用反应
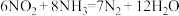 为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
①电池工作时,电解质溶液中的
 穿过阳离子交换膜向
穿过阳离子交换膜向②b电极上的电极反应式为
③电池工作一段时间后,左侧工作室溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】随着“碳达峰”、“碳中和”战略的提出,大气中CO2含量的控制和回收利用已成为当今化学研究的主题。
(1)科学家以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。______ 转化为______ 。过程①中TiO2发生了______ 反应(填“氧化”或“还原”)。根据数据计算,分解2molCO2需吸收______ kJ的能量。
(2)利用光解海水产生的H2将CO2转化为甲醇有利于减少温室气体二氧化碳排放,反应的化学方程式:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是
CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是______ (填标号)。
(3)某温度下,向2L的恒容密闭容器充入6molCO2和8molH2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。
CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。______ mol•L-1•min-1;4min时,v正(H2)______ (填“>”“<”或“=”)v逆(H2)。
②能作为反应达到平衡状态的依据的是______ (填序号)。
a.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
b.容器内混合气体的密度不再改变
c.容器内总压强不再改变
d.单位时间内断裂3mol的H-H键,同时生成1mol的C=O键
(1)科学家以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
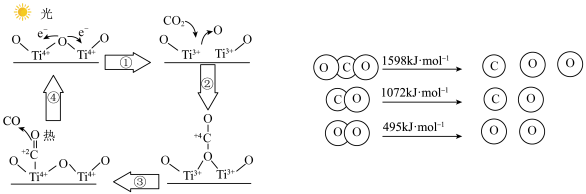
(2)利用光解海水产生的H2将CO2转化为甲醇有利于减少温室气体二氧化碳排放,反应的化学方程式:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是
CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是| A.减小容器体积 | B.升高温度 |
| C.使用合适催化剂 | D.恒容条件下充入He |
(3)某温度下,向2L的恒容密闭容器充入6molCO2和8molH2,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。
CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。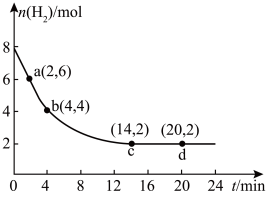
②能作为反应达到平衡状态的依据的是
a.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
b.容器内混合气体的密度不再改变
c.容器内总压强不再改变
d.单位时间内断裂3mol的H-H键,同时生成1mol的C=O键
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】能源是现代社会发展的支柱之一。请回答下列问题:
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是___________ (填字母)。
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
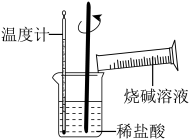
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是__________ (填“吸热”或“放热”)反应,其离子方程式是____________ 。
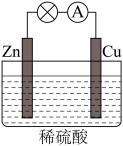
(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,其负极是___________ ,正极上 能够观察到的现象是____________________ ,正极的电极反应式是___________________ 。原电池工作一段时间后,若消耗锌6.5 g,则放出标准状况下气体__________ L。
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是

(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,其负极是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在容器体积可变的密闭容器中,反应N2(g) 3H2(g)
3H2(g)  2NH3(g)在一定条件下达到平衡。
2NH3(g)在一定条件下达到平衡。
完成下列填空:
(1)若该反应经过2秒钟后达到平衡,NH3的浓度增加了0.4mol/L,在此期间,正反应速率 (H2)的值为
(H2)的值为( )
A 0.6mol/(L·s) B 0.45 mol/(L·s) C 0.3 mol/(L·s) D 0.2 mol/(L·s)
(2)在其他条件不变的情况下,增大容器体积以减小反应体系的压强,
____ (选填“增大”、“减小”,下同),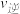
____ ,平衡向____ 方向移动(选填“正反应”、“逆反应”)。

(3)在其他条件不变的情况下,升高温度平衡向逆反应方向移动,则正反应为____ 反应(选填“吸热”、“放热”)。
(4)如图为反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是___ (填写编号)。
a.增大H2的浓度 b.缩小容器体积 c.加入催化剂 d.升高温度
改变条件后,平衡混合物中NH3的百分含量____ (选填“增大”、“减小”、“不变”)。在一定条件下,反应2A+B C达到平衡。
C达到平衡。
(5)若升高温度,平衡向正反应方向移动,则逆反应是_________ 热反应;
(6)若增加或减少B时,平衡不移动,则B是_________ 态;
(7)若A、B、C均为气态,将6mol A、3mol B充入容积为0.5L的密闭容器中,进行反应。经5s后,测得容器内有1mol B,则用A表示的反应速率为_________________________ , 5s末时C的物质的量浓度为__________________ 。
 3H2(g)
3H2(g)  2NH3(g)在一定条件下达到平衡。
2NH3(g)在一定条件下达到平衡。完成下列填空:
(1)若该反应经过2秒钟后达到平衡,NH3的浓度增加了0.4mol/L,在此期间,正反应速率
 (H2)的值为
(H2)的值为A 0.6mol/(L·s) B 0.45 mol/(L·s) C 0.3 mol/(L·s) D 0.2 mol/(L·s)
(2)在其他条件不变的情况下,增大容器体积以减小反应体系的压强,


(3)在其他条件不变的情况下,升高温度平衡向逆反应方向移动,则正反应为
(4)如图为反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是
a.增大H2的浓度 b.缩小容器体积 c.加入催化剂 d.升高温度
改变条件后,平衡混合物中NH3的百分含量
 C达到平衡。
C达到平衡。(5)若升高温度,平衡向正反应方向移动,则逆反应是
(6)若增加或减少B时,平衡不移动,则B是
(7)若A、B、C均为气态,将6mol A、3mol B充入容积为0.5L的密闭容器中,进行反应。经5s后,测得容器内有1mol B,则用A表示的反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
甲醇的合成:在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应如下:CO(g)+2H2(g)⇌CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
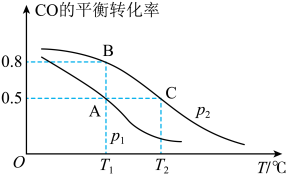
(1)A、B两点对应的压强大小关系是PA___________ PB(填“>、<、=”)。
(2)A、B、C三点的平衡常数KA,KB,KC的大小关系是___________ 。
(3)下列叙述能说明上述反应能达到化学平衡状态的是___________ (填代号)。
a、H2的消耗速率是CH3OH生成速率的2倍
b、CH3OH的体积分数不再改变
c、混合气体的密度不再改变
d、CO和CH3OH的物质的量之和保持不变
(4)在P1压强、T1℃时,经5min达到化学平衡,则用氢气表示该反应的化学速率v(H2)=___________ ,再加入1.0molCO后重新到达平衡,则CO的转化率___________ (填“增大,不变,减小”)。
甲醇的合成:在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应如下:CO(g)+2H2(g)⇌CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。

(1)A、B两点对应的压强大小关系是PA
(2)A、B、C三点的平衡常数KA,KB,KC的大小关系是
(3)下列叙述能说明上述反应能达到化学平衡状态的是
a、H2的消耗速率是CH3OH生成速率的2倍
b、CH3OH的体积分数不再改变
c、混合气体的密度不再改变
d、CO和CH3OH的物质的量之和保持不变
(4)在P1压强、T1℃时,经5min达到化学平衡,则用氢气表示该反应的化学速率v(H2)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是__
A 电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B 高温使水分解制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
C 太阳光催化分解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
D 天然气制氢:CH4+H2O CO+3H2
CO+3H2
(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1molCO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H=﹣49.0kJ•mol﹣1,测得CO2和CH3OH(g)的浓度随时间变化如图所示.
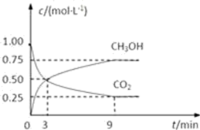
①从3min到9min,v(H2)=__ mol•L﹣1•min﹣1
②能说明上述反应达到平衡状态的是__ (填编号).
A 反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B 混合气体的密度不随时间的变化而变化
C 单位时间内消耗3mol H2,同时生成1mol H2O
D CO2的体积分数在混合气体中保持不变.
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是
A 电解水制氢:2H2O
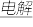 2H2↑+O2↑
2H2↑+O2↑B 高温使水分解制氢:2H2O
 2H2↑+O2↑
2H2↑+O2↑C 太阳光催化分解水制氢:2H2O
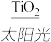 2H2↑+O2↑
2H2↑+O2↑D 天然气制氢:CH4+H2O
 CO+3H2
CO+3H2(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1molCO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H=﹣49.0kJ•mol﹣1,测得CO2和CH3OH(g)的浓度随时间变化如图所示.

①从3min到9min,v(H2)=
②能说明上述反应达到平衡状态的是
A 反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B 混合气体的密度不随时间的变化而变化
C 单位时间内消耗3mol H2,同时生成1mol H2O
D CO2的体积分数在混合气体中保持不变.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(一)将等物质的量的A和B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)=xC(g)+2D(g),5 min 后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=1∶2,C的反应速率是 0.15 mol·L-1·min-1。
(1)B的反应速率v(B)=_______ ,x=_______ 。
(2)A在5 min末的浓度是_______ 。
(3)此时容器内的压强与开始时之比为_______ 。
(二)计算下列化学反应的速率:
(4)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L-1·min-1,则以物质B表示此反应的化学反应速率为_______ mol·L-1·min-1。
(5)一定温度下,将1 mol N2O4充入体积为1 L的密闭容器中,反应3s后,NO2的物质的量为0.6 mol,则0~3s内的平均反应速率v(NO2) =_______ mol·L-1·s-1。
(6)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的反应速率为_______ 。
(1)B的反应速率v(B)=
(2)A在5 min末的浓度是
(3)此时容器内的压强与开始时之比为
(二)计算下列化学反应的速率:
(4)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L-1·min-1,则以物质B表示此反应的化学反应速率为
(5)一定温度下,将1 mol N2O4充入体积为1 L的密闭容器中,反应3s后,NO2的物质的量为0.6 mol,则0~3s内的平均反应速率v(NO2) =
(6)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】1.工业合成氨反应:N2+3H2 2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
(1)已知1 mol N2完全反应生成NH3可放出92kJ热量。如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是___________________________________ 。
(2)实验室模拟工业合成氨时,在容积为2 L的密闭容器内,反应经过10 min后,生成10 mol NH3,则用N2表示的化学反应速率为_______________ 。
(3)一定条件下,当合成氨的反应达到化学平衡时,下列说法正确的是_____________ 。
a.正反应速率和逆反应速率相等 b.正反应速率最大,逆反应速率为0
c.该条件下,N2的转化率达到最大值 d.N2和H2的浓度相等
e.N2、H2和NH3的体积分数相等 f.恒容时体系压强保持不变
1.在四个不同容器中,不同条件下进行合成氨反应。根据在相同时间内测定的结果,判断该反应的速率由大到小的顺序是__________________________ (用编号填写)。
A.V(NH3)=0.5 mol •L-1-•min-1 B.V(H2)=0.3 mol •L-1-•min-1
C.V(N2)=0.2 mol •L-1-•min-1 D.V(H2)=0.01 mol •L-1-• s -1
 2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。(1)已知1 mol N2完全反应生成NH3可放出92kJ热量。如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是
(2)实验室模拟工业合成氨时,在容积为2 L的密闭容器内,反应经过10 min后,生成10 mol NH3,则用N2表示的化学反应速率为
(3)一定条件下,当合成氨的反应达到化学平衡时,下列说法正确的是
a.正反应速率和逆反应速率相等 b.正反应速率最大,逆反应速率为0
c.该条件下,N2的转化率达到最大值 d.N2和H2的浓度相等
e.N2、H2和NH3的体积分数相等 f.恒容时体系压强保持不变
1.在四个不同容器中,不同条件下进行合成氨反应。根据在相同时间内测定的结果,判断该反应的速率由大到小的顺序是
A.V(NH3)=0.5 mol •L-1-•min-1 B.V(H2)=0.3 mol •L-1-•min-1
C.V(N2)=0.2 mol •L-1-•min-1 D.V(H2)=0.01 mol •L-1-• s -1
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段反应速率最大:_____ min(填0~1、1~2、2~3、3~4、4~5),原因是________ 。
②求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率___________________ (设溶液体积不变)。
(2)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
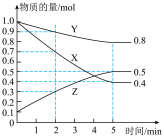
①该反应的化学方程式是___________ 。
②该反应达到平衡状态的标志是________
A.X的浓度不再改变
B.生成1mol Y的同时消耗2mol Z
C.Y的体积分数在混合气体中保持不变
D.容器内气体的总质量保持不变
③2min内Y的转化率为_________ 。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 50 | 120 | 232 | 290 | 310 |
②求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率
(2)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②该反应达到平衡状态的标志是
A.X的浓度不再改变
B.生成1mol Y的同时消耗2mol Z
C.Y的体积分数在混合气体中保持不变
D.容器内气体的总质量保持不变
③2min内Y的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在一固定容积的密闭容器中,充入2 mol CO2和1 mol H2发生如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数与温度(T)的关系如表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=__________ 。
(2)若反应在830℃下达到平衡,则CO2气体的转化率为_________ 。
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则容器内气体温度_________ (填“升高”、“降低”或“不能确定”)。
(4)在830℃达平衡后在其容器中分别又充入1 mol CO2 和1 molCO后,该反应的v正__ v逆(填“大于”“小于”“等于”)。
| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)若反应在830℃下达到平衡,则CO2气体的转化率为
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则容器内气体温度
(4)在830℃达平衡后在其容器中分别又充入1 mol CO2 和1 molCO后,该反应的v正
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业尾气H2S对环境和人体健康会产生严重危害,回收H2S制备高附加值的硫磺是保护环境和资源利用的有效措施。
已知:2H2S(g)⇌2H2(g)+S2(g) △H=+169.8kJ/mol。
回答下列问题:
(1)上述反应中相关键能数据:
①反应能自发进行的条件是___________ ,a=___________  。
。
②在恒温恒容密闭容器中,充入一定量 气体发生上述反应,下列说法正确的是
气体发生上述反应,下列说法正确的是___________ (填标号)。
A. 的体积分数不再改变,说明该反应达到平衡
的体积分数不再改变,说明该反应达到平衡
B. 与
与 体积比不再改变,说明该反应达到平衡
体积比不再改变,说明该反应达到平衡
C.平衡时向容器中充入情性气体,平衡正向移动
D.平衡时向容器中充入 和
和 ,再达平衡时,
,再达平衡时, 不变
不变
(2)保持压强恒定为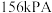 ,向密闭容器中充入
,向密闭容器中充入 和
和 (
( 不参与反应)发生上述反应,
不参与反应)发生上述反应, 的平衡转化率
的平衡转化率 ]与通入气体中
]与通入气体中 、温度
、温度 关系如下图所示。
关系如下图所示。

①从反应开始至反应体系分别达到M、N点状态,平均反应速率较快的是达到___________ (填“M”或“N”)的过程。
②相同温度下,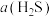 随着x增大而减小,其原因是
随着x增大而减小,其原因是___________ 。
已知:2H2S(g)⇌2H2(g)+S2(g) △H=+169.8kJ/mol。
回答下列问题:
(1)上述反应中相关键能数据:
| 化学键 |  |  |  |
键能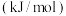 | a | 329 | 436 |
 。
。②在恒温恒容密闭容器中,充入一定量
 气体发生上述反应,下列说法正确的是
气体发生上述反应,下列说法正确的是A.
 的体积分数不再改变,说明该反应达到平衡
的体积分数不再改变,说明该反应达到平衡B.
 与
与 体积比不再改变,说明该反应达到平衡
体积比不再改变,说明该反应达到平衡C.平衡时向容器中充入情性气体,平衡正向移动
D.平衡时向容器中充入
 和
和 ,再达平衡时,
,再达平衡时, 不变
不变(2)保持压强恒定为
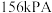 ,向密闭容器中充入
,向密闭容器中充入 和
和 (
( 不参与反应)发生上述反应,
不参与反应)发生上述反应, 的平衡转化率
的平衡转化率 ]与通入气体中
]与通入气体中 、温度
、温度 关系如下图所示。
关系如下图所示。
①从反应开始至反应体系分别达到M、N点状态,平均反应速率较快的是达到
②相同温度下,
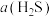 随着x增大而减小,其原因是
随着x增大而减小,其原因是
您最近一年使用:0次

 (
(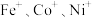 等)与
等)与 反应可得
反应可得 。
。 反应能高选择性地生成甲醇。分别在
反应能高选择性地生成甲醇。分别在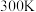 和
和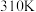 下(其他反应条件相同)进行反应
下(其他反应条件相同)进行反应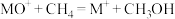 ,结果如下图所示。图中
,结果如下图所示。图中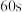 时
时